填空题 较易0.85 引用1 组卷149
(1)联氨(又称肼,N2H4,无色液体)为二元弱碱,在水中的电离方式与氨相似。写出在水中联氨第一步电离反应的方程式_______________ 。氯化镁溶液在某条件下可生Mg(OH)Cl沉淀,请写出相关离子方程式_________
(2)实验室可通过向盛装有碱石灰的锥形瓶中滴加浓氨水来制取氨气,请利用相关化学反应原理来解释______________________________
(3)室温下向10mL0.1 mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如图所示

则HA为_______ 电解质(填“强”或“弱”),a点所示溶液c(Na)_____ c(A)(填“>”、“<”或“”=),a、b两点所示溶液中水的电离程度a_______ b(填“>”、“<”或“"=)。
(4)25℃时0.05mol/L的醋酸溶液,pH=______ 该溶液中水电离出的c(H+)=____ (已知室温下醋酸电离平衡常数为2.0×10-5)
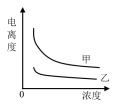
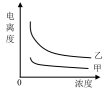
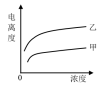
(5)常温下,0.01mol/L的HCN溶液加水稀释1000倍的过程中,下列选项增大的是_____
A. B.Kac(HCN) C.
B.Kac(HCN) C. D.
D.
(2)实验室可通过向盛装有碱石灰的锥形瓶中滴加浓氨水来制取氨气,请利用相关化学反应原理来解释
(3)室温下向10mL0.1 mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如图所示

则HA为
(4)25℃时0.05mol/L的醋酸溶液,pH=
(5)常温下,0.01mol/L的HCN溶液加水稀释1000倍的过程中,下列选项增大的是
A.
19-20高二上·广东广州·期中
类题推荐
已知水在25℃和95℃时的电离平衡曲线分别如下图所示:
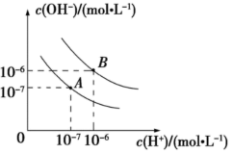
(1)25℃时水的电离平衡曲线应为_________ (填“A”或“B”)。
(2)95℃时,某溶液中由水电离出c(H+)=1×10-10mol/L,该溶液pH为_________ 。
(3)25℃时,向0.01mol·L-1、pH=2的NaHA溶液中加入NaOH溶液,请写出反应的离子方程式_________ 。
(4)在曲线B对应的温度下,有下列四组溶液:
若将V1L溶液①和V2L④混合后溶液呈中性,则V1_________ V2(填“>”=“”或“<”);若对溶液①②③④分别加水稀释10倍,则所得溶液pH由大到小排序为_________ (填序号);若向VL溶液②中逐滴加入溶液③,下列各选项中数值变大的有_________ (填序号);
A. B.
B. C.
C. D.
D.
(5)25℃时,将nmol•L-1的氨水与0.2mol•L-1的盐酸等体积混合反应,溶液中 时溶液显
时溶液显_________ 性(填“酸”、“碱”或“中”),NH3•H2O的电离常数Kb=_________ (用含n的代数式表示)。

(1)25℃时水的电离平衡曲线应为
(2)95℃时,某溶液中由水电离出c(H+)=1×10-10mol/L,该溶液pH为
(3)25℃时,向0.01mol·L-1、pH=2的NaHA溶液中加入NaOH溶液,请写出反应的离子方程式
(4)在曲线B对应的温度下,有下列四组溶液:
| 序号 | ① | ② | ③ | ④ |
| 溶液 | 氢氧化钠溶液 | 氨水 | 盐酸 | 醋酸 |
| pH | 9 | 9 | 3 | 3 |
A.
(5)25℃时,将nmol•L-1的氨水与0.2mol•L-1的盐酸等体积混合反应,溶液中
(1)已知常温时,0.1mol/L醋酸在水中有0.1%发生电离,则该溶液的pH=_____ ,醋酸的电离平衡常数Ka=______ 。
(2)向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如图所示:
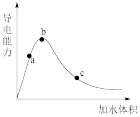
①a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是___ 。
②a、c两点对应的溶液分别吸收氨气,若两溶液最终pH均为7(25℃时),则a点溶液中的c(CH3COO-)_______ c点溶液中的c(NH4+)。(填“<”、“>”或“=”)
(3)25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
①H2CO3的第二级电离平衡常数的表达式Ka2=_______ 。
②25℃时,向0.1mol•L-1的氨水中缓缓通入CO2气体的过程中(忽略溶液体积的变化),下列表达式的数值变小的是___ 。
A. B.
B. C.
C. D.
D.
③向NaCN溶液中通入少量CO2气体,发生反应的离子方程式为___ 。
(2)向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如图所示:

①a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是
②a、c两点对应的溶液分别吸收氨气,若两溶液最终pH均为7(25℃时),则a点溶液中的c(CH3COO-)
(3)25℃时,部分物质的电离平衡常数如表所示:
| 化学式 | CH3COOH | NH3·H2O | H2CO3 | HCN |
| 电离平衡常数 | 1.7×10-5 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K=5.0×10-10 |
请回答下列问题:
①H2CO3的第二级电离平衡常数的表达式Ka2=
②25℃时,向0.1mol•L-1的氨水中缓缓通入CO2气体的过程中(忽略溶液体积的变化),下列表达式的数值变小的是
A.
③向NaCN溶液中通入少量CO2气体,发生反应的离子方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网