解答题-实验探究题 适中0.65 引用1 组卷90
请根据要求填写下列空白:
(1)NaHCO3溶液呈碱性的原因是______________ (用方程式和必要文字表示),写出该溶液存在的物料守恒的关系式 ________________ 。
(2)把AlCl3溶液蒸干、灼烧,最后得到的主要产物是________________________ 。
(3)若想除去CuCl2 溶液中混有FeCl3杂质,则往往加入试剂______________ 。
①NaOH ②NH3·H2O ③CuO ④CuCO3
(4)在酸碱滴定中,我们用0.1000mol/L HCl来滴定未知浓度的NaOH溶液,①在滴定过程中,操作或说法错误的是_______________ 。
a.滴定终点为:当滴完最后一滴恰好变色,且在半分钟内不恢复原色
b.进行中和滴定操作时,左手振荡锥形瓶,右手转动活塞控制液滴流速,眼睛要始终注视滴定管内溶液液面的变化
c.酸式滴定管中的盐酸装液前未经润洗,导致所测定的c(NaOH)偏低。
d.酸式滴定管在滴定前有气泡,滴定后气泡消失,导致所测定的c(NaOH)偏高
②某学生根据三次实验分别记录有关数据如下:
请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度:c(NaOH)=________________
(1)NaHCO3溶液呈碱性的原因是
(2)把AlCl3溶液蒸干、灼烧,最后得到的主要产物是
(3)若想除去CuCl2 溶液中混有FeCl3杂质,则往往加入试剂
①NaOH ②NH3·H2O ③CuO ④CuCO3
(4)在酸碱滴定中,我们用0.1000mol/L HCl来滴定未知浓度的NaOH溶液,①在滴定过程中,操作或说法错误的是
a.滴定终点为:当滴完最后一滴恰好变色,且在半分钟内不恢复原色
b.进行中和滴定操作时,左手振荡锥形瓶,右手转动活塞控制液滴流速,眼睛要始终注视滴定管内溶液液面的变化
c.酸式滴定管中的盐酸装液前未经润洗,导致所测定的c(NaOH)偏低。
d.酸式滴定管在滴定前有气泡,滴定后气泡消失,导致所测定的c(NaOH)偏高
②某学生根据三次实验分别记录有关数据如下:
| 滴定次数 | 待测氢氧化钠 溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度:c(NaOH)=
19-20高二上·山东淄博·期中
类题推荐
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视___ 。当滴入最后一滴___ 溶液,锥形瓶中颜色由___ 变成___ 且半分钟内不复原则为滴定终点。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是___ 。
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:所用盐酸溶液的体积为__ mL。

(4)某学生根据三次实验分别记录有关数据如表:
请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度c(NaOH)=___ (保留4位小数)
(5)酸性高锰酸钾溶液应该用___ 滴定管盛装(酸式或碱式)。
(6)若用氢氧化钠标准溶液滴定未知浓度的乙酸可用___ 指示剂。
(1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:所用盐酸溶液的体积为

(4)某学生根据三次实验分别记录有关数据如表:
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol·L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
(5)酸性高锰酸钾溶液应该用
(6)若用氢氧化钠标准溶液滴定未知浓度的乙酸可用
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液。
(1)若滴定开始和结束时,酸式滴定管中的液面如图所示:则所用盐酸的体积为__ mL。滴定终点时的现象是:当滴入最后一滴盐酸时,锥形瓶中溶液颜色由___ ,且30s不恢复原色。
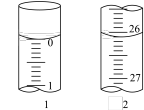
(2)某学生根据三次实验分别记录有关数据如下表:
请选用其中合理数据算出该氢氧化钠溶液物质的量浓度(计算结果保留4位有效数字):c(NaOH)=__ mol·L-1。
(3)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是__ (填字母)。
A.滴定前滴定管中有气泡,滴定后消失 B.碱式滴定管量取NaOH溶液时,未进行润洗操作
C.滴定时达到滴定终点时俯视读数 D.锥形瓶取用NaOH待测液前加少量水洗涤
(1)若滴定开始和结束时,酸式滴定管中的液面如图所示:则所用盐酸的体积为

(2)某学生根据三次实验分别记录有关数据如下表:
| 滴定次数 | 待测氢氧化钠 溶液的体积/mL | 0.1000mol·L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积 | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
(3)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是
A.滴定前滴定管中有气泡,滴定后消失 B.碱式滴定管量取NaOH溶液时,未进行润洗操作
C.滴定时达到滴定终点时俯视读数 D.锥形瓶取用NaOH待测液前加少量水洗涤
某学生欲用0.100 0 mol·L-1的盐酸来滴定未知浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用0.100 0 mol·L-1的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_______ 。直到因加入一滴盐酸后,溶液由红色变为无色,且_______ 为止。
(2)若滴定开始和结束时,酸式滴定管中的液面如图所示:则起始读数为_______ mL,终点读数为_______ mL。

(3)某学生根据三次实验分别记录有关数据如下:
请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度:c(NaOH)=_______ 。
(4)以下操作造成测定结果偏高的原因可能是_______ 。
A. 配制标准溶液的氢氧化钠中混有Na2CO3杂质
B. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C. 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E. 未用标准液润洗碱式滴定管
(1)用0.100 0 mol·L-1的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视
(2)若滴定开始和结束时,酸式滴定管中的液面如图所示:则起始读数为

(3)某学生根据三次实验分别记录有关数据如下:
| 滴定次数 | 氢氧化钠溶液/mL | 0.1000 mol·L-1盐酸的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗 | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
(4)以下操作造成测定结果偏高的原因可能是
A. 配制标准溶液的氢氧化钠中混有Na2CO3杂质
B. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C. 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E. 未用标准液润洗碱式滴定管
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


