解答题-原理综合题 较难0.4 引用1 组卷119
(1)氨是最重要的氮肥,是产量最大的化工产品之一。在1L密闭容器中,起始投入4mol N2和6mol H2在一定条件下生成NH3,平衡时仅改变温度测得的数据如表所示 (已知:T1<T2)
①则K1_______ K2 (填“>”、“<”或“=”),原因:__________ 。
②在T2下,经过10s达到化学平衡状态,则平衡时H2的转化率为______________ 。若再同时增加各物质的量为1mol,则该反应的速率v正_____ v逆(>或=或<),平衡常数将______ (填“增大”、“减小”或“不变)。
(2)一定温度下,将3mol A气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:
3A(g)+B(g) xC(g),请填写下列空白:
xC(g),请填写下列空白:
①反应1min时测得剩余1.8mol A,C的浓度为0.4 mol/L,则1min内B的反应速率为______ ,x为_______ 。
②若混合气体起始压强为P0,10min后达平衡,容器内混合气体总压强为P,用P0、P来表示达平衡时反应物A的转化率a(A)为__________ 。
③能够说明该反应达到平衡的标志是___________ 。
A 容器内混合气体的密度保持不变
B v(A)=3v(B)
C A、B的浓度之比为3:1
D 单位时间内消耗3 n molA的同时生成n mol B
E 体系的温度不再变化
| 温度 | 平衡时NH3的物质的量/mol |
| T1 | 3.6 |
| T2 | 2 |
①则K1
②在T2下,经过10s达到化学平衡状态,则平衡时H2的转化率为
(2)一定温度下,将3mol A气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:
3A(g)+B(g)
①反应1min时测得剩余1.8mol A,C的浓度为0.4 mol/L,则1min内B的反应速率为
②若混合气体起始压强为P0,10min后达平衡,容器内混合气体总压强为P,用P0、P来表示达平衡时反应物A的转化率a(A)为
③能够说明该反应达到平衡的标志是
A 容器内混合气体的密度保持不变
B v(A)=3v(B)
C A、B的浓度之比为3:1
D 单位时间内消耗3 n molA的同时生成n mol B
E 体系的温度不再变化
19-20高二上·广东广州·期中
类题推荐
Ⅰ、在 2L 密闭容器中,起始投入 4mol N2和 6mol H2 在一定条件下生成 NH3,平衡时仅改变温度测得的数据如表所示(已知:T1<T2)
(1)则 K1_______ K2(填“>”、“<”或“=”),原因:_______ 。
(2)在 T2下,经过 10s 达到化学平衡状态,则 0~10s 内 N2的平均速率 v(N2)为_______ , 平衡时 H2的转化率为_______ 。若同时再增加各物质的量为 1mol,该反应的 V 正_______ V 逆 (>或=或<),平衡常数将_______ (填“增大”、“减小”或“不变”)
(3)下列能说明该反应已达到平衡状态的是_______ 。
A.3v(H2)正=2v(NH3)逆
B. 容器内气体压强不变
C.混合气体的平均相对分子质量不再改变的状态
D. ΔH 保持不变
Ⅱ、甲烷蒸气转化法制H2的主要反应为:CH4(g)+H2O(g)⇌CO(g)+3H2(g)。在恒容密闭容器中充入 2mol CH4和H2O(g)的混合气体,且 CH4 和H2O(g)的物质的量之比为x,相同温度下达到平衡时测得H2 的体积分数 φ(H2)与 x 的关系如图所示。
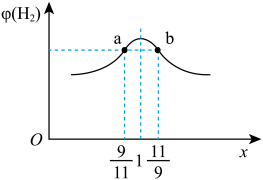
则 CH4的转化率:a点_______ (填“>”“=”或“<”,下同)b 点,CH4(g)的浓度:a点_______ b 点,氢气的产率:a 点_______ b 点。
| 温度/K | 平衡时NH3的物质的量/mol |
| T1 | 3.6 |
| T2 | 2 |
(2)在 T2下,经过 10s 达到化学平衡状态,则 0~10s 内 N2的平均速率 v(N2)为
(3)下列能说明该反应已达到平衡状态的是
A.3v(H2)正=2v(NH3)逆
B. 容器内气体压强不变
C.混合气体的平均相对分子质量不再改变的状态
D. ΔH 保持不变
Ⅱ、甲烷蒸气转化法制H2的主要反应为:CH4(g)+H2O(g)⇌CO(g)+3H2(g)。在恒容密闭容器中充入 2mol CH4和H2O(g)的混合气体,且 CH4 和H2O(g)的物质的量之比为x,相同温度下达到平衡时测得H2 的体积分数 φ(H2)与 x 的关系如图所示。

则 CH4的转化率:a点
(1)在2L密闭容器中,起始投入4molN2和6molH2在一定条件下生成NH3,平衡时仅改变温度测得的数据如表所示(已知:T1<T2)
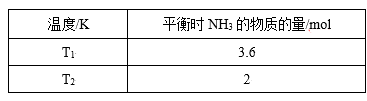
①则K1___ K2(填“>”、“<”或“=”),原因:__ 。
②在T2下,经过10s达到化学平衡状态,则0~10s内N2的平均速率v(N2)为__ ,平衡时H2的转化率为__ 。若再同时增加各物质的量为1mol,该反应的平衡V正__ V逆(>或=或<);平衡常数将__ (填“增大”、“减小”或“不变”)
③下列能说明该反应已达到平衡状态的是__ 。
A.3v(H2)正=2v(NH3)逆 B.容器内气体压强不变
C.混合气体的平均相对分子质量不再改变的状态 D.ΔH保持不变
(2)已知下列化学键的键能写出工业上制氨的热化学方程式:
热化学方程式:___ 。

①则K1
②在T2下,经过10s达到化学平衡状态,则0~10s内N2的平均速率v(N2)为
③下列能说明该反应已达到平衡状态的是
A.3v(H2)正=2v(NH3)逆 B.容器内气体压强不变
C.混合气体的平均相对分子质量不再改变的状态 D.ΔH保持不变
(2)已知下列化学键的键能写出工业上制氨的热化学方程式:
| 化学键 | H-H | N≡N | N-H |
| 键能/kJ·mol-1 | 430 | 936 | 390 |
热化学方程式:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


