解答题-原理综合题 适中0.65 引用1 组卷93
甲烷是非常重要的能源和化工原料,请回答下列问题。
(1)用CH4催化还原NOx可以消除氮氧化物的污染。例如:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1,CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1,写出CH4还原NO2至N2的热化学方程式:_____ 。
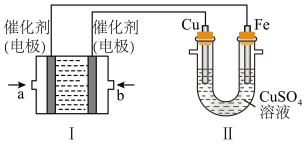
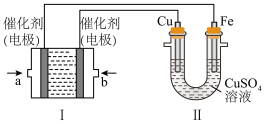
(2)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒镀铜。
①a处应通入______ (填“CH4”或“O2”),a处电极上发生的电极反应式是 ___________ 。
②电镀结束后,装置Ⅱ中Cu2+的物质的量浓度____ (填写“变大”“变小”或“不变”)。
③若实验过程中Ⅱ中的铜片质量减少了1.28g,则Ⅰ中理论上消耗CH4的体积(标准状况)__ _L。
(3)若将题(2)装置Ⅱ中的两电极均改为石墨惰性电极 ,电解质溶液仍为CuSO4溶液。
①写出装置Ⅱ中发生的总化学反应方程式_________ 。
②电解硫酸铜溶液一段时间后,装置Ⅱ中溶液的pH____ (填写“变大”“变小”或“不变”);要使原溶液复原,可向电解后的溶液中加入_______ 。
(1)用CH4催化还原NOx可以消除氮氧化物的污染。例如:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1,CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1,写出CH4还原NO2至N2的热化学方程式:
(2)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒镀铜。
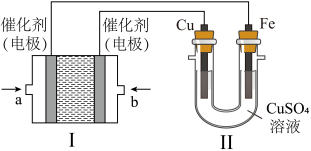
①a处应通入
②电镀结束后,装置Ⅱ中Cu2+的物质的量浓度
③若实验过程中Ⅱ中的铜片质量减少了1.28g,则Ⅰ中理论上消耗CH4的体积(标准状况)
(3)若将题(2)装置Ⅱ中的两电极均改为石墨
①写出装置Ⅱ中发生的总化学反应方程式
②电解硫酸铜溶液一段时间后,装置Ⅱ中溶液的pH
19-20高二上·福建宁德·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网