解答题-原理综合题 适中0.65 引用1 组卷82
工业废气、汽车尾气排放出的NOx、SO2等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
(1)已知:①CO燃烧热为283.0kJ·mol-l,②N2(g)+O2(g) ==2NO(g) △H=+180.5kJ·mol-1,汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应,能消除污染,写出该反应的热化学方程式_________________________________________________________
(2)将0.20mol NO和0.10molCO充入一个容积恒定为1L的密闭容器中发生上述反应,反应过程中部分物质的浓度变化如下图所示.
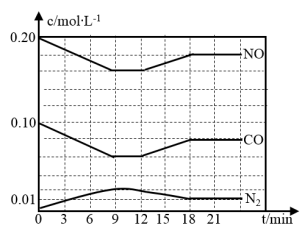
①该反应第一次达到平衡时的平衡常数为________ 。
②第12min时改变的条件是________ 。
③在第24min时,若保持温度不变,再向容器中充入CO和N2各0.060mol,平衡将________ 移动(填“正向”、“逆向”或“不”).
(3)SNCR-SCR脱硝技术是一种新型的除去烟气中氮氧化物的脱硝技术,一般采用氨气或尿素。
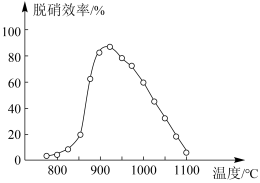
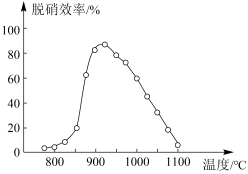
①SNCR脱硝技术中:在催化剂作用下用NH3作还原剂还原NO,其主要反应为:4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g),△H<0。体系温度直接影响SNCR技术的脱硝效率,如图所示。当体系温度约为925℃时,SNCR脱硝效率最高,其可能的原因是________ 。

②SCR脱硝技术中则用尿素[CO(NH2)2]作还原剂还原NO2的化学方程式为____________
(1)已知:①CO燃烧热为283.0kJ·mol-l,②N2(g)+O2(g) ==2NO(g) △H=+180.5kJ·mol-1,汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应,能消除污染,写出该反应的热化学方程式
(2)将0.20mol NO和0.10molCO充入一个容积恒定为1L的密闭容器中发生上述反应,反应过程中部分物质的浓度变化如下图所示.

①该反应第一次达到平衡时的平衡常数为
②第12min时改变的条件是
③在第24min时,若保持温度不变,再向容器中充入CO和N2各0.060mol,平衡将
(3)SNCR-SCR脱硝技术是一种新型的除去烟气中氮氧化物的脱硝技术,一般采用氨气或尿素。
①SNCR脱硝技术中:在催化剂作用下用NH3作还原剂还原NO,其主要反应为:4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g),△H<0。体系温度直接影响SNCR技术的脱硝效率,如图所示。当体系温度约为925℃时,SNCR脱硝效率最高,其可能的原因是

②SCR脱硝技术中则用尿素[CO(NH2)2]作还原剂还原NO2的化学方程式为
19-20高二上·河南南阳·阶段练习
类题推荐
氮氧化物排放是形成臭氧层空洞、酸雨、雾霾的重要成因之一
I.NO和CO气体均为汽车尾气的成分,目前降低尾气的可行方法是在汽车排气管上安装催化转化器,这两种气体在催化转换器中发生反应:2CO(g)+2NO(g) N2(g)+2CO2(g) △H
N2(g)+2CO2(g) △H
已知反应中相关键能数据如下:
(1)由此计算△H=__________ 。
(2)在一定温度下,将2.0molNO、2.4molCO通入到容积固定为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示:
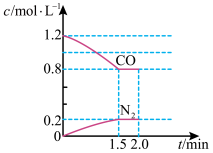
①有害气体NO的转化率为__________ 。
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件可能是__________ (填序号)。
a.缩小容器体积 b.催化剂 c.降低温度 d.再通入2.0molNO
③ 若保持反应体系的温度不变,20min时再向容器中充入NO、N2各0.4mol,平衡将__________ (填“正向” 或“逆向”)移动。
Ⅱ.SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为:4NO(g)+4NH3(g)+O2(g) 4N2(g)+6H2O(g) △H<0
(3)该法可能发生副反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ,减少副反应的主要措施是
4NO(g)+6H2O(g) ,减少副反应的主要措施是___________ (写一条即可)。
(4)其他条件相同,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图。
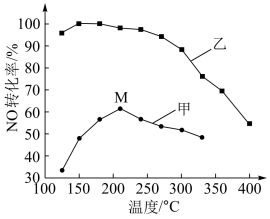
①工业上选择催化剂__________ (填“甲”或“乙”),原因是____________ 。
②在催化剂甲作用下,图中M点处(对应温度为210℃)NO的转化率______ (填“可能是”、“一定是”或“一定不是”) 该温度下的平衡转化率。高于210℃时,NO转化率降低的原因可能是__________ 。(写一条即可)
I.NO和CO气体均为汽车尾气的成分,目前降低尾气的可行方法是在汽车排气管上安装催化转化器,这两种气体在催化转换器中发生反应:2CO(g)+2NO(g)
已知反应中相关键能数据如下:
| 化学键 | C | N≡O | N≡N | C=O |
| 键能/kJ·mol-1 | 1076 | 632 | 946 | 750 |
(2)在一定温度下,将2.0molNO、2.4molCO通入到容积固定为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示:

①有害气体NO的转化率为
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件可能是
a.缩小容器体积 b.催化剂 c.降低温度 d.再通入2.0molNO
③ 若保持反应体系的温度不变,20min时再向容器中充入NO、N2各0.4mol,平衡将
Ⅱ.SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为:4NO(g)+4NH3(g)+O2(g) 4N2(g)+6H2O(g) △H<0
(3)该法可能发生副反应4NH3(g)+5O2(g)
(4)其他条件相同,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图。

①工业上选择催化剂
②在催化剂甲作用下,图中M点处(对应温度为210℃)NO的转化率
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网