解答题-实验探究题 适中0.65 引用1 组卷52
碳酸镁晶体是一种新型吸波隐形材料中的增强剂。
实验一:合成碳酸镁晶体的步骤:
①配制一定浓度的MgSO4溶液和NH4HCO3溶液;
②量取一定量的NH4 HCO3溶液于容器中,搅拌并逐滴加入MgSO4溶液,控制温度50℃,反应一段时间;
③用氨水调节溶液pH至9.5,放置一段时间后,过滤、洗涤、干燥得碳酸镁晶体产品。
称取3.000gMgSO4样品配制250mL溶液流程如图所示:
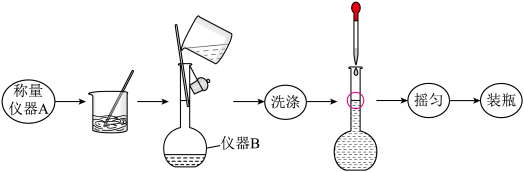
回答下列问题:
(1)写出实验仪器名称:A_____ ;B_____ 。配制溶液过程中定容后的“摇匀”的实验操作为______ 。
(2)检验碳酸镁晶体是否洗干净的方法是_________ 。
实验二:测定产品MgCO3·nH2O中的n值(仪器和药品如图所示):
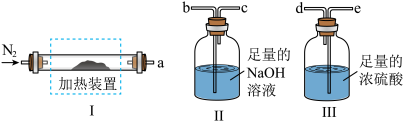
(3)实验二装置的连接顺序为_____ (按气流方向,用接口字母abcde表示),其中Ⅱ装置的作用是_____ 。
(4)加热前先通入N2排尽装置Ⅰ中的空气,然后称取装置Ⅱ、Ⅲ的初始质量。进行加热时还需通入N2的作用是______ 。
(5)若要准确测定n值,至少需要下列所给数据中的_____ (填选项字母),写出相应1种组合情景下,求算n值的数学表达式:n=______ 。
a.装置Ⅰ反应前后质量差m1 b.装置Ⅱ反应前后质量差m2 c.装置Ⅲ反应前后质量差m3
实验一:合成碳酸镁晶体的步骤:
①配制一定浓度的MgSO4溶液和NH4HCO3溶液;
②量取一定量的NH4 HCO3溶液于容器中,搅拌并逐滴加入MgSO4溶液,控制温度50℃,反应一段时间;
③用氨水调节溶液pH至9.5,放置一段时间后,过滤、洗涤、干燥得碳酸镁晶体产品。
称取3.000gMgSO4样品配制250mL溶液流程如图所示:

回答下列问题:
(1)写出实验仪器名称:A
(2)检验碳酸镁晶体是否洗干净的方法是
实验二:测定产品MgCO3·nH2O中的n值(仪器和药品如图所示):

(3)实验二装置的连接顺序为
(4)加热前先通入N2排尽装置Ⅰ中的空气,然后称取装置Ⅱ、Ⅲ的初始质量。进行加热时还需通入N2的作用是
(5)若要准确测定n值,至少需要下列所给数据中的
a.装置Ⅰ反应前后质量差m1 b.装置Ⅱ反应前后质量差m2 c.装置Ⅲ反应前后质量差m3
2016·上海长宁·二模
类题推荐
碳酸镁晶须是一种新型的吸波隐形材料中的增强材料。
(1)合成该物质的步骤如下:
步骤1:配制0.5mol·L-1 MgSO4溶液和0.5mol·L-1 NH4HCO3溶液。
步骤2:用量筒量取500mL NH4HCO3溶液于1000mL三颈烧瓶中,开启搅拌器。温度控制在50℃。
步骤3:将250mL MgSO4溶液逐滴加入NH4HCO3溶液中,1min内滴加完后,用氨水调节溶液pH到9.5。
步骤4:放置1h后,过滤,洗涤。
步骤5:在40℃的真空干燥箱中干燥10h,得碳酸镁晶须产品(MgCO3·nH2O n=1~5)。
①步骤2控制温度在50℃,较好的加热方法是_________ 。
②步骤3生成MgCO3·nH2O沉淀的化学方程式为__________ 。
③步骤4检验沉淀是否洗涤干净的方法是__________ 。
(2)测定生成的MgCO3·nH2O中的n值。
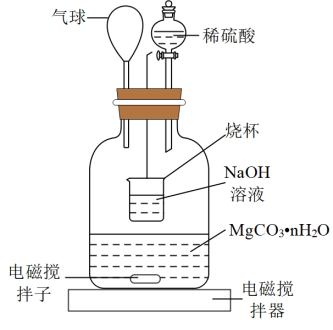
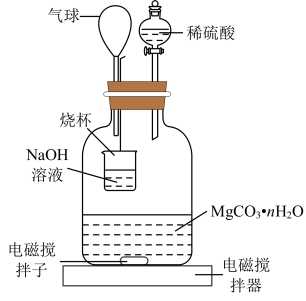
称量1.000碳酸镁晶须,放入如图所示的广口瓶中加入适量水,并滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5h,反应后期将温度升到30℃,最后将烧杯中的溶液用已知浓度的盐酸滴定,测得CO2的总量;重复上述操作2次。

①图中气球的作用是_________ 。
②上述反应后期要升温到30℃,主要目的是______ 。
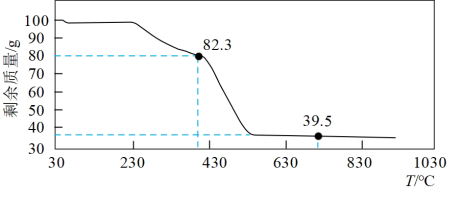
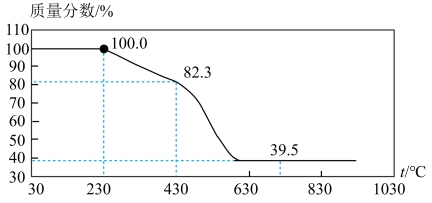
③测得每7.8000g碳酸镁晶须产生标准状况下CO2为1.12L,则n值为_______ 。
(3)碳酸镁晶须可由菱镁矿获得,为测定某菱镁矿(主要成分是碳酸镁,含少量碳酸亚铁、二氧化硅)中铁的含量,在实验室分别称取12.5g菱镁矿样品溶于过量的稀硫酸并完全转移到锥形瓶中,加入指示剂,用0.010mol/L H2O2溶液进行滴定。平行测定四组。消耗H2O2溶液的体积数据如表所示。
①H2O2溶液应装在_________ (填“酸式”或“碱式”)滴定管中。
②根据表中数据,可计算出菱镁矿中铁元素的质量分数为_________ %(保留小数点后两位)。
(1)合成该物质的步骤如下:
步骤1:配制0.5mol·L-1 MgSO4溶液和0.5mol·L-1 NH4HCO3溶液。
步骤2:用量筒量取500mL NH4HCO3溶液于1000mL三颈烧瓶中,开启搅拌器。温度控制在50℃。
步骤3:将250mL MgSO4溶液逐滴加入NH4HCO3溶液中,1min内滴加完后,用氨水调节溶液pH到9.5。
步骤4:放置1h后,过滤,洗涤。
步骤5:在40℃的真空干燥箱中干燥10h,得碳酸镁晶须产品(MgCO3·nH2O n=1~5)。
①步骤2控制温度在50℃,较好的加热方法是
②步骤3生成MgCO3·nH2O沉淀的化学方程式为
③步骤4检验沉淀是否洗涤干净的方法是
(2)测定生成的MgCO3·nH2O中的n值。
称量1.000碳酸镁晶须,放入如图所示的广口瓶中加入适量水,并滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5h,反应后期将温度升到30℃,最后将烧杯中的溶液用已知浓度的盐酸滴定,测得CO2的总量;重复上述操作2次。

①图中气球的作用是
②上述反应后期要升温到30℃,主要目的是
③测得每7.8000g碳酸镁晶须产生标准状况下CO2为1.12L,则n值为
(3)碳酸镁晶须可由菱镁矿获得,为测定某菱镁矿(主要成分是碳酸镁,含少量碳酸亚铁、二氧化硅)中铁的含量,在实验室分别称取12.5g菱镁矿样品溶于过量的稀硫酸并完全转移到锥形瓶中,加入指示剂,用0.010mol/L H2O2溶液进行滴定。平行测定四组。消耗H2O2溶液的体积数据如表所示。
| 实验编号 | 1 | 2 | 3 | 4 |
| 消耗H2O2溶液体积/mL | 15.00 | 15.02 | 15.62 | 14.98 |
①H2O2溶液应装在
②根据表中数据,可计算出菱镁矿中铁元素的质量分数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网