填空题 适中0.65 引用2 组卷94
完成下列化学用语:
(1)画出 O2﹣结构示意图:_____ ,某种核素质量数 37,中子数 20,其原子符号:_____
(2)写出实验室制氯气的化学方程式:______________________
(3)工厂里常用浓氨水来检验氯气管道是否泄漏,其原理为:8NH3+3Cl2=6NH4Cl+N2,请用双线桥表示其电子转移的方向和数目__________________________________
(1)画出 O2﹣结构示意图:
(2)写出实验室制氯气的化学方程式:
(3)工厂里常用浓氨水来检验氯气管道是否泄漏,其原理为:8NH3+3Cl2=6NH4Cl+N2,请用双线桥表示其电子转移的方向和数目
19-20高一上·浙江杭州·期中
类题推荐
阅读下面一段材料并回答问题。
(1) K2FeO4中铁元素的化合价为___________ 。
(2)下列关于K2FeO4的说法中,不正确的是___________ 。
a.是具有强氧化性的盐
b.固体保存时需要防潮
c.制备需要在碱性环境中进行
d.其消毒原理和净水原理相同
e.其用于饮用水消毒净化的优点有:作用快、安全性好、无异味
(3)消毒净化300m3的水,至少需要K2FeO4的质量为___________ kg。
(4)将K2FeO4与水反应的化学方程式配平并补充完整___________ 。
4K2FeO4+_________ H2O=_________ Fe(OH)3(胶体)+_________ KOH+_________
(5)高铁酸钠Na2FeO4是一种新型的净水剂,可以通过下述反应制取:
2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
①用双线桥法在方程式中标出电子转移的方向和数目___________ 。
②当反应中转移1mol电子时,生成的氧化产物的质量是___________ g(保留至小数点后一位)。
| 高铁酸钾使用说明书 【化学式】K2FeO4 【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着碱性减弱,稳定性下降,与水反应放出氧气 K2FeO4,通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用 【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放5mg K2FeO4,即可达到卫生标准…… |
(2)下列关于K2FeO4的说法中,不正确的是
a.是具有强氧化性的盐
b.固体保存时需要防潮
c.制备需要在碱性环境中进行
d.其消毒原理和净水原理相同
e.其用于饮用水消毒净化的优点有:作用快、安全性好、无异味
(3)消毒净化300m3的水,至少需要K2FeO4的质量为
(4)将K2FeO4与水反应的化学方程式配平并补充完整
4K2FeO4+_________ H2O=_________ Fe(OH)3(胶体)+_________ KOH+_________
(5)高铁酸钠Na2FeO4是一种新型的净水剂,可以通过下述反应制取:
2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
①用双线桥法在方程式中标出电子转移的方向和数目
②当反应中转移1mol电子时,生成的氧化产物的质量是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
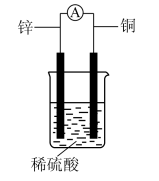
 CuSO4+SO2↑+2H2O,回答下列问题:
CuSO4+SO2↑+2H2O,回答下列问题:

