解答题-工业流程题 较难0.4 引用2 组卷289
氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如图。

请回答下列问题:
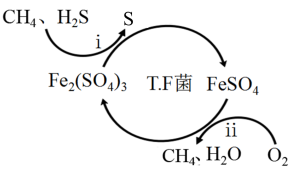
Ⅰ.转化脱硫:将天然气压入吸收塔,30℃时,在T·F菌作用下,酸性环境中脱硫过程示意图如图。
过程i的离子反应方程式为_____ 。
已知:①Fe3+在pH=1.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T·F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如表。
在转化脱硫中,请在表中选择最佳pH范围是____ <pH<____ ,这样选择的原因是:______ 。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合如图回答问题。
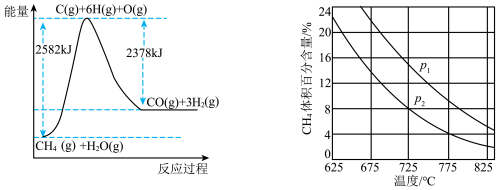
(3)①该过程的热化学方程式是_____ 。
②比较压强P1和P2的大小关系:P1____ P2(选填“<”、“>”或“=”)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.提纯:将CO2和H2分离得到H2的过程如示意图如图。
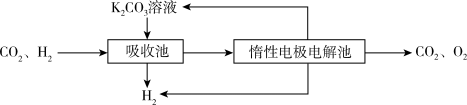
(4)吸收池中发生反应的离子方程式是______ 。

请回答下列问题:
Ⅰ.转化脱硫:将天然气压入吸收塔,30℃时,在T·F菌作用下,酸性环境中脱硫过程示意图如图。

过程i的离子反应方程式为
已知:①Fe3+在pH=1.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T·F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如表。
| pH | 0.7 | 1.1 | 1.5 | 1.9 | 2.3 | 2.7 |
| Fe2+的氧化速率 | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 |
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合如图回答问题。

(3)①该过程的热化学方程式是
②比较压强P1和P2的大小关系:P1
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.提纯:将CO2和H2分离得到H2的过程如示意图如图。

(4)吸收池中发生反应的离子方程式是
19-20高三上·河北秦皇岛·阶段练习
类题推荐
氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下图所示。

请回答下列问题:
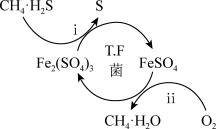
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程如图所示。
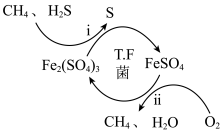
(1)过程i的氧化剂是_____________ 。
(2)过程ii的离子方程式是________________ 。
(3)已知:①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
请结合以上信息,判断工业脱硫应选择的最合适的pH范围是____ <pH<____ 。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。

(4)①该过程的热化学方程式是____________________ 。
②比较压强p1和p2的大小关系:p1____ p2(选填“>”、“<”或“=”)。
③在一定温度和一定压强下的体积可变的密闭容器中充入1mol CH4和1mol水蒸气充分反应达平衡后,测得起始时混合气体的密度是平衡时混合气体密度的1.4倍,则CH4的转化率为________ 。

请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程如图所示。

(1)过程i的氧化剂是
(2)过程ii的离子方程式是
(3)已知:①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
| pH | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.4 | 2.7 | 3.0 |
| Fe2+的氧化速率/g·L-1·h-1 | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 | 6.2 | 5.6 |
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。

(4)①该过程的热化学方程式是
②比较压强p1和p2的大小关系:p1
③在一定温度和一定压强下的体积可变的密闭容器中充入1mol CH4和1mol水蒸气充分反应达平衡后,测得起始时混合气体的密度是平衡时混合气体密度的1.4倍,则CH4的转化率为
氢气作为清洁能源有着广泛的应用前景,请回答下列问题:
Ⅰ.转化脱硫:将天然气压入吸收塔,30 ℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。
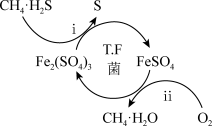
(1)过程ⅰ中H2S发生了_______ (填“氧化”或“还原”)反应。
(2)过程ⅱ的离子方程式是_______ 。
(3)已知:①Fe3+在pH为1.9时开始沉淀,3.2时沉淀完全。②30 ℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如表。
请结合以上信息,判断工业脱硫应选择的最佳pH范围为_______ ,并说明原因:_______ 。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合图回答问题。
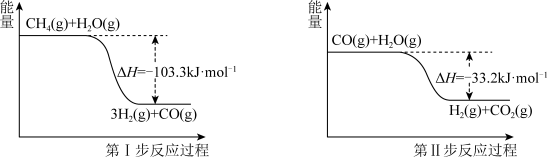
(4)写出甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式:_______ 。
(5)第Ⅱ步为可逆反应。在800 ℃时,恒容密闭容器中CO的起始浓度为a mol/L,水蒸气的起始浓度为1.5a mol/L,达到化学平衡状态后,CO平衡转化率为60%,则此反应的平衡常数为_______ 。
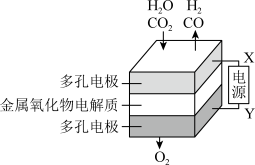
(6)在固态金属氧化物电解池中,高温共电解H2O—CO2混合气体制备H2和CO,基本原理如图所示,阴极的反应式是_______ 和CO2+2e—=CO+O2—。
Ⅰ.转化脱硫:将天然气压入吸收塔,30 ℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。

(1)过程ⅰ中H2S发生了
(2)过程ⅱ的离子方程式是
(3)已知:①Fe3+在pH为1.9时开始沉淀,3.2时沉淀完全。②30 ℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如表。
| pH | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.4 | 2.7 | 3.0 |
| Fe2+氧化速率/(g·L-1·h-1) | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 | 6.2 | 5.6 |
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合图回答问题。

(4)写出甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式:
(5)第Ⅱ步为可逆反应。在800 ℃时,恒容密闭容器中CO的起始浓度为a mol/L,水蒸气的起始浓度为1.5a mol/L,达到化学平衡状态后,CO平衡转化率为60%,则此反应的平衡常数为
(6)在固态金属氧化物电解池中,高温共电解H2O—CO2混合气体制备H2和CO,基本原理如图所示,阴极的反应式是

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网