单选题 较易0.85 引用8 组卷496
下列有关中和热实验的说法正确的是
| A.用铜丝替代环形玻璃搅拌棒,测得ΔH偏高 |
| B.强酸与强碱反应生成1 mol水的ΔH都约为-57.3 kJ·mol-1 |
| C.测定中和热实验中,读取混合溶液不再变化的温度为终止温度 |
| D.某同学通过实验测出稀盐酸和稀NaOH溶液反应的中和热ΔH=-52.3 kJ·mol-1,造成这一结果的原因不可能是:用测量盐酸的温度计直接测定NaOH溶液的温度 |
19-20高二上·浙江杭州·阶段练习
类题推荐
下列有关测定中和反应反应热实验的说法正确的是
| A.所有酸的稀溶液与所有碱的稀溶液反应生成1molH2O的ΔH均为-57.3kJ•mol-1 |
| B.中和热的测定实验中,氢氧化钠分批加入,反应更充分,测定的中和热数值误差更小 |
| C.测定中和反应反应热的实验中,混合溶液的温度不再变化时,该温度为终止温度 |
| D.某同学通过实验测出稀盐酸和稀NaOH溶液反成1molH2O反应热ΔH=-52.3kJ•mol-1,造成这一结果的原因可能是用铜丝代替玻璃搅拌器 |
下列有关中和热概念、中和热测定实验(如图)的说法正确的是
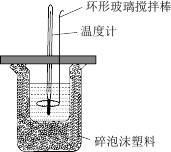

A. 已知在稀溶液中:H+(aq)+OH-(aq) =H2O(l);ΔH=-57.3kJ·mol-1,则有 已知在稀溶液中:H+(aq)+OH-(aq) =H2O(l);ΔH=-57.3kJ·mol-1,则有 |
| B.已知2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) △H=-114.6kJ·mol-1,则该反应的中和热为114.6 kJ·mol-1。 |
| C.中和热测定实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小 |
| D.酸碱混合时,量筒中的NaOH溶液应分多次倒入已装有盐酸的小烧杯中,并不断用环形玻璃搅拌棒搅拌。 |
50mL0.50mol·L-1盐酸与50mL0.55 mol·L -1INaOH 溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法正确的是
| A.在测定中和热的实验中,至少需要测定并记录的温度是3次 |
| B.大烧杯上如不盖硬纸板,测得的中和热数值会偏小 |
| C.用相同浓度和体积的氨水代替NaOH 溶液进行上述实验,测得中和热的数值会偏大 |
| D.测定中和热的实验中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热ΔH< -57.3 kJ·mol-1 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


