单选题 适中0.65 引用1 组卷172
镁-空气电池的总反应方程式为:2Mg+O2+2H2O=2Mg(OH)2,其工作原理如图所示,下列说法不正确的是
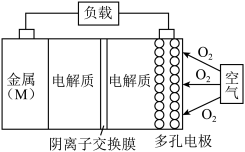

| A.该电池的正极反应方程式为O2+4e-+2H2O=4OH- |
| B.为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜 |
| C.该电池中电子从金属电极流出,流经电解质到多孔电极 |
| D.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面 |
19-20高二上·浙江绍兴·阶段练习
类题推荐
金属(M)-空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应为:4M+nO2+2nH2O=4M(OH)n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是
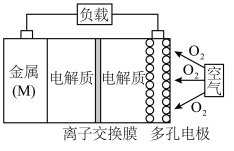

| A.比较Mg、Al、Zn三种金属-空气电池,Mg-空气电池的理论比能量最高 |
| B.为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜 |
| C.电池放电过程的正极反应式:O2+2H2O+4e-=4OH- |
| D.多孔电极可提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面 |
镁-空气电池的工作原理如图所示,电池反应方程式为:2Mg+O2+2H2O=2Mg(OH)2。下列说法错误的是
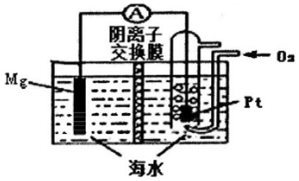

| A.通入氧气的电极为正极 |
| B.放电时,溶液中的OH-由正极移向负极 |
| C.负极的电极反应为Mg-2e-=Mg2+ |
| D.采用多孔Pt电极有利于氧气扩散,提高电极与电解质溶液的接触而积 |
金属(M)–空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH) n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是
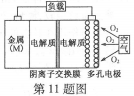

| A.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面 |
| B.比较Mg、Al、Zn三种金属–空气电池,Al–空气电池的理论比能量最高 |
| C.M–空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne–=4M(OH)n |
| D.在M–空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


