单选题 较易0.85 引用3 组卷157
将 0.1mol/LCH3COOH 溶液加水稀释或者加入少量 CH3COONa 晶体时,都会引起
| A.溶液的 pH 变大 |
| B.CH3COOH 的电离程度增大 |
| C.溶液的导电能力增强 |
| D.溶液中c(OH-)减小 |
17-18高三上·上海·期中
类题推荐
向起始pH相同的盐酸和醋酸溶液中加水稀释,pH随 (稀释后的溶液总体积为Vt,稀释前的体积V0)的变化关系如下图所示,下列说法正确的是
(稀释后的溶液总体积为Vt,稀释前的体积V0)的变化关系如下图所示,下列说法正确的是
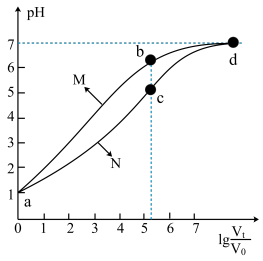

| A.曲线N表示的是盐酸加水稀释过程中,pH随 |
| B.升高温度,CH3COOH的电离平衡向电离方向移动,c点将向下移动 |
| C.当 |
| D.a→c→d过程中,CH3COOH的电离程度减小 |
人的血液中存在H2CO3~HCO3﹣这样“一对”物质,前者的电离和后者的水解两个平衡使正常人血液的pH保持在7.35~7.45之间.血液中注射碱性物质时,上述电离和水解受到的影响分别是
| A.促进、促进 | B.促进、抑制 | C.抑制、促进 | D.抑制、抑制 |
相同温度下,根据三种酸的电离常数,下列判断正确的是( )
| 酸 | HX | HY | HZ |
| 电离常数 | 9×10-7 | 9×10-6 | 10-2 |
| A.三种酸的强弱关系:HX>HY>HZ |
| B.反应HZ+Y-═HY+Z-能够发生 |
| C.酸根离子结合氢离子的能力强弱关系为:Z->Y->X- |
| D.相同温度下,1mol/LHX溶液的电离常数大于0.1mol/LHX |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


