解答题-工业流程题 适中0.65 引用7 组卷364
高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
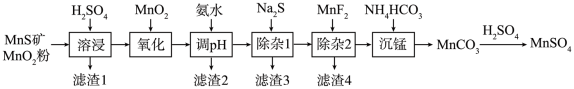
相关金属离子[c0(Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下:
(1)“滤渣1”含有S和________________ ;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式_______ 。
(2)“氧化”中添加适量的MnO2的作用是将________________________ 。
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______ ~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________ 。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是______
(6)写出“沉锰”的离子方程式_____________________________________ 。

相关金属离子[c0(Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(2)“氧化”中添加适量的MnO2的作用是将
(3)“调pH”除铁和铝,溶液的pH范围应调节为
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
(6)写出“沉锰”的离子方程式
19-20高三上·宁夏石嘴山·阶段练习
类题推荐
工业上常用天然二氧化锰粉与硫化锰矿(含Fe、Al、Mg、Ni、Si等的氧化物杂质)制备MnSO4,其工艺如图所示。回答下列问题:
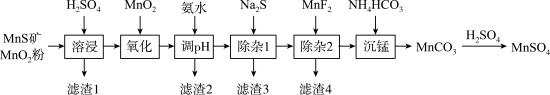
资料1:常温下,MnCO3的溶度积Ksp=2.1 10-11,当c0(Mn+)≤ 1.0
10-11,当c0(Mn+)≤ 1.0 10-5 mol·L-1时该离子已沉淀完全。
10-5 mol·L-1时该离子已沉淀完全。
资料2:相关金属离子 [c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
(1)“滤渣1”含有S和___________ ;“溶浸”中二氧化锰与硫化锰反应的化学方程式为___________ 。
(2)“氧化”中添加适量的MnO2的作用是___________ 。
(3)“调pH”只除去铁和铝,溶液的pH范围为___________ 。
(4)“除杂1”的目的是除去Ni2+,“滤渣3”的主要成分是___________ 。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+,若溶液酸度过高,Mg2+沉淀不完全。请用平衡移动原理解释其原因___________ 。
(6)MnCO3是一种重要的化工原料。常温下,向溶液中加入NH4HCO3溶液使Mn2+完全沉淀,则混合溶液中 浓度不低于
浓度不低于___________ mol·L-1。

资料1:常温下,MnCO3的溶度积Ksp=2.1
资料2:相关金属离子 [c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.9 |
(2)“氧化”中添加适量的MnO2的作用是
(3)“调pH”只除去铁和铝,溶液的pH范围为
(4)“除杂1”的目的是除去Ni2+,“滤渣3”的主要成分是
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+,若溶液酸度过高,Mg2+沉淀不完全。请用平衡移动原理解释其原因
(6)MnCO3是一种重要的化工原料。常温下,向溶液中加入NH4HCO3溶液使Mn2+完全沉淀,则混合溶液中
高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Si等元素)制备,工艺如下图所示:
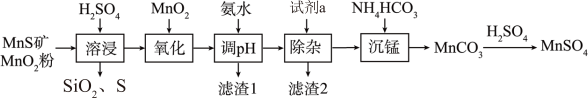
0.1mol/L金属离子形成氢氧化物沉淀的pH范围如下表:
(1)“氧化”过程中添加适量的MnO2,其作用是将溶液中的___________ 离子氧化,便于调pH除去。通过表格中数据分析,调pH过程为了除去溶液中的铁和铝而尽量不损耗锰,溶液的pH范围为___________ 。
(2)写出氢氧化锰的溶度积表达式Ksp[Mn(OH)2]=___________ ,根据表格中Mn2+开始沉淀的pH数据,求Mn2+沉淀完全的pH,x=___________ 。

0.1mol/L金属离子形成氢氧化物沉淀的pH范围如下表:
| Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀的pH | 8.0 | 6.3 | 1.5 | 3.4 | 8.9 |
| 沉淀完全的pH | x | 8.3 | 2.8 | 4.7 | 10.9 |
(1)“氧化”过程中添加适量的MnO2,其作用是将溶液中的
(2)写出氢氧化锰的溶度积表达式Ksp[Mn(OH)2]=
高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(主要成分为MnS,还含Fe、Al、Mg、Zn、Ni、Si等元素的氧化物)制备,工艺流程如图所示,回答下列问题:
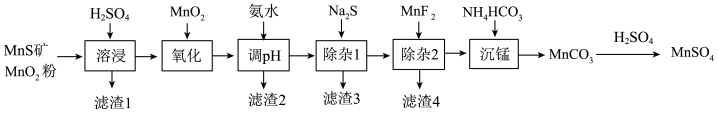
相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下表:
(1)已知“溶浸”中发生反应的化学方程式为 ,当生成0.5molMnSO4时,该反应中转移的电子数为
,当生成0.5molMnSO4时,该反应中转移的电子数为_____ ,该反应中n(还原剂):n(氧化剂)=_____ ,“滤渣1”的主要成分为_____ (化学式)。
(2)“氧化”中添加适量的MnO2的作用是将Fe2+氧化为Fe3+,酸性条件下MnO2氧化Fe2+反应的离子方程式为_____ 。
(3)“除杂1”的目的是去Zn2+和Ni2+,“除杂2”的目的是将Mg2+转化为MgF2沉淀从而除去Mg2+,试推测“调pH”是为了除_____ (填元素符号),溶液的pH范围应调节在_____ ~6(当某金属离子沉淀完全视作该金属离子已除净)。
(4)写出“沉锰”时发生反应的离子方程式_____ 。
(5)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为Li3NixCoyMnzO6,其中Ni、Co、Mn、O的化合价次为+2、+3、+4、-2,当x=y=1时,z=_____ ,试用氧化物的形式表示镍钴锰三元材料:_____ [某些含氧酸盐可以写成氧化物的形式(例如:NaAlO2以表示为NaO·Al2O3]。

相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下表:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(2)“氧化”中添加适量的MnO2的作用是将Fe2+氧化为Fe3+,酸性条件下MnO2氧化Fe2+反应的离子方程式为
(3)“除杂1”的目的是去Zn2+和Ni2+,“除杂2”的目的是将Mg2+转化为MgF2沉淀从而除去Mg2+,试推测“调pH”是为了除
(4)写出“沉锰”时发生反应的离子方程式
(5)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为Li3NixCoyMnzO6,其中Ni、Co、Mn、O的化合价次为+2、+3、+4、-2,当x=y=1时,z=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


