填空题 适中0.65 引用1 组卷81
氯化亚砜(SOCl2)在科研和工业上应用比较广泛。回答下列问题:
I.工业上利用尾气SO2与SCl2、Cl2反应合成氯化亚砜。发生如下反应:
①Cl2(g)+SO2(g) SO2Cl2(g) △H =-471.7kJ•mol-1
SO2Cl2(g) △H =-471.7kJ•mol-1
②SO2Cl2(g)+SCl2(g) 2SOCl2(g) △H=-5.6kJ•mol-1
2SOCl2(g) △H=-5.6kJ•mol-1
567K时,在10L密闭容器中,充入一定量的Cl2、SO2和SCl2,测得初始压强为P0反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与起始温度相同)如图所示,起始各组分及达平衡时SO2Cl2(g)的物质的量如表。
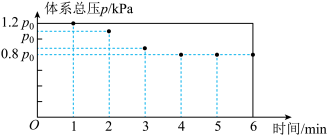
(1)图中数据显示0~l min体系压强增大的原因是____ 。
(2)反应①、②达到平衡时,SCl2的转化率为__ 。
(3)pK=-lgK,567K时,上述反应②的pK=___ (结果保留两位有效数字,已知lg2=0.30)。
(4)567K下,若压缩容器体积为5L,则平衡时c(SO2)__ (填“大于” “小于”或“等于”)上述反应平衡时的c(SO2)。
II.氯化亚砜常用于合成正丁酰氯。向连有尾气吸收装置的容器中按照物质的量1:1.5投料比加入正丁酸和氯化亚砜,反应为CH3CH2CH2COOH+SOCl2 CH3CH2CH2COCl+SO2↑+HCl↑。实验测得温度和时间对反应的影响如表:
CH3CH2CH2COCl+SO2↑+HCl↑。实验测得温度和时间对反应的影响如表:
(5)若开始在较高温度下反应,则会放出大量气体。通过分析上表数据,选择合理实验方法的序号为___ 。说明你选用实验方法的理由:____ 。
I.工业上利用尾气SO2与SCl2、Cl2反应合成氯化亚砜。发生如下反应:
①Cl2(g)+SO2(g)
②SO2Cl2(g)+SCl2(g)
567K时,在10L密闭容器中,充入一定量的Cl2、SO2和SCl2,测得初始压强为P0反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与起始温度相同)如图所示,起始各组分及达平衡时SO2Cl2(g)的物质的量如表。

| 各组分 | Cl2 | SO2(g) | SCl2(g) | SO2Cl2(g) | SOCl2(g) |
| 起始/mol | 0.5 | 0.5 | 0.5 | 0 | 0 |
| 平衡/mol | 0.2 |
(1)图中数据显示0~l min体系压强增大的原因是
(2)反应①、②达到平衡时,SCl2的转化率为
(3)pK=-lgK,567K时,上述反应②的pK=
(4)567K下,若压缩容器体积为5L,则平衡时c(SO2)
II.氯化亚砜常用于合成正丁酰氯。向连有尾气吸收装置的容器中按照物质的量1:1.5投料比加入正丁酸和氯化亚砜,反应为CH3CH2CH2COOH+SOCl2
| 序号 | 实验方法 | 收率/% |
| 1 | 25℃,反应6h | 73.60 |
| 2 | 25℃,反应8h | 74.60 |
| 3 | 75℃,反应2h | 75.00 |
| 4 | 75℃,反应3h | 76.00 |
| 5 | 先25℃,反应1h;后75℃,反应0~1h | 81.10 |
| 6 | 先25℃,反应1h;后75℃,反应0~1h | 87.10 |
(5)若开始在较高温度下反应,则会放出大量气体。通过分析上表数据,选择合理实验方法的序号为
19-20高三上·山东日照·阶段练习
类题推荐
氧化亚砜(SOCl2)在科研和工业上应用比较广泛。回答下列问题:
I.工业上利用尾气SO2与SCl2、Cl2反应合成氯化亚砜。发生如下反应:
①
②
在567K时,在10L密闭容器中,充入一定量的Cl2、SO2和SCl2,测得初始压强为P0,反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与初始温度相同)如图所示,起始各组分及达平衡时SO2Cl2(g)的物质的量如表。
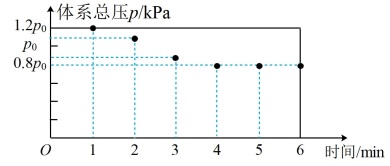
(1)图中数据显示0~1min体系压强增大的原因是_______ 。
(2)反应①、②达到平衡时,SCl2的转化率为_______ 。
(3) ,567K时,上述反应②的
,567K时,上述反应②的
_____ (结果保留两位有效数字,已知 )。
)。
(4)567K下,若压缩容器体积为5L,则平衡时c(SO2)_____ (填“大于”“小于”或“等于”)上述反应平衡时的c(SO2)。
II.Li/SOCl2电池是一种高比能量电池,电解液为非水的LiAlCl4的SOCl2溶液。正极为金属酞菁配合物(M-Pe,电池正极催化剂)附着的碳棒。正极催化过程为:SOCl2先与酞菁形成加合物,接着发生加合物的两步快速的电子转移,过程如图所示。
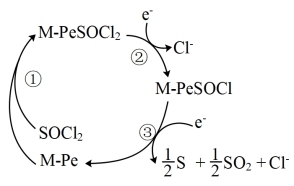
(5)上述正极催化过程M-PeSOCl2为_______ (填“催化剂”或“中间产物”),电池总反应的化学方程式为_______ 。放电时,电解质中锂离子移向_______ 极。
I.工业上利用尾气SO2与SCl2、Cl2反应合成氯化亚砜。发生如下反应:
①
②
在567K时,在10L密闭容器中,充入一定量的Cl2、SO2和SCl2,测得初始压强为P0,反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与初始温度相同)如图所示,起始各组分及达平衡时SO2Cl2(g)的物质的量如表。

| 各组分 | Cl2 | SO2(g) | SCl2(g) | SO2Cl2(g) | SOCl2(g) |
| 起始/mol | 0.5 | 0.5 | 0.5 | 0 | 0 |
| 平衡/mol | 0.2 |
(1)图中数据显示0~1min体系压强增大的原因是
(2)反应①、②达到平衡时,SCl2的转化率为
(3)
(4)567K下,若压缩容器体积为5L,则平衡时c(SO2)
II.Li/SOCl2电池是一种高比能量电池,电解液为非水的LiAlCl4的SOCl2溶液。正极为金属酞菁配合物(M-Pe,电池正极催化剂)附着的碳棒。正极催化过程为:SOCl2先与酞菁形成加合物,接着发生加合物的两步快速的电子转移,过程如图所示。

(5)上述正极催化过程M-PeSOCl2为
氯化亚砜(SOCl2)在科研和工业上应用比较广泛。回答下列问题:
I.工业上利用尾气SO2与SCl2、C12反应合成氯化亚砜。发生如下反应:
①C12(g)+SO2(g) SO2C12(g) △H=-471.7kJ·mol-1
SO2C12(g) △H=-471.7kJ·mol-1
②SO2C12(g)+SCl2(g) 2SOC12(g)△H=-5.6kJ·mol-1
2SOC12(g)△H=-5.6kJ·mol-1
567K时,在10L密闭容器中,充入一定量的C12、SO2和SCl2,测得初始压强为p0,反应过程中容器内总压强(p)随时间(t)变化(反应达到平衡时的温度与初始温度相同)如下图所示,起始各组分及达平衡时SO2C12(g)的物质的量如下表。
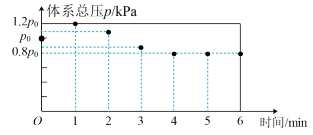
(1)0~1min,图中数据显示体系压强增大的原因是________________ 。
(2)0~4min内,v(C12)=_____ mol·L-1·min-1,5min时SCl2的转化率为________ 。
(3)567K时,上述反应②的KP______ 。
(4)567K下,若扩大容器体积为20L,则平衡时c(SO2)_____ (填“大于”“小于”或“等于”)上述反应平衡时的c(SO2)。
II.Li/SOCl2电池是一种高比能量电池,电解液为非水的LiAlC14的SOCl2溶液。正极为金属酞菁配合物(M-Pe,电池正极催化剂)附着的碳棒。正极催化过程为:SOCl2先与酞菁形成加合物,接着发生加合物的两步快速的电子转移,过程如图所示。
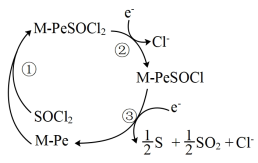
(5)上述正极催化过程M-PeSOCl2为_______ (填“催化剂”或“中间产物”),放电过程中每转移1mol电子生成_____ g硫单质。电池总反应的化学方程式为_______________________________________ 。
I.工业上利用尾气SO2与SCl2、C12反应合成氯化亚砜。发生如下反应:
①C12(g)+SO2(g)
②SO2C12(g)+SCl2(g)
567K时,在10L密闭容器中,充入一定量的C12、SO2和SCl2,测得初始压强为p0,反应过程中容器内总压强(p)随时间(t)变化(反应达到平衡时的温度与初始温度相同)如下图所示,起始各组分及达平衡时SO2C12(g)的物质的量如下表。

| 各分组 | Cl2 | SO2 | SCl2(g) | SO2Cl2(g) | SOCl2(g) |
| 起始/mol | 0.5 | 0.5 | 0.5 | 0 | 0 |
| 平衡/mol | 0.2 |
(2)0~4min内,v(C12)=
(3)567K时,上述反应②的KP
(4)567K下,若扩大容器体积为20L,则平衡时c(SO2)
II.Li/SOCl2电池是一种高比能量电池,电解液为非水的LiAlC14的SOCl2溶液。正极为金属酞菁配合物(M-Pe,电池正极催化剂)附着的碳棒。正极催化过程为:SOCl2先与酞菁形成加合物,接着发生加合物的两步快速的电子转移,过程如图所示。

(5)上述正极催化过程M-PeSOCl2为
氯化亚砜(SOCl2)具有很强的氯化能力和脱水能力,在有机合成中具有重要的应用。工业上用硫酸厂尾气中的SO2与SCl2、Cl2为原料合成SOCl2,反应如下:
Ⅰ. SO2(g)+Cl2(g) SO2Cl2(g) ΔH = −471.7 kJ·mol−1
SO2Cl2(g) ΔH = −471.7 kJ·mol−1
Ⅱ. SCl2(g)+SO2Cl2(g) 2SOCl2(g) ΔH = −5.6 kJ·mol−1
2SOCl2(g) ΔH = −5.6 kJ·mol−1
回答下列问题:
(1)该条件下,由SO2(g)、Cl2(g)和SCl2(g),制备1 mol SOCl2(g)放出的热量为______ kJ。
(2)一定条件下,在5 L的恒容密闭容器中通入一定量的SO2、SCl2与Cl2,反应4 min后达到平衡。若初始压强为p0,反应过程中容器内总压强(p)随时间(t)变化如下图所示(平衡时温度与初始温度相同)。

容器内各组分物质的量如下表。
①0~1 min容器内压强增大的原因为___________ 。
②反应Ⅰ、Ⅱ达平衡时,SCl2的平衡转化率为________ 。
③K为平衡常数,pK=−lg K,该温度下,反应Ⅱ的pK =______ (保留两位有效数字,lg2 = 0.30)。
(3)常温下,将SO2通入到NaOH溶液中,充分反应后得到a mol·L−1的NaHSO3溶液,该溶液的pH=5,则溶液中c( )
)_____ c(H2SO3)(填“>”“=”或“<”), 的电离常数约为
的电离常数约为_________ (用含a的式子表示)。
Ⅰ. SO2(g)+Cl2(g)
Ⅱ. SCl2(g)+SO2Cl2(g)
回答下列问题:
(1)该条件下,由SO2(g)、Cl2(g)和SCl2(g),制备1 mol SOCl2(g)放出的热量为
(2)一定条件下,在5 L的恒容密闭容器中通入一定量的SO2、SCl2与Cl2,反应4 min后达到平衡。若初始压强为p0,反应过程中容器内总压强(p)随时间(t)变化如下图所示(平衡时温度与初始温度相同)。

容器内各组分物质的量如下表。
| 组分 | SO2 | Cl2 | SCl2 | SO2Cl2 | SOCl2 |
| 起始/mol | 0.25 | 0.25 | 0.25 | 0 | 0 |
| 平衡/mol | 0.1 |
②反应Ⅰ、Ⅱ达平衡时,SCl2的平衡转化率为
③K为平衡常数,pK=−lg K,该温度下,反应Ⅱ的pK =
(3)常温下,将SO2通入到NaOH溶液中,充分反应后得到a mol·L−1的NaHSO3溶液,该溶液的pH=5,则溶液中c(
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


