解答题-实验探究题 适中0.65 引用4 组卷580
叠氮化钾( )能促使作物或难于萌发的种子发育。设计如下实验制备叠氮化钾并测定其纯度:
)能促使作物或难于萌发的种子发育。设计如下实验制备叠氮化钾并测定其纯度:
I.制备
步骤1:制备亚硝酸丁酯( )
)

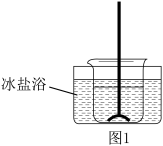
反应装置如图1(夹持装置略去),向烧杯中依次加入稀硫酸、丁醇、亚硝酸钠溶液,待反应完全后,分离出上层油状物,用 和
和 的混合溶液洗涤三次,经干燥后备用。
的混合溶液洗涤三次,经干燥后备用。
步骤2:制备叠氮化钾

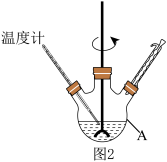
反应装置如图2(夹持及加热装置路去),向仪器A中加入 乙醇溶液、
乙醇溶液、 的联氨(
的联氨( )、亚硝酸丁酯,蒸汽浴加热,反应完全后,叠氮化钾即沉淀出来,冰浴冷却,过滤,先用无水乙醇洗涤,再用无水乙醚洗涤,在空气中于
)、亚硝酸丁酯,蒸汽浴加热,反应完全后,叠氮化钾即沉淀出来,冰浴冷却,过滤,先用无水乙醇洗涤,再用无水乙醚洗涤,在空气中于 干燥。
干燥。
相关物质性质如下:
请回答:
(1)仪器A的名称为_____________ .
(2)步骤1中分离出亚硝酸丁酯的操作名称为_____________ ;步骤1中用NaCl和NaHCO3的混合溶液洗涤的目的是__________________________ .
(3)步骤2中冰浴冷却的目的是__________________________ ;步骤2中干燥产品的温度控制在55~60℃,原因是__________________________
(4)如需提高产品的纯度,可在_____________ (填编号)中进行重结晶。
A.无水乙醇 B.无水乙醚 C.水 D.乙醇的水溶液
Ⅱ.分光光度法测定产品的纯度
原理: 与
与 反应非常灵敏,生成红色络合物,在一定波长下测量红色溶液的吸光度,利用“
反应非常灵敏,生成红色络合物,在一定波长下测量红色溶液的吸光度,利用“ 吸光度”曲线确定样品溶液中的
吸光度”曲线确定样品溶液中的 。测定步骤如下:
。测定步骤如下:
①用 晶体配制
晶体配制 标准溶液;
标准溶液;
②配制一组相同体积( )不同浓度的
)不同浓度的 标准溶液,分别加入
标准溶液,分别加入 (足量)
(足量) 标准溶液,摇匀,测量吸光度,绘制标准溶液的
标准溶液,摇匀,测量吸光度,绘制标准溶液的 与吸光度的关系曲线,如图;
与吸光度的关系曲线,如图;
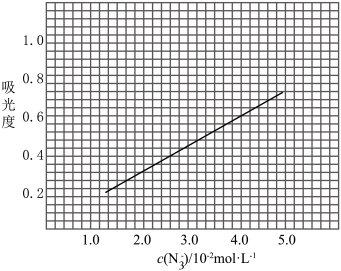
③产品测定:称取0.360g产品,配成 溶液,取出
溶液,取出 于标准管中,加入
于标准管中,加入 (足量)
(足量) 标准溶液,摇匀,测得吸光度为0.6。
标准溶液,摇匀,测得吸光度为0.6。
(5)实验室用 晶体配制
晶体配制 标准溶液的方法为
标准溶液的方法为_________________ .
(6)产品的纯度为_________________ ;若③中加入的 标准溶液不足以将产品完全反应,则测得的产品纯度
标准溶液不足以将产品完全反应,则测得的产品纯度________________ (填“偏高”“偏低”或“无影响”)。
I.制备
步骤1:制备亚硝酸丁酯(
反应装置如图1(夹持装置略去),向烧杯中依次加入稀硫酸、丁醇、亚硝酸钠溶液,待反应完全后,分离出上层油状物,用
步骤2:制备叠氮化钾
反应装置如图2(夹持及加热装置路去),向仪器A中加入


相关物质性质如下:
| 物质 | 颜色、状态 | 沸点(℃) | 溶解性 |
| 无色晶体 | 受热易分解 | 易溶于水,微溶于乙醇,不溶于乙醚 | |
| 无色液体 | 118 | 微溶于水,与乙醇、乙醚混溶 | |
| 无色或淡黄色油状液体 | 78 | 不溶于水,与乙醇、乙醚混溶 | |
| 无色油状液体 | 118 | 与水、乙醇混溶,不溶于乙醚 |
请回答:
(1)仪器A的名称为
(2)步骤1中分离出亚硝酸丁酯的操作名称为
(3)步骤2中冰浴冷却的目的是
(4)如需提高产品的纯度,可在
A.无水乙醇 B.无水乙醚 C.水 D.乙醇的水溶液
Ⅱ.分光光度法测定产品的纯度
原理:
①用
②配制一组相同体积(

③产品测定:称取0.360g产品,配成
(5)实验室用
(6)产品的纯度为
19-20高三上·浙江·开学考试
类题推荐
叠氮化钾能促进难以萌发的种子发育,在新作物育种中应用广泛,实验室制备 流程如下。回答下列问题:
流程如下。回答下列问题: 。已知:
。已知:
①制备亚硝酸异丙酯 在烧杯中进行
在烧杯中进行
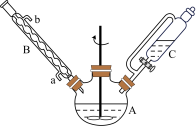
②制备 的D、E和F阶段均在如图装置中完成。
的D、E和F阶段均在如图装置中完成。
(1)仪器B的作用是_______ 。
(2)仪器A中发生反应时, 与水合肼
与水合肼 在碱性条件下,重新生成
在碱性条件下,重新生成 (异丙醇),该反应的化学方程式为
(异丙醇),该反应的化学方程式为_______ 。
(3)在制备亚硝酸异丙酯 中,洗涤亚硝酸异丙酯使用
中,洗涤亚硝酸异丙酯使用 溶液,目的:
溶液,目的:_______ 。
(4)关于上述流程中各步骤的说法,正确的是_______ (填标号)。
A.步骤D还需要的仪器是容量瓶和胶头滴管
B.制备亚硝酸异丙酯时用冰盐浴的目的是防止反应过于剧烈
C.步骤F加入无水乙醇的目的是促进 的析出
的析出
(5)在F阶段,向反应后混合物中“加入无水乙醇”并“冰盐浴冷却”的目的_______ 。
II.纯度检测——“分光光度法”: 与
与 反应灵敏,生成红色配合物,在一定波长下测量红色溶液的吸光度,利用“
反应灵敏,生成红色配合物,在一定波长下测量红色溶液的吸光度,利用“ ——吸光度”曲线确定样品溶液中的
——吸光度”曲线确定样品溶液中的 。
。
查阅文献可知:不同浓度的5.0mL标准溶液,分别加入5.0mL(足量) 溶液,摇匀后测量吸光度,可绘制标准溶液的
溶液,摇匀后测量吸光度,可绘制标准溶液的 与吸光度的关系曲线如图所示。
与吸光度的关系曲线如图所示。
①准确称 晶体,配制
晶体,配制 标准液(与文献浓度一致)。
标准液(与文献浓度一致)。
②准确称取0.72g样品,配制成100mL溶液,取5.0mL待测溶液,向其中加入 (足量)标准液,摇匀后测得吸光度为0.6。
(足量)标准液,摇匀后测得吸光度为0.6。
(6)简述配制 标准液时,溶解
标准液时,溶解 晶体的方法
晶体的方法_______ 。
(7)步骤②中取用 标准液
标准液
_______ mL,样品的质量分数为_______ 。

①制备亚硝酸异丙酯
②制备
| 物质 | 颜色、状态 | 沸点(℃) | 溶解性 |
| 无色晶体 | 受热易分解 | 易溶于水,微溶于乙醇,不溶于乙醚 | |
| 无色液体 | 118 | 微溶于水,与乙醇、乙醚混溶 | |
| 无色或淡黄色油状液体 | 78 | 不溶于水,与乙醇、乙醚混溶 | |
| 无色油状液体 | 118 | 与水、乙醇混溶,不溶于乙醚 |
(1)仪器B的作用是
(2)仪器A中发生反应时,
(3)在制备亚硝酸异丙酯
(4)关于上述流程中各步骤的说法,正确的是
A.步骤D还需要的仪器是容量瓶和胶头滴管
B.制备亚硝酸异丙酯时用冰盐浴的目的是防止反应过于剧烈
C.步骤F加入无水乙醇的目的是促进
(5)在F阶段,向反应后混合物中“加入无水乙醇”并“冰盐浴冷却”的目的
II.纯度检测——“分光光度法”:
查阅文献可知:不同浓度的5.0mL标准溶液,分别加入5.0mL(足量)

①准确称
②准确称取0.72g样品,配制成100mL溶液,取5.0mL待测溶液,向其中加入
(6)简述配制
(7)步骤②中取用
叠氮化合物是重要的有机合成试剂,实验室可用肼与亚硝酸异丙酯反应制备KN3。回答下列问题:
Ⅰ.制备KN3的流程如图甲。

甲
已知:①制备亚硝酸异丙酯在烧杯中进行
②制备KN3的D、E和F阶段均在图乙所示仪器中完成
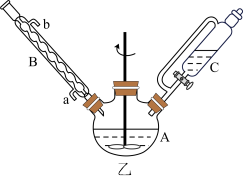
③下表为文献资料
(1)图中仪器B的作用是_______ ,仪器C的名称为_______ 。
(2)制备亚硝酸异丙酯的化学方程式为_______ 。
(3)洗涤亚硝酸异丙酯使用NaHCO3溶液的主要目的是_______ ,写出E阶段发生反应的化学方程式_______ 。
(4)在F阶段中,向反应后混合物中“加入无水乙醇”并“冰盐浴冷却”的目的是_______ 。
Ⅱ.纯度检测—“分光光度法”,其原理:Fe3+与N 反应灵敏,生成红色配合物,在一定波长下测量红色溶液的吸光度,利用“c(N
反应灵敏,生成红色配合物,在一定波长下测量红色溶液的吸光度,利用“c(N )—吸光度”曲线确定样品溶液中的c(N
)—吸光度”曲线确定样品溶液中的c(N )。
)。
查阅文献可知:不同浓度的5.0mLNaN3标准溶液,分别加入5.0mL(足量)FeCl3标准溶液,摇匀后测量吸光度,可绘制标准溶液的c(N )与吸光度的关系曲线图如图丙所示。
)与吸光度的关系曲线图如图丙所示。

纯度检测步骤如下:
①准确称量m gFeCl3·6H2O晶体,配制100mLFeCl3标准液(与文献浓度一致)。
②准确称量0.360gKN3样品,配制成100mL溶液,取5.0mL待测溶液加入V mL(足量)FeCl3标准液,摇匀后测得吸光度为0.6。
(5)步骤②中取用FeCl3标准液V =_______ mL,样品的质量分数为_______ 。
Ⅰ.制备KN3的流程如图甲。

甲
已知:①制备亚硝酸异丙酯在烧杯中进行
②制备KN3的D、E和F阶段均在图乙所示仪器中完成

③下表为文献资料
| 物质 | 颜色、状态 | 沸点 | 溶解性 |
| KN3 | 无色晶体 | 300℃,受热易分解 | 易溶于水,微溶于乙醇,不溶于乙醚 |
| (CH3)2CHOH | 无色液体 | 82.45℃ | 微溶于水,与乙醇、乙醚混溶 |
| (CH3)2CHONO | 无色油状液体 | 39℃ | 不溶于水,与乙醇、乙醚混溶 |
| N2H4·H2O | 无色油状液体 | 118℃ | 与水、乙醇混溶,不溶于乙醚 |
(2)制备亚硝酸异丙酯的化学方程式为
(3)洗涤亚硝酸异丙酯使用NaHCO3溶液的主要目的是
(4)在F阶段中,向反应后混合物中“加入无水乙醇”并“冰盐浴冷却”的目的是
Ⅱ.纯度检测—“分光光度法”,其原理:Fe3+与N
查阅文献可知:不同浓度的5.0mLNaN3标准溶液,分别加入5.0mL(足量)FeCl3标准溶液,摇匀后测量吸光度,可绘制标准溶液的c(N

纯度检测步骤如下:
①准确称量m gFeCl3·6H2O晶体,配制100mLFeCl3标准液(与文献浓度一致)。
②准确称量0.360gKN3样品,配制成100mL溶液,取5.0mL待测溶液加入V mL(足量)FeCl3标准液,摇匀后测得吸光度为0.6。
(5)步骤②中取用FeCl3标准液V =
叠氮化合物是重要的有机合成剂,实验室可用肼与亚硝酸异丙酯反应制备KN3。回答下列问题:
I.制备KN3的流程如图:
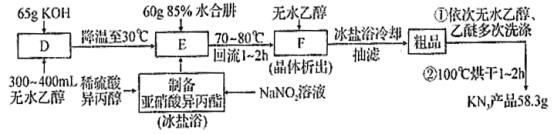
已知:①制备亚硝酸异丙酯在烧杯中进行;②制备KN3的D、E和F阶段均在如图所示仪器中完成;③下表为文献资料。
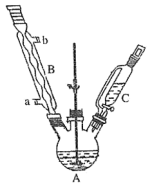
(1)图中仪器B的作用是__ 。
(2)制备亚硝酸异丙酯的化学方程式为__ 。
(3)在“制备亚硝酸异丙酯”中,分离亚硝酸异丙酯的主要玻璃仪器__ ,洗涤亚硝酸异丙酯使用NaHCO3溶液的主要原因是__ 。
(4)在F阶段中,向反应后混合物中“加入无水乙醇"并“冰盐浴冷却”的目的是__ ;烘干前,用抽滤方法并用乙醇和乙醚洗涤的主要目的是__ 。
II.纯度检测——“分光光度法”,其原理:Fe3+与N3-反应灵敏,生成红色络合物,在一定.波长下测量红色溶液的吸光度,利用“c(N )一吸光度”曲线确定样品溶液中的c(N
)一吸光度”曲线确定样品溶液中的c(N )。查阅文献可知:
)。查阅文献可知:
不同浓度的5.0mLNaN3标准溶液,分别加入5.0mL(足量)FeCl3标准溶液,摇匀后测量吸光度,绘制标准溶液的c(N )与吸光度的关系曲线图:
)与吸光度的关系曲线图:
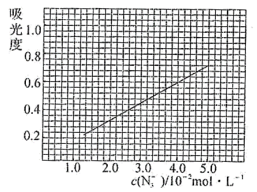
步骤如下:
①准确称量mgFeCl3•6H2O晶体,配制100mLFeCl3标准液(与文献浓度一致)。
②准确称量0.360gKN3样品,配制成100mL溶液,取5.0mL待测溶液加入VmL(足量)FeCl3标准液,摇匀后测得吸光度为0.6。
(5)简述配制FeCl3标准液时,溶解FeCl3•6H2O晶体的方法:___ 。
(6)步骤②中取用FeCl3标准液V=__ ;样品的质量分数为__ 。
I.制备KN3的流程如图:

已知:①制备亚硝酸异丙酯在烧杯中进行;②制备KN3的D、E和F阶段均在如图所示仪器中完成;③下表为文献资料。
物质 | 颜色、状态 | 沸点 | 溶解性 |
KN3 | 无色晶体 | 300℃受热易分解 | 易溶于水,微溶于乙醇,不溶于乙醚 |
(CH3)2CHOH | 无色液体 | 82.45℃ | 微溶于水,与乙醇、乙醚混溶 |
(CH3)2CHONO亚硝酸异丙酯 | 无色油状液体 | 39℃ | 不溶于水,与乙醇、乙醚混溶 |
N2H4•H2O水合肼 | 无色油状液体 | 118℃ | 与水、乙醇混溶,不溶于乙醚 |

(1)图中仪器B的作用是
(2)制备亚硝酸异丙酯的化学方程式为
(3)在“制备亚硝酸异丙酯”中,分离亚硝酸异丙酯的主要玻璃仪器
(4)在F阶段中,向反应后混合物中“加入无水乙醇"并“冰盐浴冷却”的目的是
II.纯度检测——“分光光度法”,其原理:Fe3+与N3-反应灵敏,生成红色络合物,在一定.波长下测量红色溶液的吸光度,利用“c(N
不同浓度的5.0mLNaN3标准溶液,分别加入5.0mL(足量)FeCl3标准溶液,摇匀后测量吸光度,绘制标准溶液的c(N

步骤如下:
①准确称量mgFeCl3•6H2O晶体,配制100mLFeCl3标准液(与文献浓度一致)。
②准确称量0.360gKN3样品,配制成100mL溶液,取5.0mL待测溶液加入VmL(足量)FeCl3标准液,摇匀后测得吸光度为0.6。
(5)简述配制FeCl3标准液时,溶解FeCl3•6H2O晶体的方法:
(6)步骤②中取用FeCl3标准液V=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


