解答题-实验探究题 适中0.65 引用1 组卷894
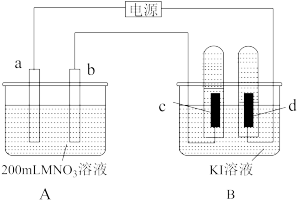
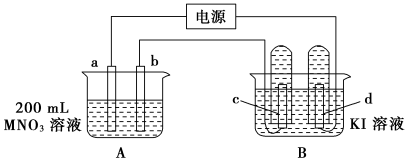
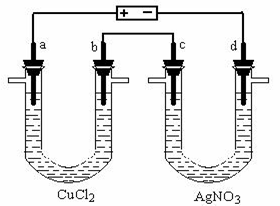
如下图所示装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。
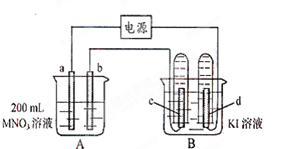
试回答:
(1)a为____ 极,c极的电极反应式为:_____________________________ 。
(2)电解开始时,在B烧杯的中央滴几滴淀粉溶液,你能观察到的现是____________ 。电解进行一段时间后,罩在c极上的试管中也收集到了气体,此时c极上的电极反应式为:______________ 。
(3)当d电极上收集到44.8 ml气体(标准状况)时停止电解,a极上放出了____ mol气体,若b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为_______________ ;若要使A池中溶液恢复原浓度,应加_____________ 。
(4)电解停止后加蒸馏水使A烧杯中的溶液体积仍为200 ml,取这种溶液加入到25.0 ml 0.100 mol·L-1的HCl溶液中,当加入31.25 ml 溶液时刚好沉淀完全。由此可知电解前A烧杯中MNO3溶液的物质的量浓度为_______________ mol·L-1。

试回答:
(1)a为
(2)电解开始时,在B烧杯的中央滴几滴淀粉溶液,你能观察到的现是
(3)当d电极上收集到44.8 ml气体(标准状况)时停止电解,a极上放出了
(4)电解停止后加蒸馏水使A烧杯中的溶液体积仍为200 ml,取这种溶液加入到25.0 ml 0.100 mol·L-1的HCl溶液中,当加入31.25 ml 溶液时刚好沉淀完全。由此可知电解前A烧杯中MNO3溶液的物质的量浓度为
11-12高二上·黑龙江大庆·阶段练习