解答题-实验探究题 较难0.4 引用1 组卷198
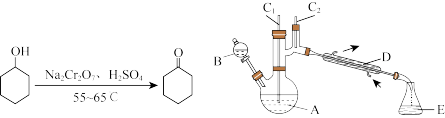
实验室可利用环己醇的氧化反应制备环己酮,反应原理和实验装置(部分夹持装置略)如下:
有关物质的物理性质见下表。
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中,在55~60℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的名称为____________________________ 。
(2)酸性Na2Cr2O7溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应增多。
①滴加酸性Na2Cr2O7溶液的操作为_______________ ;
②蒸馏不能分离环己酮和水的原因是______________ 。
(3)环己酮的提纯需要经过以下一系列的操作:
a.往液体中加入NaCl固体至饱和,静置,分液;
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层;
c.加入无水MgSO4固体,除去有机物中少量的水;
d.过滤;
e.蒸馏、除去乙醚后,收集151~156℃馏分。
①B中水层用乙醚萃取的目的是_________ ;
②上述操作a、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有__ ,操作a中,加入NaCl固体的作用是____ 。
③恢复至室温时,分离得到纯产品体积为6mL,则环已酮的产率为_____ 。(计算结果精确到0.1%)
有关物质的物理性质见下表。
| 物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
| 环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
| 水 | 100.0 | 1.0 |
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中,在55~60℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的名称为
(2)酸性Na2Cr2O7溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应增多。
①滴加酸性Na2Cr2O7溶液的操作为
②蒸馏不能分离环己酮和水的原因是
(3)环己酮的提纯需要经过以下一系列的操作:
a.往液体中加入NaCl固体至饱和,静置,分液;
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层;
c.加入无水MgSO4固体,除去有机物中少量的水;
d.过滤;
e.蒸馏、除去乙醚后,收集151~156℃馏分。
①B中水层用乙醚萃取的目的是
②上述操作a、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有
③恢复至室温时,分离得到纯产品体积为6mL,则环已酮的产率为
18-19高二下·贵州安顺·期末
类题推荐
环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮:
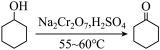
环己醇、环己酮和水的部分物理性质见下表:
★括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
(1)酸性Na2Cr2O7溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应增多。实验中将酸性Na2Cr2O7溶液加到盛有环己醇的烧杯中,在55~60℃进行反应。
反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮和水的混合物。
①酸性Na2Cr2O7溶液的加料方式为_______________ 。
②蒸馏不能分离环己酮和水的原因是_______________ 。
(2)环己酮的提纯需要经过以下一系列的操作:
a. 蒸馏,收集151~156℃的馏分; b. 过滤;
c. 在收集到的馏分中加NaCl 固体至饱和,静置,分液;
d. 加入无水MgSO4固体,除去有机物中的少量水。
①上述操作的正确顺序是________ (填字母)。
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需__________ 。
③在上述操作c中,加入NaCl 固体的作用是____________ 。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有___ 种不同化学环境的氢原子。
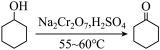
环己醇、环己酮和水的部分物理性质见下表:
| 物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)★ | 0.9624 | 能溶于水 |
| 环己酮 | 155.6(95)★ | 0.9478 | 微溶于水 |
| 水 | 100.0 | 0.9982 |
★括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
(1)酸性Na2Cr2O7溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应增多。实验中将酸性Na2Cr2O7溶液加到盛有环己醇的烧杯中,在55~60℃进行反应。
反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮和水的混合物。
①酸性Na2Cr2O7溶液的加料方式为
②蒸馏不能分离环己酮和水的原因是
(2)环己酮的提纯需要经过以下一系列的操作:
a. 蒸馏,收集151~156℃的馏分; b. 过滤;
c. 在收集到的馏分中加NaCl 固体至饱和,静置,分液;
d. 加入无水MgSO4固体,除去有机物中的少量水。
①上述操作的正确顺序是
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需
③在上述操作c中,加入NaCl 固体的作用是
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有
实验室可用环己醇制备环己酮,反应原理和实验装置(部分夹持装置略)如图:
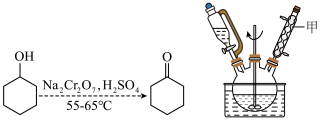
已知:环己醇、环己酮的部分物理性质如表(括号中的沸点数据表示该有机物与水形成的具有固定组成的恒沸混合物的沸点)。
I.制备:实验中通过恒压滴液漏斗将酸性Na2Cr2O7溶液加到盛有8.4mL(0.08mol环己醇的三颈烧瓶中,保持反应温度在55-65℃之间继续搅拌20min后,加入1.0g草酸,反应液变为墨绿色。
(1)仪器甲的名称是______ 。
(2)酸性Na2Cr2O7溶液氧化环己醇反应放热,则滴加酸性Na2Cr2O7溶液的方式为______ 。
(3)为控制反应体系温度在55-65℃范围内,可采取的加热方式是______ 。
(4)上述步骤中,加入草酸的目的是______ 。
Ⅱ.分离提纯:环己酮的提纯需要经过以下操作:

a.向反应后的混合液中加入NaCl固体至饱和,静置,分液;
b.水层用乙醚(乙醚沸点34.6℃)萃取,萃取液并入有机层;
c.有机层中加入无水MgSO4固体,除去少量的水,过滤;
d.将滤液在50-55℃蒸馏除去乙醚:
e.再用如图所示装置蒸馏,收集151-156℃馏分。
(5)①操作b中水层用乙醚萃取的目的是______ 。
②如果不经操作c,直接蒸馏不能分离环己酮和水的原因是______ 。
③操作e中蒸馏收集环己酮产品时,不用水冷凝,而用空气冷凝管的原因是______ 。
(6)最终得到纯产品4.9mL,则环已酮的产率为______ (计算结果精确到0.1%)。

已知:环己醇、环己酮的部分物理性质如表(括号中的沸点数据表示该有机物与水形成的具有固定组成的恒沸混合物的沸点)。
| 物质 | 沸点/℃ | 密度/g•cm-3•20℃ | 溶解性 | 相对分子质量 |
| 环己醇 | 161.1(97.8) | 0.96 | 能溶于水和醚 | 100 |
| 环己酮 | 155.6(95.0) | 0.95 | 微溶于水,能溶于醚 | 98 |
(1)仪器甲的名称是
(2)酸性Na2Cr2O7溶液氧化环己醇反应放热,则滴加酸性Na2Cr2O7溶液的方式为
(3)为控制反应体系温度在55-65℃范围内,可采取的加热方式是
(4)上述步骤中,加入草酸的目的是
Ⅱ.分离提纯:环己酮的提纯需要经过以下操作:

a.向反应后的混合液中加入NaCl固体至饱和,静置,分液;
b.水层用乙醚(乙醚沸点34.6℃)萃取,萃取液并入有机层;
c.有机层中加入无水MgSO4固体,除去少量的水,过滤;
d.将滤液在50-55℃蒸馏除去乙醚:
e.再用如图所示装置蒸馏,收集151-156℃馏分。
(5)①操作b中水层用乙醚萃取的目的是
②如果不经操作c,直接蒸馏不能分离环己酮和水的原因是
③操作e中蒸馏收集环己酮产品时,不用水冷凝,而用空气冷凝管的原因是
(6)最终得到纯产品4.9mL,则环已酮的产率为
环己酮是重要化工原料,是制造尼龙的主要中间体,也是重要的工业溶剂,实验室利用如下反应原理和实验装置制备环己酮(夹持、加热装置略,C1、C2处有仪器未画出):

环己醇、环己酮和饱和食盐水的部分物理性质见表(括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点)
实验步骤:
I.实验中通过装置B将酸性Na2Cr2O7溶液分批滴加到盛有30mL环己醇的A中,加入第一批Na2Cr2O7溶液后,待反应物的橙红色消失后再加入第二批……依次进行下去,直至反应结束,控制反应在55~65℃进行。反应结束后,向反应液中加入适量的草酸。
II.反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
III.进一步分离提纯得到精环已酮18.0g。
(1)实验装置图中C1处应放置的仪器名称为___________ 。
(2)用蒸馏不能分离环己酮和水的原因是___________ 。
(3)实验过程中Na2Cr2O7溶液分批加入的原因是___________ 。
(4)步骤I加入适量草酸为了将剩余的Na2Cr2O7完全反应,草酸与Na2Cr2O7的物质的量之比为________ 时反应恰好进行完全。
(5)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏,收集151-156℃馏分,得到精品
b.过滤
c.在收集到的粗品中加NaCl固体至饱和,静置,分液
d.加入无水MgSO4固体,除去有机物中少量水。
上述操作的正确顺序是_______ 序号)。上述操作c中,加入NaCl固体的作用是_________ 。
(6)计算环己酮的产率_________ 。(保留整数)

环己醇、环己酮和饱和食盐水的部分物理性质见表(括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点)
| 物质 | 密度/(g/cm3) | 沸点/℃ | 部分性质 |
| 环己醇 | 0.90 | 161.1(97.8) | 能溶于水,具有还原性,易被氧化 |
| 环己酮 | 0.88 | 155.6(95) | 微溶于水,遇氧化剂易发生开环反应 |
| 饱和食盐水 | 1.33 | 108.0 |
I.实验中通过装置B将酸性Na2Cr2O7溶液分批滴加到盛有30mL环己醇的A中,加入第一批Na2Cr2O7溶液后,待反应物的橙红色消失后再加入第二批……依次进行下去,直至反应结束,控制反应在55~65℃进行。反应结束后,向反应液中加入适量的草酸。
II.反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
III.进一步分离提纯得到精环已酮18.0g。
(1)实验装置图中C1处应放置的仪器名称为
(2)用蒸馏不能分离环己酮和水的原因是
(3)实验过程中Na2Cr2O7溶液分批加入的原因是
(4)步骤I加入适量草酸为了将剩余的Na2Cr2O7完全反应,草酸与Na2Cr2O7的物质的量之比为
(5)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏,收集151-156℃馏分,得到精品
b.过滤
c.在收集到的粗品中加NaCl固体至饱和,静置,分液
d.加入无水MgSO4固体,除去有机物中少量水。
上述操作的正确顺序是
(6)计算环己酮的产率
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


