填空题 适中0.65 引用1 组卷145
高铁酸钾(K2FeO4)是一种可溶于水,具有极强氧化性的高效多功能水处理剂,也可作高容量电池材料。回答下列问题:
(1)高铁酸钾中铁元素的化合价为___________ 。
(2)工业上通常先用干法制备高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,析出高铁酸钾。干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2==2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中还原剂为_______________ 。低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾,其原因是_________________ 。
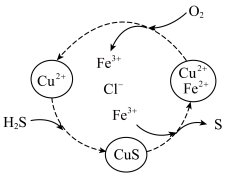
(3)常温下,高铁酸钾能氧化浓盐酸生成氯气,该反应离子方程式为___ 。
(4)比亚迪双模电动汽车使用高铁电池供电,其电池反应为3Zn+2K2FeO4+8H2O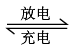 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为_______________________________________ ,正极附近溶液的pH变__________ (填“大”或“小”)。
(5)工业上可用K2FeO4溶液氧化废水中的还原性污染物M,为研究反应效果,设计如下所示的对比实验探究温度、浓度、pH对降解速率和反应效果的影响,实验测得M的浓度与时间关系如图所示。
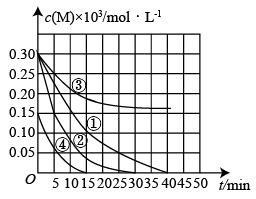
实验①中前25 min内M的反应速率为_____________________ ;其他条件相同时,实验①、②说明温度越高,M的反应速率越_________ (填“大”或“小”);其他条件相同时,实验①、③说明pH越大,M的反应速率越_________ (填“大”或“小”)。
(1)高铁酸钾中铁元素的化合价为
(2)工业上通常先用干法制备高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,析出高铁酸钾。干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2==2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中还原剂为
(3)常温下,高铁酸钾能氧化浓盐酸生成氯气,该反应离子方程式为
(4)比亚迪双模电动汽车使用高铁电池供电,其电池反应为3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为(5)工业上可用K2FeO4溶液氧化废水中的还原性污染物M,为研究反应效果,设计如下所示的对比实验探究温度、浓度、pH对降解速率和反应效果的影响,实验测得M的浓度与时间关系如图所示。

实验编号 | 温度(℃) | pH |
① | 25 | 1 |
② | 45 | 1 |
③ | 25 | 7 |
④ | 25 | 1 |
19-20高三上·安徽安庆·开学考试
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网