解答题-原理综合题 适中0.65 引用1 组卷367
NO、CO、 是大气污染物但又有着重要用途。
是大气污染物但又有着重要用途。
已知:





(1)某反应的平衡常数表达式为 ,此反应的热化学方程式为:
,此反应的热化学方程式为:______ 。
(2)向绝热恒容密闭容器中充入等量的NO和CO进行反应,能判断反应已达到化学平衡状态的是______ (填序号)。
a.容器中的压强保持不变 b.
c.气体的平均相对分子质量保持34.2不变 d.该反应平衡常数保持不变
e.NO和CO的体积比保持不变
Ⅱ.(3)甲烷转化为 和CO的反应为:
和CO的反应为:

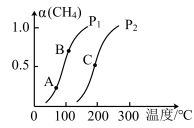
①一定条件下, 的平衡转化率与温度、压强的关系如图所示。则
的平衡转化率与温度、压强的关系如图所示。则
______  (填“<”“>”或“=”);
(填“<”“>”或“=”);
A、B、C三点处对应的平衡常数( 、
、 、
、 ),由大到小的顺序为
),由大到小的顺序为______ 。
②将 和
和 按等物质的量混合,一定条件下反应达到平衡,
按等物质的量混合,一定条件下反应达到平衡, 转化率为50%。则反应前与平衡后,混合气体的平均相对分子质量之比为
转化率为50%。则反应前与平衡后,混合气体的平均相对分子质量之比为______ 。
Ⅲ.含 的烟气可用
的烟气可用 溶液吸收。
溶液吸收。
(4)已知 时由
时由 ,和
,和 形成的混合溶液恰好呈中性,此时溶液中离子浓度大小顺序为
形成的混合溶液恰好呈中性,此时溶液中离子浓度大小顺序为______ 。(已知 时,
时, 的电离平衡常数
的电离平衡常数 ,
, )
)
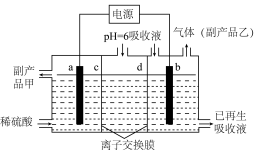
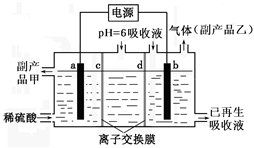
(5)可将吸收液送至电解槽再生后循环使用。再生电解槽如图所示。a电极上含硫微粒放电的反应式为______ (任写一个)。离子交换膜______ (填标号)为阴离子交换膜。
已知:
(1)某反应的平衡常数表达式为
(2)向绝热恒容密闭容器中充入等量的NO和CO进行反应,能判断反应已达到化学平衡状态的是
a.容器中的压强保持不变 b.
c.气体的平均相对分子质量保持34.2不变 d.该反应平衡常数保持不变
e.NO和CO的体积比保持不变
Ⅱ.(3)甲烷转化为

①一定条件下,
A、B、C三点处对应的平衡常数(
②将
Ⅲ.含
(4)已知
(5)可将吸收液送至电解槽再生后循环使用。再生电解槽如图所示。a电极上含硫微粒放电的反应式为

2019·天津河西·一模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



 ,
,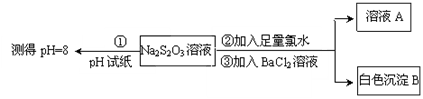
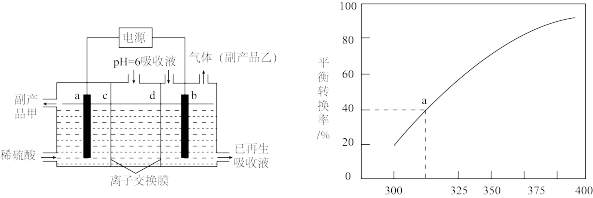
 2SO2(g)+O2(g),将一定量的SO3放入恒容的密闭容器中,测得其平衡转化率随温度变化如图所示。图中a点对应温度下,已知SO3的起始压强为P0,该温度下反应的平衡常数Kp=
2SO2(g)+O2(g),将一定量的SO3放入恒容的密闭容器中,测得其平衡转化率随温度变化如图所示。图中a点对应温度下,已知SO3的起始压强为P0,该温度下反应的平衡常数Kp= 


