单选题 较难0.4 引用1 组卷350
常温下,Ca(OH)2的溶解度为0.16克/100克水。向盛有50毫升水的烧杯中加入2克生石灰,搅拌后恢复到原温。下列说法正确的是
| A.在此过程中,水的Kw值始终保持不变 |
| B.在此过程中,Ca(OH)2的电离程度先变大后变小,最后不变 |
| C.反应结束后,溶液中水的电离程度比纯水小 |
| D.最后所得体系中的平衡状态只有水的电离平衡 |
18-19高三下·上海长宁·阶段练习
类题推荐
常温下向盛水烧杯中加2g生石灰(如下图)。搅拌后再恢复到原温,在此过程中,下列说法正确的是

| A.水的电离常数不变 |
| B.Ca(OH)2的电离程度先大后变小然最后不变 |
| C.水的电离平衡向逆反应方向移动最后不变 |
| D.水的电离度将会先变小然后变大最后不变 |
向10mL1mol/L的HCOOH溶液中不断滴加1mol/L的NaOH溶液,并一直保持常温,所加碱溶液的体积与-1gc水(H+)的关系如图所示。c水(H+)为溶液中水电离的c(H+)。下列说法中正确的是
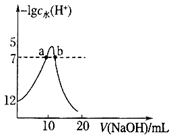

| A.常温下,Ka(HCOOH)的数量级为10-5 |
| B.a点显酸性,b点pH值为7 |
| C.从a点到b点,水的电离程度先增大后减小 |
| D.混合溶液的导电性先增强后减弱最后保持不变 |
下列说法正确的是
| A.反应A(g) |
| B.常温下,pH相同的NaOH溶液和Ba(OH)2溶液中,水的电离程度相同 |
| C.某温度氯化钠在水中的溶解度是20 g,该温度饱和氯化钠溶液的质量分数为20% |
| D.将浓度为0.1 mol/L HF溶液加水不断稀释过程中,电离平衡常数Ka(HF)保持不变, |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


