解答题-原理综合题 适中0.65 引用1 组卷327
含硫化合物在自然界中广泛存在。请按要求回答下列问题:
(1)火山喷发产生 在大气中发生如下反应:
在大气中发生如下反应:
①

②
 。
。
写出 与
与 反应产生
反应产生 和
和 的热化学方程式:
的热化学方程式:_________________ 。
(2) 和
和 混合加热的反应是
混合加热的反应是
①某温度下,在 恒容密闭容器中,通入
恒容密闭容器中,通入 和
和 ,平衡时测得
,平衡时测得 的转化率为60%,则该温度下反应的平衡常数
的转化率为60%,则该温度下反应的平衡常数
__________ 。
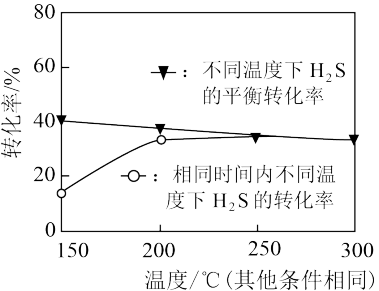
②由图分析该反应的
______ 0(填“<”“>”)。
③如图250℃以前,曲线 变化的可能原因:
变化的可能原因:_____________ 。
(3)工业上可用 碱性溶液脱硫,吸收大气污染物之一
碱性溶液脱硫,吸收大气污染物之一 。
。
①该反应的离子方程式为_______________________________ 。
②用 作催化剂,催化该反应的过程如图示:
作催化剂,催化该反应的过程如图示:
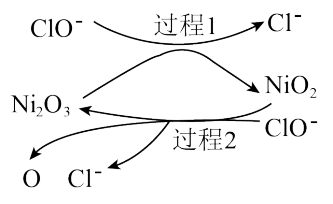
过程2中, 所起的作用是
所起的作用是______________________________ 。(填“氧化剂”“还原剂”或“既作氧化剂又作还原剂”)。
(4)不同温度下 溶液与
溶液与 酸性溶液反应速率的探究:均取
酸性溶液反应速率的探究:均取 溶液(含少量淀粉)与
溶液(含少量淀粉)与 (过量)酸性溶液混合(已知:
(过量)酸性溶液混合(已知: ),做不同温度下系列实验,
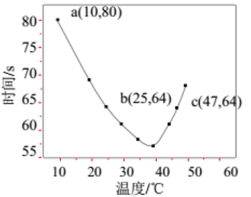
),做不同温度下系列实验, ℃间溶液由无色变蓝的时间,55℃未观察到溶液变蓝,实验记录结果如图所示:
℃间溶液由无色变蓝的时间,55℃未观察到溶液变蓝,实验记录结果如图所示:
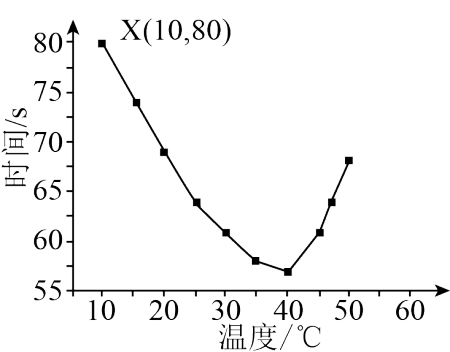
①X点 的反应速率为
的反应速率为______ 。
②40℃之前溶液由无色变蓝速率变快的主要因素是__________________ ;40℃之后溶液由无色变蓝的时间变长,且55℃未观察到溶液变蓝,可能的原因是__________________ 。
(1)火山喷发产生
①
②
写出
(2)
①某温度下,在
②由图分析该反应的
③如图250℃以前,曲线
 变化的可能原因:
变化的可能原因:
(3)工业上可用
①该反应的离子方程式为
②用

过程2中,
(4)不同温度下

①X点
②40℃之前溶液由无色变蓝速率变快的主要因素是
2019·天津河西·三模
类题推荐
碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)向碘水中加入四氯化碳后充分振荡,静置后的现象是__ 。
(2)①已知反应H2(g)+I2(g)=2HI(g),该反应中相关化学键的键能数据如表所示:
则该反应的ΔH=___ kJ·mol−1。
②下列叙述能说明上述反应已达到平衡的是___ 。
a.单位时间内生成nmolH2,同时生成nmolHI
b.温度和体积一定时,HI浓度不再变化
c.温度和体积一定时,混合气体颜色不再变化
d.温度和压强一定时,混合气体的密度不再变化
(3)NaHSO3溶液在不同温度下均可被过量KIO3(IO 被还原成I-)氧化,当NaHSO3完全消耗即有I2析出,写出I2析出时发生反应的离子方程式:
被还原成I-)氧化,当NaHSO3完全消耗即有I2析出,写出I2析出时发生反应的离子方程式:__ 。依据I2析出所需时间可以求得NaHSO3的反应速率,将浓度均为0.020mol·L-1NaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。
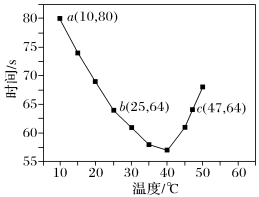
图中a点对应的NaHSO3反应速率为__ mol·L-1·s-1。b、c两点对应的NaHSO3反应速率v(b)__ v(c)(填“>”、“=”、“<”)。
(4)在1L真空密闭容器中加入amolNH4I固体,t℃时发生如下反应:
NH4I(s)=NH3(g)+HI(g)①
2NH3(g)=N2(g)+3H2(g)②
2HI(g)=I2(g)+H2(g)③
达平衡时,体系中n(HI)=bmol,n(I2)=cmol,n(H2)=dmol,则n(N2)=__ mol,t℃时反应①的平衡常数K值为__ (用字母表示)。
(1)向碘水中加入四氯化碳后充分振荡,静置后的现象是
(2)①已知反应H2(g)+I2(g)=2HI(g),该反应中相关化学键的键能数据如表所示:
| 共价键 | H-H | I-I | H-I |
| 键能/kJ·mol−1 | 436 | 151 | 299 |
则该反应的ΔH=
②下列叙述能说明上述反应已达到平衡的是
a.单位时间内生成nmolH2,同时生成nmolHI
b.温度和体积一定时,HI浓度不再变化
c.温度和体积一定时,混合气体颜色不再变化
d.温度和压强一定时,混合气体的密度不再变化
(3)NaHSO3溶液在不同温度下均可被过量KIO3(IO

图中a点对应的NaHSO3反应速率为
(4)在1L真空密闭容器中加入amolNH4I固体,t℃时发生如下反应:
NH4I(s)=NH3(g)+HI(g)①
2NH3(g)=N2(g)+3H2(g)②
2HI(g)=I2(g)+H2(g)③
达平衡时,体系中n(HI)=bmol,n(I2)=cmol,n(H2)=dmol,则n(N2)=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网