解答题-实验探究题 适中0.65 引用1 组卷287
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2•2H2O晶体,加入___________________ ,调节pH=4过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2•2H2O晶体。在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,原因是(用化学方程式表示)______________________________________________________________________ 。
(2) 由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是________________________ 。
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I―发生反应的氧化性质杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL(已知:I2+2 =
= +2I―)
+2I―)
①可选用___________ 作滴定指示剂,滴定终点的现象是_________________________ 。
②CuCl2溶液与KI反应的离子方程式为_____________________________________ 。(已知在相同条件下CuCl的溶解度大于CuI)
③该试样中CuCl2•2H2O的质量百分数为__________________________________ 。
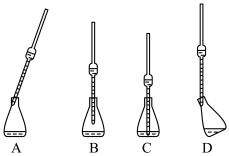
④如果试样是液体,用移液管移取时,下列使用正确的是_____________________ 。
(2) 由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I―发生反应的氧化性质杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL(已知:I2+2
①可选用
②CuCl2溶液与KI反应的离子方程式为
③该试样中CuCl2•2H2O的质量百分数为
④如果试样是液体,用移液管移取时,下列使用正确的是

18-19高二下·浙江绍兴·期中
类题推荐
常温下,几种物质的溶度积常数见下表:
(1)某酸性CuCl2溶液中含少量的FeCl3,为制得纯净的CuCl2溶液,宜加入________ 调至溶液pH=4,使Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=____________________ 。
(2)过滤后,将所得滤液经过_________ 、_______ 操作,可得到CuCl2·2H2O晶体。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.800 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液40.00 mL。(已知:I2+2S2O =S4O
=S4O +2I-)。
+2I-)。
①可选用_______________ 作指示剂。
②CuCl2溶液与KI反应的离子方程式为_______________ 。
③该试样中CuCl2·2H2O的质量百分数为________ 。
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含少量的FeCl3,为制得纯净的CuCl2溶液,宜加入
(2)过滤后,将所得滤液经过
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.800 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液40.00 mL。(已知:I2+2S2O
①可选用
②CuCl2溶液与KI反应的离子方程式为
③该试样中CuCl2·2H2O的质量百分数为
常温下,几种物质的溶度积常数见下表:
(1)某酸性CuCl2溶液中含少量的FeCl3,为制得纯净的CuCl2溶液,宜加入___________ 调至溶液pH=4,使Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=___________ 。
过滤后,将所得滤液经浓缩、过滤、洗涤、低温干燥操作,可得到CuCl2·2H2O晶体。
(2)由CuCl2·2H2O晶体得到纯的无水CuCl2,需要进行的操作是___________ 。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.800g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。向其中加入淀粉溶液后,用0.1000 mol∙L−1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液40.00mL。(已知:I2+2S2O =S4O
=S4O +2I-)。
+2I-)。
①CuCl2溶液与KI反应的离子方程式为___________ 。
②选用淀粉溶液作指示剂,滴定终点的现象是___________ 。
③该试样中CuCl2·2H2O的质量百分数为___________ 。
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10−20 | 2.6×10−39 | 1.7×10−7 | 1.3×10−12 |
过滤后,将所得滤液经浓缩、过滤、洗涤、低温干燥操作,可得到CuCl2·2H2O晶体。
(2)由CuCl2·2H2O晶体得到纯的无水CuCl2,需要进行的操作是
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.800g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。向其中加入淀粉溶液后,用0.1000 mol∙L−1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液40.00mL。(已知:I2+2S2O
①CuCl2溶液与KI反应的离子方程式为
②选用淀粉溶液作指示剂,滴定终点的现象是
③该试样中CuCl2·2H2O的质量百分数为
常温下,几种物质的溶度积常数如下表:
(1)某酸性 溶液中含少量的
溶液中含少量的 ,为制得纯净
,为制得纯净 溶液,宜加入
溶液,宜加入_______ 调至溶液pH=4,使 转化为
转化为 沉淀,此时溶液中
沉淀,此时溶液中
_______ 。
(2)过滤后,将所得滤液经过_______ 、_______ 、过滤等操作,可得到 晶体。
晶体。
(3)由 晶体得到纯的无水
晶体得到纯的无水 ,需要进行的操作是
,需要进行的操作是_______ 。
(4)某学习小组用“间接碘量法”测定含有 晶体的试样(不含能与
晶体的试样(不含能与 发生反应的氧化性杂质)的纯度,过程如下:取0.800g试样溶于水,加入过量KI固体。充分反应,生成白色沉淀(CuI)。用0.1000ml/L
发生反应的氧化性杂质)的纯度,过程如下:取0.800g试样溶于水,加入过量KI固体。充分反应,生成白色沉淀(CuI)。用0.1000ml/L 标准溶液滴定,达到滴定终点时,消耗
标准溶液滴定,达到滴定终点时,消耗 标准溶液40.00mL。(已知:
标准溶液40.00mL。(已知: )
)
①可选用_______ 作指示剂,滴定终点的现象是_______ 。
② 溶液与KI反应的离子方程式为
溶液与KI反应的离子方程式为_______ 。
③该试样中 的质量分数为
的质量分数为_______ 。
| 物质 | CuI | |||
(2)过滤后,将所得滤液经过
(3)由
(4)某学习小组用“间接碘量法”测定含有
①可选用
②
③该试样中
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


