解答题-工业流程题 适中0.65 引用1 组卷145
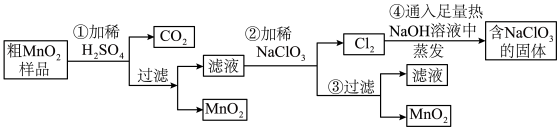
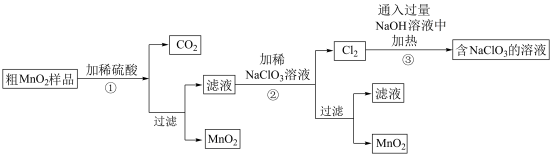
MnO2是重要化学物质,某学习小组设计了将粗MnO2(含有较多的MnO、MnCO3和Fe2O3)样品转化为纯MnO2实验,其流程如下:
回答下列问题:
(1)第②步操作中,氧化性强弱顺序:ClO3-________ (填“>”或“<”)MnO2,当NaClO3转移2 mol电子时,生成的氧化产物的物质的量为________ mol。NaClO3在常温下能够与盐酸反应生成氯气,该反应的离子方程式为___________________ 。
(2)第④步操作中,最终得到的固体除NaClO3外,还一定含有下列物质中的_____ (填字母)。
a. NaCl b. NaClO c. NaClO4 d. NaOH
(3)已知测定锰的一种方法是:锰离子转化为高锰酸根离子,反应体系中有H+、Mn2+、H2O、IO3-、MnO4-、IO4-。有关反应的离子方程式为_____________ 。
(4)氯酸是一种强酸,氯酸的浓度超过40%,就会迅速分解,反应的方程式为:8HClO3 = 3O2 ↑+ 2Cl2 ↑+ 4HClO4 + 2H2O,所得混合气体的平均式量为_______ 。

回答下列问题:
(1)第②步操作中,氧化性强弱顺序:ClO3-
(2)第④步操作中,最终得到的固体除NaClO3外,还一定含有下列物质中的
a. NaCl b. NaClO c. NaClO4 d. NaOH
(3)已知测定锰的一种方法是:锰离子转化为高锰酸根离子,反应体系中有H+、Mn2+、H2O、IO3-、MnO4-、IO4-。有关反应的离子方程式为
(4)氯酸是一种强酸,氯酸的浓度超过40%,就会迅速分解,反应的方程式为:8HClO3 = 3O2 ↑+ 2Cl2 ↑+ 4HClO4 + 2H2O,所得混合气体的平均式量为
18-19高二下·辽宁大连·期末
类题推荐
KMnO4和MnO2都是重要化学物质,在实验室可以做氧化剂和催化剂,某学习小组对两种物质的制备和性质探究如下:
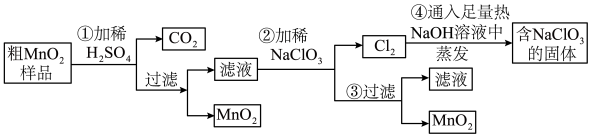
Ⅰ.MnO2的制备:该学习小组设计了将粗MnO2(含有较多的MnO、MnCO3和Fe2O3)样品转化为纯MnO2实验,其工艺流程如下:
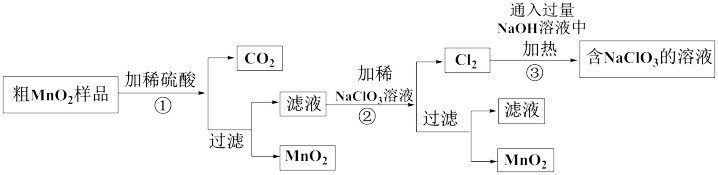
请回答下列问题:
(1)第①步操作中,生成CO2的化学方程式为___________
(2)第②步操作中,NaClO3氧化MnSO4的离子方程式为___________
(3)第③步操作中,最终得到的固体除NaClO3外,还一定含有的是___________
a.NaCl b.NaClO c.NaClO4 d.NaOH
(4)判断是否洗涤干净可选用的试剂是___________ (填化学式)。
(5)NaClO3和MnO2在一定条件下都可以氧化浓盐酸制取氯气,制取等量的氯气消耗NaClO3与MnO2的物质的量之比为___________
Ⅱ.KMnO4的制备和性质:
(6)该小组同学为了探究KMnO4溶液和Na2C2O4溶液的反应,将酸性KMnO4溶液逐滴滴入一定体积的Na2C2O4溶液中(温度相同,并不断振荡),记录现象如下:
①请将MnO 氧化C2O
氧化C2O 的离子方程式补充完整:
的离子方程式补充完整:___________
___________MnO +___________C2O
+___________C2O +___________=___________Mn2++___________CO2↑+___________
+___________=___________Mn2++___________CO2↑+___________
②请分析KMnO4溶液褪色时间变化的最可能原因___________
Ⅰ.MnO2的制备:该学习小组设计了将粗MnO2(含有较多的MnO、MnCO3和Fe2O3)样品转化为纯MnO2实验,其工艺流程如下:

请回答下列问题:
(1)第①步操作中,生成CO2的化学方程式为
(2)第②步操作中,NaClO3氧化MnSO4的离子方程式为
(3)第③步操作中,最终得到的固体除NaClO3外,还一定含有的是
a.NaCl b.NaClO c.NaClO4 d.NaOH
(4)判断是否洗涤干净可选用的试剂是
(5)NaClO3和MnO2在一定条件下都可以氧化浓盐酸制取氯气,制取等量的氯气消耗NaClO3与MnO2的物质的量之比为
Ⅱ.KMnO4的制备和性质:
(6)该小组同学为了探究KMnO4溶液和Na2C2O4溶液的反应,将酸性KMnO4溶液逐滴滴入一定体积的Na2C2O4溶液中(温度相同,并不断振荡),记录现象如下:
| 滴入KMnO4溶液的次序 | KMnO4溶液紫色褪去所需的时间 |
| 先滴入第1滴 | 60s |
| 褪色后,再滴入第2滴 | 15s |
| 褪色后,再滴入第3滴 | 3s |
| 褪色后,再滴入第4滴 | 1s |
___________MnO
②请分析KMnO4溶液褪色时间变化的最可能原因
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网