解答题-实验探究题 较难0.4 引用1 组卷253
某化学小组探究酸性条件下NO3-、SO42-、Fe3+三种微粒的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
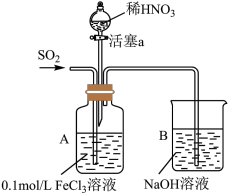
实验记录如下:
请回答下列问题:
(1)配制FeCl3溶液时,常常加入盐酸,目的是(用化学用语和简单文字叙述 ):________ 。
(2)资料表明,Fe3+能与SO2结合形成深红棕色物质Fe(SO2)63+,反应方程式为: Fe3+ + 6SO2 Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因
Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因________ 。
(3)实验II中发生反应的离子方程式是__________________ 。
(4)实验III中,浅绿色溶液变为黄色的原因是__________________ (用离子方程式表示)。
(5)实验IV中液面上方有少量红棕色气体生成,发生反应的化学方程式是______________ 。
(6)综合上述实验得出的结论是:在酸性条件下,氧化性强弱是:NO3->Fe3+>SO42-。请从微粒变化的角度解释________ 。

实验记录如下:
| 实验序号 | 实验操作 | 实验现象 |
| I | 向A装置中通入一段时间的SO2气体。 | A中黄色溶液迅速变成深红棕色,最终变为浅绿色。 |
| II | 取出少量A装置中的溶液,先加入KSCN溶液,再加入BaCl2溶液。 | 加入KSCN溶液后溶液不变色,再加入BaCl2溶液产生白色沉淀。 |
| III | 打开活塞a,将 | A中浅绿色溶液最终变为黄色。 |
| IV | 取出少量A装置中的溶液,加入KSCN溶液;向A装置中注入空气。 | 溶液变为红色;液面上方有少量红棕色气体生成。 |
(1)配制FeCl3溶液时,常常加入盐酸,目的是(
(2)资料表明,Fe3+能与SO2结合形成深红棕色物质Fe(SO2)63+,反应方程式为: Fe3+ + 6SO2
 Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因
Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因(3)实验II中发生反应的离子方程式是
(4)实验III中,浅绿色溶液变为黄色的原因是
(5)实验IV中液面上方有少量红棕色气体生成,发生反应的化学方程式是
(6)综合上述实验得出的结论是:在酸性条件下,氧化性强弱是:NO3->Fe3+>SO42-。请从微粒变化的角度解释
18-19高二下·广东揭阳·期末
类题推荐
某小组同学为比较酸性条件下NO3-、SO42-、Fe3+的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
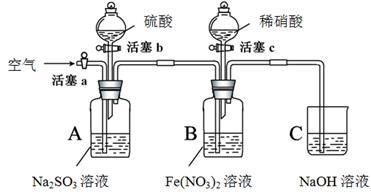
实验记录如下:
请回答下列问题:
(1)保存Fe(NO3)2溶液时,常加入铁粉,目的是(用化学方程式表示)________。
(2)实验I中,发生反应的离子方程式是________。
(3)资料表明,Fe2+能与NO结合形成深棕色物质[Fe(NO)]2+: Fe2++ NO [Fe(NO)]2+
[Fe(NO)]2+
用平衡移动原理解释实验I中溶液由深棕色变为黄色的原因是________________________。
(4)分析实验现象,同学们得出了结论。则:
① 实验IV的后续操作是________________,观察到的现象是________________。
② 由实验得出的结论是_______________________。
(5)实验反思
① 实验操作V的目的是_______________________________________。
② 实验操作III,开始时B中溶液的颜色并无明显变化,此时溶液中发生反应的离子方程式是________。
③ 有同学认为装置中的空气会干扰实验结论的得出,应在实验前通一段时间的氮气。你是否同意该看法,理由是________________________________________。

实验记录如下:
| 实验操作 | 实验现象 | |
| I | 打开活塞c,将过量稀HNO3加入装置B中,关闭活塞c | B中浅绿色溶液立即变为深棕色;一段时间后,溶液最终变为黄色。 |
| II | 用注射器取出少量B装置中的溶液,加入KSCN溶液 | 溶液变为红色。 |
| III | 打开活塞b,向A装置中加入足量硫酸,关闭活塞b | A中产生气体;B中有气泡,液面上有少量红棕色气体生成。 |
| IV | 一段时间后,用注射器取出少量B装置中的溶液,…… | …… |
| V | 打开活塞a,通入一段时间空气 | ———— |
请回答下列问题:
(1)保存Fe(NO3)2溶液时,常加入铁粉,目的是(用化学方程式表示)________。
(2)实验I中,发生反应的离子方程式是________。
(3)资料表明,Fe2+能与NO结合形成深棕色物质[Fe(NO)]2+: Fe2++ NO
 [Fe(NO)]2+
[Fe(NO)]2+用平衡移动原理解释实验I中溶液由深棕色变为黄色的原因是________________________。
(4)分析实验现象,同学们得出了结论。则:
① 实验IV的后续操作是________________,观察到的现象是________________。
② 由实验得出的结论是_______________________。
(5)实验反思
① 实验操作V的目的是_______________________________________。
② 实验操作III,开始时B中溶液的颜色并无明显变化,此时溶液中发生反应的离子方程式是________。
③ 有同学认为装置中的空气会干扰实验结论的得出,应在实验前通一段时间的氮气。你是否同意该看法,理由是________________________________________。
某化学小组探究酸性条件下NO 、SO
、SO 、Fe3+三种微粒的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验,忽略氧气对反应的影响)。
、Fe3+三种微粒的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验,忽略氧气对反应的影响)。
查阅资料已知:
①可用KSCN溶液检验溶液中Fe3+的存在(显红色),但与Fe2+不显色。
②在氧化还原反应中稀硝酸做氧化剂时,生成的还原产物是污染性无色NO气体,NO气体常温下与氧气反应生成红棕色污染性气体NO2。

实验记录如下:
请回答下列问题:
(1)指出仪器a的名称_________ 。
(2)写出A装置中通入二氧化硫气体发生反应的离子方程式_________ 。
(3)实验Ⅱ中发生反应的离子方程式是_________ 。
(4)实验Ⅲ中,浅绿色溶液变为黄色的原因是_________ 。(用语言叙述)。
(5)若将实验Ⅳ改为:往A中通入空气,液面上方的现象_________ 。
(6)综合上述实验得出的结论是:在酸性条件下,氧化性强弱顺序为_________ 。
查阅资料已知:
①可用KSCN溶液检验溶液中Fe3+的存在(显红色),但与Fe2+不显色。
②在氧化还原反应中稀硝酸做氧化剂时,生成的还原产物是污染性无色NO气体,NO气体常温下与氧气反应生成红棕色污染性气体NO2。

实验记录如下:
| 实验 | 实验操作 | 实验现象 |
| I | 向A装置中通入一段时间的SO2气体 | A中溶液最终变为浅绿色 |
| Ⅱ | 取出少量A装置中的溶液,先加入KSCN溶液,再加入BaCl2溶液 | 加入KSCN溶液后溶液不变色,再加入BaCl2溶液产生白色沉淀 |
| Ⅲ | 打开活塞a,将过量稀HNO3加入装置A中,关闭活塞a | A中浅绿色溶液最终变为黄色 |
| Ⅳ | 取出Ⅲ中少量A装置中的溶液,加入KSCN溶液 | 溶液变为红色 |
(1)指出仪器a的名称
(2)写出A装置中通入二氧化硫气体发生反应的离子方程式
(3)实验Ⅱ中发生反应的离子方程式是
(4)实验Ⅲ中,浅绿色溶液变为黄色的原因是
(5)若将实验Ⅳ改为:往A中通入空气,液面上方的现象
(6)综合上述实验得出的结论是:在酸性条件下,氧化性强弱顺序为
某化学小组探究酸性条件下NO 、SO
、SO 、Fe3+三种微粒的氧化性强弱,设计如图实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
、Fe3+三种微粒的氧化性强弱,设计如图实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
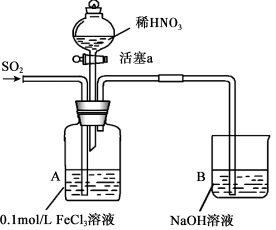
实验记录如表:
请回答下列问题:
(1)指出仪器a的名称_______ 。
(2)写出A装置中通入二氧化硫气体发生反应的离子方程式_______ 。
(3)实验Ⅱ中发生反应的离子方程式是_______ 。
(4)实验Ⅲ中,浅绿色溶液变为黄色的原因是_______ 。(用语言叙述)。
(5)若将实验Ⅳ改为:往A中通入空气,液面上方的现象是_______ 。
(6)综合上述实验得出的结论是:在酸性条件下,氧化性强弱顺序为_______ 。

实验记录如表:
| 选项 | 实验操作 | 实验现象 |
| Ⅰ | 向A装置中通入一段时间SO2气体 | A中溶液最终变为浅绿色 |
| Ⅱ | 取出少量A装置中的溶液,先加入KSCN溶液,再加入BaCl2溶液 | 加入KSCN溶液后溶液不变色,再加入BaCl2溶液产生白色沉淀 |
| Ш | 打开活塞a,将过量HNO3加入装置A中,关闭活塞a | A中浅绿色溶液最终变为黄色 |
| Ⅳ | 取出Ш中少量A装置中的溶液,加入KSCN溶液 | 溶液变为红色 |
(1)指出仪器a的名称
(2)写出A装置中通入二氧化硫气体发生反应的离子方程式
(3)实验Ⅱ中发生反应的离子方程式是
(4)实验Ⅲ中,浅绿色溶液变为黄色的原因是
(5)若将实验Ⅳ改为:往A中通入空气,液面上方的现象是
(6)综合上述实验得出的结论是:在酸性条件下,氧化性强弱顺序为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


