解答题-原理综合题 适中0.65 引用1 组卷29
金属及其化合物在生活中应用广泛。
Ⅰ.铁的腐蚀示意图如下所示:
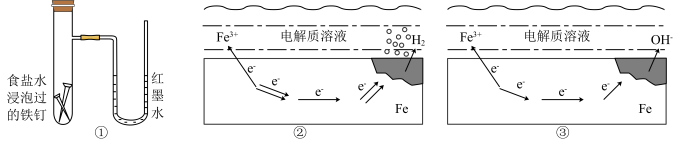
(1)装置①的反应原理和示意图__________ 的反应原理一致(填“②”或“③”)。
(2)装置图①U形管的现象是________ ,原因是_______ (用电极反应表示)。
Ⅱ.银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电场和照明器材等领域亦有广泛应用。某原电池装置如下图所示:
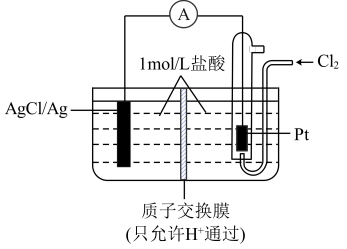
(3)负极的电极反应为__________ 。
(4)当电路中转移amole-时,交换膜左侧溶液中约减少__________ mol离子。
(5)已知Ksp(AgCl)=1.8×10-10,若向50mL0.018mol·L-1的AgNO3溶液中加入50mL0.020mol·L-1的盐酸,混合后溶液中的Ag+的浓度为__________ mol·L-1,pH为__________ 。
Ⅰ.铁的腐蚀示意图如下所示:

(1)装置①的反应原理和示意图
(2)装置图①U形管的现象是
Ⅱ.银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电场和照明器材等领域亦有广泛应用。某原电池装置如下图所示:

(3)负极的电极反应为
(4)当电路中转移amole-时,交换膜左侧溶液中约减少
(5)已知Ksp(AgCl)=1.8×10-10,若向50mL0.018mol·L-1的AgNO3溶液中加入50mL0.020mol·L-1的盐酸,混合后溶液中的Ag+的浓度为
17-18高二上·广东·期中
类题推荐
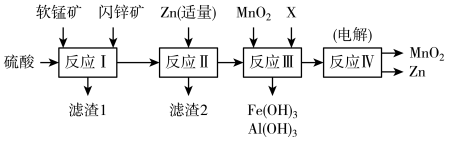
铋(Bi)与氮同族,氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂、油漆调色、生产金属铋等。一种用火法炼铜过程产生的铜转炉烟尘(除含铋的化合物之外,还有CuSO4、ZnSO4、CuS、Fe2O3、PbSO4及As2O3)制备高纯氯氧化铋的工艺流程如下:
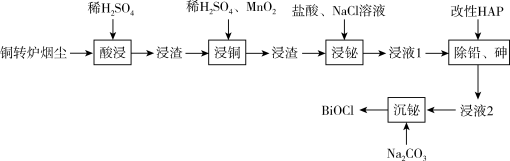
请回答:
(1)Bi位于第六周期,其原子结构示意图为__________________________________ 。
(2)向“酸浸”所得浸液中加入Zn粉,充分反应后过滤,从溶液中获得ZnSO4·7H2O的操作为__________ 、过滤、洗涤、干燥。
(3)“浸铜”时,有单质硫生成,其离子方程式为____________________________ 。
(4)“浸铋”时,温度升高,铋的浸出率降低,其原因为____________________________ 。
(5)“除铅、砷”时,可以采用以下两种方法。
①加入改性HAP。浸液1与HAP的液固比(L/S)与铅、砷去除率以及后续沉铋量的关系如下表:
实验中应采用的L/S=_________________________ 。
②铁盐氧化法,向浸液1中加入Fe2(SO4)3,并调节pH,生成FeAsO4沉淀。欲使溶液中c(AsO )<10-9mol/L且不产生Fe(OH)3沉淀,应控制pH的范围为
)<10-9mol/L且不产生Fe(OH)3沉淀,应控制pH的范围为__________ 。
已知:1g2=0.3:;FeAsO4、Fe(OH)3的Ksp分别为5×10-23、4×10-38。
(6)“沉铋“时需控制溶液的pH=3.0,此时BiCl3发生反应的化学方程式为___________________ 。

请回答:
(1)Bi位于第六周期,其原子结构示意图为
(2)向“酸浸”所得浸液中加入Zn粉,充分反应后过滤,从溶液中获得ZnSO4·7H2O的操作为
(3)“浸铜”时,有单质硫生成,其离子方程式为
(4)“浸铋”时,温度升高,铋的浸出率降低,其原因为
(5)“除铅、砷”时,可以采用以下两种方法。
①加入改性HAP。浸液1与HAP的液固比(L/S)与铅、砷去除率以及后续沉铋量的关系如下表:
| L/S | 125:1 | 50:1 | 25:1 | 15:1 |
| Pb2+去除率/% | 84.86 | 94.15 | 95.40 | 96.83 |
| As3+去除率/% | 98.79 | 98.92 | 98.34 | 99.05 |
| m(沉铋)/g | 2.34 | 2.33 | 2.05 | 1.98 |
实验中应采用的L/S=
②铁盐氧化法,向浸液1中加入Fe2(SO4)3,并调节pH,生成FeAsO4沉淀。欲使溶液中c(AsO
已知:1g2=0.3:;FeAsO4、Fe(OH)3的Ksp分别为5×10-23、4×10-38。
(6)“沉铋“时需控制溶液的pH=3.0,此时BiCl3发生反应的化学方程式为
一维纳米材料因其特殊的纳米结构,呈现出一系列独特的光、电、磁、催化等性能,具有十分广阔的应用前景。ZnS-C(ZnS纳米粒子分散在碳纳米材料上)是新型一维纳米材料,某科研小组用下列流程制备ZnS-C纳米材料。
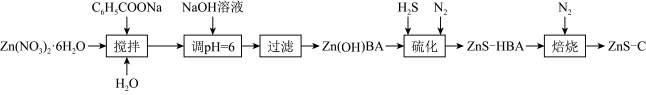
已知:BA表示C6H5COO
回答下列问题:
(1)“搅拌”后所得溶液显__________ (填“酸性”“中性”或“碱性”)。
(2)配制NaOH溶液时,蒸馏水要煮沸的原因是____________ 。
(3)向混合盐溶液中缓缓滴加NaOH溶液,促进相关离子的水解,出现Zn(OH)(C6H5COO)白色沉淀。
①写出生成沉淀的离子方程式_________ 。
②25℃,调pH=6,不产生Zn(OH)2沉淀,该溶液中c(Zn2+)<____ mol·L-1。[已知Ksp[Zn(OH)2]=1.2×10-17]
(4)“硫化”、“焙烧”过程,Zn(OH)BA通过原位固相反应制备ZnS-C纳米纤维的过程示意图如下:

①该过程中一直处于原位的离子是____________ ;
②在N2氛围中“焙烧”时,HBA(C6H5COOH)分解的化学方程式为___________ 。
(5)用N2吸附法对不同焙烧温度下制备得到的ZnS-C纳米纤维的比表面积进行测定,在不同温度(400℃-800℃)下焙烧所得ZnS-C纳米纤维的比表面积如下表:
① 随着温度的升高,ZnS纳米粒子__________ (填“变大”“不变”或“变小”)。
② ZnS-C纳米纤维可将N2吸附在其表面,形成均匀的单分子层。氮气分子横截面积为0.162 nm2,则在400℃焙烧所得的1g ZnS-C纳米纤维最大吸附的氮分子数为______ (保留3位有效数字)。

已知:BA表示C6H5COO
回答下列问题:
(1)“搅拌”后所得溶液显
(2)配制NaOH溶液时,蒸馏水要煮沸的原因是
(3)向混合盐溶液中缓缓滴加NaOH溶液,促进相关离子的水解,出现Zn(OH)(C6H5COO)白色沉淀。
①写出生成沉淀的离子方程式
②25℃,调pH=6,不产生Zn(OH)2沉淀,该溶液中c(Zn2+)<
(4)“硫化”、“焙烧”过程,Zn(OH)BA通过原位固相反应制备ZnS-C纳米纤维的过程示意图如下:

①该过程中一直处于原位的离子是
②在N2氛围中“焙烧”时,HBA(C6H5COOH)分解的化学方程式为
(5)用N2吸附法对不同焙烧温度下制备得到的ZnS-C纳米纤维的比表面积进行测定,在不同温度(400℃-800℃)下焙烧所得ZnS-C纳米纤维的比表面积如下表:
| t/℃ | 400 | 500 | 600 | 700 | 800 |
| 比表面积/m2 ·g-1 | 130.1 | 123.1 | 70.2 | 49.2 | 47.6 |
② ZnS-C纳米纤维可将N2吸附在其表面,形成均匀的单分子层。氮气分子横截面积为0.162 nm2,则在400℃焙烧所得的1g ZnS-C纳米纤维最大吸附的氮分子数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网