解答题-实验探究题 0.4 引用1 组卷386
氯化亚砜又称亚硫酰氯,其分子式为 SOCl2,常温常压下为淡黄色液体,遇水易水解。国内的氯化亚砜主要应用于医药、农药、染料等行业。实验室用干燥纯净的 Cl2、SO2和 SCl2制备 SOCl2的部分装置如图所示:
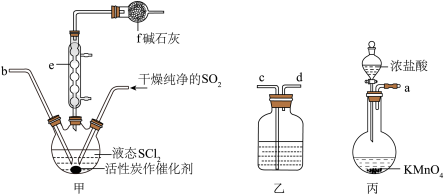
已知:①SOCl2沸点为 78.8℃,SCl2 的沸点为 50℃,且两种液体可互溶。
②SOCl2遇水剧烈反应,液面上产生白雾,并有气体产生。
请回答:
(1)实验室制取 SOCl2的反应方程式为____________
(2)写出丙中发生的离子反应_____________
(3)仪器 e 的名称是___________ ,实验仪器的连接顺序为a→_________ (仪器可以重复使用)。
(4)仪器 f 的作用是____________
(5)实验结束后,将三颈烧瓶中混合物分离的实验操作名称是______ 。
(6)工业上常用 ZnCl2·2H2O 与 SOCl2共热制取 ZnCl2。写出用惰性电极电解ZnCl2和盐酸的混合溶液的总反应离子反应式为_______ 。甲同学认为 SOCl2还可用作FeCl3·6H2O 制取无水 FeCl3的脱水剂,但乙同学对此提出质疑,可能的原因是____

已知:①SOCl2沸点为 78.8℃,SCl2 的沸点为 50℃,且两种液体可互溶。
②SOCl2遇水剧烈反应,液面上产生白雾,并有气体产生。
请回答:
(1)实验室制取 SOCl2的反应方程式为
(2)写出丙中发生的离子反应
(3)仪器 e 的名称是
(4)仪器 f 的作用是
(5)实验结束后,将三颈烧瓶中混合物分离的实验操作名称是
(6)工业上常用 ZnCl2·2H2O 与 SOCl2共热制取 ZnCl2。写出用惰性电极电解ZnCl2和盐酸的混合溶液的总反应离子反应式为
18-19高二下·四川内江·阶段练习


