解答题-工业流程题 适中0.65 引用1 组卷498
著名化学家徐光宪在稀土领域贡献突出,被誉为“稀土界的袁隆平”。钇是稀土元素之一,我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),工业上通过如下工艺流程制取氧化钇,并获得副产物铍。
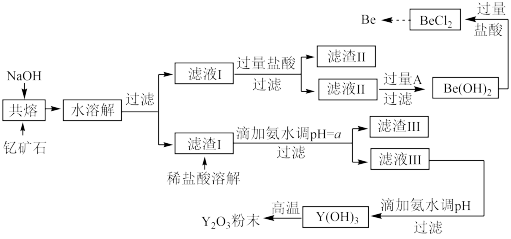
已知:ⅰ.钇(Y)的常见化合价为+3价;
ⅱ.铍和铝处于元素周期表的对角线位置,化学性质相似;
ⅲ.Fe3+、Y3+形成氢氧化物沉淀时的pH如下表:
(1)将钇矿石与NaOH共熔的反应方程式补充完整:
__ Y2FeBe2Si2O10+__ NaOH+____ 
__ Y(OH)3 +__ Fe2O3 + __ Na2SiO3 + __ Na2BeO2 + __ H2O
(2)滤渣Ⅱ的主要成分是____________ 。
(3)试剂A可以是___________ 。
A.NaOH溶液 B.氨水 C.CO2 D.CaO
(4)用氨水调节pH=a时,a的取值范围是_____________________ 。
(5)计算常温下Y3+ +3H2O Y(OH)3+3H+的平衡常数K=
Y(OH)3+3H+的平衡常数K=________ 。(常温下Ksp [Y(OH)3] = 8.0×10-23)
(6)滤液Ⅲ加入氨水产生沉淀的离子方程式为_______________ 。
(7)从BeCl2溶液中得到BeCl2固体的操作是________ 。
(8)常见的由BeCl2固体生产Be的工业方法有两种:①电解法:电解NaCl-BeCl2混合熔融盐制备Be;②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并请说明理由_________ 。

已知:ⅰ.钇(Y)的常见化合价为+3价;
ⅱ.铍和铝处于元素周期表的对角线位置,化学性质相似;
ⅲ.Fe3+、Y3+形成氢氧化物沉淀时的pH如下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.1 | 3.1 |
| Y3+ | 6.0 | 8.3 |
(2)滤渣Ⅱ的主要成分是
(3)试剂A可以是
A.NaOH溶液 B.氨水 C.CO2 D.CaO
(4)用氨水调节pH=a时,a的取值范围是
(5)计算常温下Y3+ +3H2O
(6)滤液Ⅲ加入氨水产生沉淀的离子方程式为
(7)从BeCl2溶液中得到BeCl2固体的操作是
(8)常见的由BeCl2固体生产Be的工业方法有两种:①电解法:电解NaCl-BeCl2混合熔融盐制备Be;②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并请说明理由
18-19高三下·福建龙岩·阶段练习
类题推荐
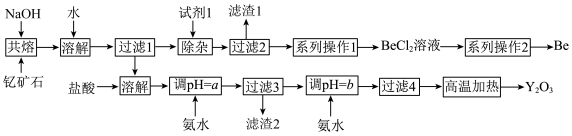
钇是稀土元素之一。我国蕴藏着丰富的钇矿石( ,其中Y为+3价),工业上通过如下工艺流程制取氧化钇,并获得副产物铍。
,其中Y为+3价),工业上通过如下工艺流程制取氧化钇,并获得副产物铍。
ii. 、
、 形成氢氧化物沉淀时的pH如下表:
形成氢氧化物沉淀时的pH如下表:
(1)钇矿石 用氧化物的形式可表示为
用氧化物的形式可表示为________ 。
(2)将钇矿石与NaOH共熔的化学方程式补充完整:_____
________ ________
________ ________
________ ________
________ ________
________ ________
________ ________
________ ________
________
(3)试剂1应加入过量的________ (填名称),滤渣1的主要成分是________ (填化学式)。
(4)“系列操作1”为除去BeCl,溶液中的杂质 ,请选择合理步骤并排序;
,请选择合理步骤并排序;________ (填序号)。
a.加入适量的盐酸 b.通入过量的 c.过滤 d.加入过量的NaOH溶液
c.过滤 d.加入过量的NaOH溶液
e.加入过量的氨水 f.洗涤
(5)为使 沉淀完全,用氨水调节
沉淀完全,用氨水调节 时,a应控制在
时,a应控制在________ 范围内;继续加氨水调节 发生反应的离子方程式为
发生反应的离子方程式为________ ;检验 是否沉淀完全的操作是
是否沉淀完全的操作是________ 。
(6)常见的由 固体生产Be的工业方法有两种:①电解法:电解
固体生产Be的工业方法有两种:①电解法:电解 混合熔融盐制备Be;②热还原法:熔融条件下,钾还原
混合熔融盐制备Be;②热还原法:熔融条件下,钾还原 制备Be。以上两种方法你认为哪种更好并说明理由:
制备Be。以上两种方法你认为哪种更好并说明理由:________ (合理即可)。
ii.
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
2.1 | 3.1 | |
6.0 | 8.3 |
(1)钇矿石
(2)将钇矿石与NaOH共熔的化学方程式补充完整:
________
(3)试剂1应加入过量的
(4)“系列操作1”为除去BeCl,溶液中的杂质
a.加入适量的盐酸 b.通入过量的
e.加入过量的氨水 f.洗涤
(5)为使
(6)常见的由
钇(Y)是一种重要的稀土金属,在激光材料和超导材料方面有着重要的应用。以硅铍钇矿(Y2FeBe2Si2O10)为原料生产氧化钇(Y2O3)的主要流程如下:

已知:①钇(Y)的常见化合价为+3;
②金属铍与铝单质及其化合物的化学性质相似;
③25℃时,相关金属离子形成氢氧化物沉淀的pH范围如表:
(1)硅铍钇矿石中Fe的化合价是_______ ,写出用氧化物形式表示硅铍钇矿石组成的化学式_______ 。
(2)将钇矿石与NaOH共熔的反应方程式补充完整:_________
_______Y2FeBe2Si2O10+_______NaOH+_______ _______Y(OH)3 +_______Fe2O3 + _______Na2SiO3 + _______Na2BeO2 + _______H2O
_______Y(OH)3 +_______Fe2O3 + _______Na2SiO3 + _______Na2BeO2 + _______H2O
(3)欲从Na2SiO3和Na2BeO2混合溶液中制得Be(OH)2沉淀。最好选用盐酸和_______两种试剂,再通过必要的操作即可实现。
(4)“滤渣I ”的主要成分为_______ ,为使Fe3+沉淀完全,需用氨水调节pH控制在_______ 范围内,检验Fe3+沉淀完全的操作方法是_______ 。
(5)煅烧草酸钇时发生分解反应,其固体产物为氧化钇,气体产物能使澄清石灰水变浑浊。写出草酸钇[Y2(C2O4)3·nH2O] 煅烧的化学方程式_______ 。
(6)常见的由BeCl2固体生产Be的工业方法有两种:
①电解法:用石墨棒和铜棒作两极,通过电解NaCl-BeCl2混合熔融盐来制备Be同时得到副产物Cl2,则铜棒上发生的电极反应式为_______ ;
②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并请说明理由_______ 。

已知:①钇(Y)的常见化合价为+3;
②金属铍与铝单质及其化合物的化学性质相似;
③25℃时,相关金属离子形成氢氧化物沉淀的pH范围如表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.1 | 3.1 |
| Y3+ | 6.5 | 7.5 |
(2)将钇矿石与NaOH共熔的反应方程式补充完整:
_______Y2FeBe2Si2O10+_______NaOH+_______
(3)欲从Na2SiO3和Na2BeO2混合溶液中制得Be(OH)2沉淀。最好选用盐酸和_______两种试剂,再通过必要的操作即可实现。
| A.NaOH溶液 | B.氨水 | C.CO2 | D.硝酸溶液 |
(5)煅烧草酸钇时发生分解反应,其固体产物为氧化钇,气体产物能使澄清石灰水变浑浊。写出草酸钇[Y2(C2O4)3·nH2O] 煅烧的化学方程式
(6)常见的由BeCl2固体生产Be的工业方法有两种:
①电解法:用石墨棒和铜棒作两极,通过电解NaCl-BeCl2混合熔融盐来制备Be同时得到副产物Cl2,则铜棒上发生的电极反应式为
②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并请说明理由
钇(Y)是一种重要的稀土金属,在激光材料和超导材料方面有着重要的应用。以硅铍钇矿(Y2FeBe2Si2O10)为原料生产氧化钇(Y2O3)的主要流程如下:
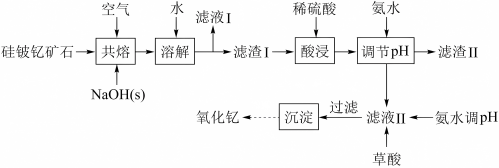
已知:①钇(Y)的常见化合价为+3;
②金属铍与铝单质及其化合物的化学性质相似;
③25℃时,相关金属离子形成氢氧化物沉淀的pH范围如表:
(1)硅铍钇矿石中Fe的化合价是___________ ,写出用氧化物形式表示硅铍钇矿石组成的化学式___________ 。
(2)将钇矿石与NaOH共熔的反应方程式补充完整:___________ 。
____Y2FeBe2Si2O10+____NaOH+____ ____Y(OH)3+____Fe2O3+___Na2SiO3+____Na2BeO2+____H2O
____Y(OH)3+____Fe2O3+___Na2SiO3+____Na2BeO2+____H2O
(3)欲从Na2SiO3和Na2BeO2混合溶液中制得Be(OH)2沉淀。最好选用盐酸和________两种试剂,再通过必要的操作即可实现。
(4)煅烧草酸钇时发生分解反应,其固体产物为氧化钇,气体产物能使澄清石灰水变浑浊。写出草酸钇[Y2(C2O4)3·nH2O]煅烧的化学方程式___________ 。
(5)常见的由BeCl2固体生产Be的工业方法有两种:
①电解法:用石墨棒和铜棒作两极,通过电解NaCl-BeCl2混合熔融盐来制备Be同时得到副产物Cl2,则铜棒上发生的电极反应式为___________ ;
②热还原法:熔融条件下,钾还原BeCl2制备Be.以上两种方法你认为哪种更好并请说明理由___________ 。

已知:①钇(Y)的常见化合价为+3;
②金属铍与铝单质及其化合物的化学性质相似;
③25℃时,相关金属离子形成氢氧化物沉淀的pH范围如表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.1 | 3.1 |
| Y3+ | 6.5 | 7.5 |
(1)硅铍钇矿石中Fe的化合价是
(2)将钇矿石与NaOH共熔的反应方程式补充完整:
____Y2FeBe2Si2O10+____NaOH+____
(3)欲从Na2SiO3和Na2BeO2混合溶液中制得Be(OH)2沉淀。最好选用盐酸和________两种试剂,再通过必要的操作即可实现。
| A.NaOH溶液 | B.氨水 | C.CO2 | D.硝酸溶液 |
(4)煅烧草酸钇时发生分解反应,其固体产物为氧化钇,气体产物能使澄清石灰水变浑浊。写出草酸钇[Y2(C2O4)3·nH2O]煅烧的化学方程式
(5)常见的由BeCl2固体生产Be的工业方法有两种:
①电解法:用石墨棒和铜棒作两极,通过电解NaCl-BeCl2混合熔融盐来制备Be同时得到副产物Cl2,则铜棒上发生的电极反应式为
②热还原法:熔融条件下,钾还原BeCl2制备Be.以上两种方法你认为哪种更好并请说明理由
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


