解答题-结构与性质 适中0.65 引用1 组卷113
铁为日常生活中常见的金属,有着广泛的用途。回答下列问题:

(1)基态铁原子的价电子轨道表示式为________________ 。
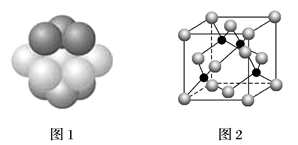
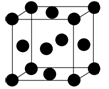
(2)Fe和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,该反应的化学方程式为___ 。
(3)已知配合物Fe(CO)x,在常温下呈液态,熔点为-20.5℃,沸点103℃,易溶于非极性溶剂。据此可判断晶体Fe(CO)x的晶体类型是_________________ 。
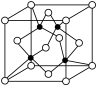
(4)Fe3O4具有许多优异的性能,在磁性材料等领域应用广泛。晶体Fe3O4的晶胞如图所示:

①晶胞中亚铁离子处于氧离子围成的_________ (填空间结构)空隙。
②晶胞中氧离子的堆积方式与某金属晶体原子堆积方式相同,该堆积方式名称为_______ 。
③解释Fe3O4晶体能导电的原因:_________________________ 。
④若晶胞的体对角线长为a nm,则Fe3O4晶体的密度为_________ g/cm3。(阿伏伽德罗常数用NA表示)

(1)基态铁原子的价电子轨道表示式为
(2)Fe和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,该反应的化学方程式为
(3)已知配合物Fe(CO)x,在常温下呈液态,熔点为-20.5℃,沸点103℃,易溶于非极性溶剂。据此可判断晶体Fe(CO)x的晶体类型是
(4)Fe3O4具有许多优异的性能,在磁性材料等领域应用广泛。晶体Fe3O4的晶胞如图所示:

①晶胞中亚铁离子处于氧离子围成的
②晶胞中氧离子的堆积方式与某金属晶体原子堆积方式相同,该堆积方式名称为
③解释Fe3O4晶体能导电的原因:
④若晶胞的体对角线长为a nm,则Fe3O4晶体的密度为
18-19高二下·福建莆田·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网