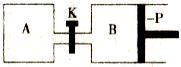解答题-原理综合题 适中0.65 引用1 组卷107
(1)已知:①Fe(s)+l/2O2(g)===FeO(s) △H1=—272.0 kJ/mol
②2Al(s)+3/2O2(g)==Al2O3(s) △H2=-1675.7 kJ/mol
A1和FeO发生铝热反应的热化学方程式是________________ 。
(2)如图所示的装置中发生反应2A2(g)+B2(g) 2C(g) △H=-akJ·mol-1(a>0),已知P是可自由滑动的活塞。在相同温度时关闭K,向A、B容器中分别充入2molA2和1molB2两容器分别在500℃时达平衡,A中C的浓度为w1mol·L-1,放出热量 bkJ,B中C的浓度为w2mol·L-1,放出热量 ckJ。请回答下列问题:
2C(g) △H=-akJ·mol-1(a>0),已知P是可自由滑动的活塞。在相同温度时关闭K,向A、B容器中分别充入2molA2和1molB2两容器分别在500℃时达平衡,A中C的浓度为w1mol·L-1,放出热量 bkJ,B中C的浓度为w2mol·L-1,放出热量 ckJ。请回答下列问题:

①此反应的平衡常数表达式为__________ ;若将温度升高到700℃,反应的平衡常数将____________ (填“增大”、“减小”或“不变”)。
②比较大小:w1________ w2(填“>”、“=”、“<”),a、b、c由大到小的关系___________ 。
③若打开K,一段时间后重新达平衡,容器B的体积将___________ (填“增大”、“减小”或“不变”)。
④若让A,B体积相等且固定P,在B中改充入4mol A2和2mol B2,在500℃时达平衡后C 的浓度为w3mol·L-1,则 w1,w3的关系___________ 。
⑤能说明A中已达到平衡状态的是________ (填序号,有一个或多个选项符合题意)。
A.υ(C)=2υ(B2)
b.容器内气体压强保持不变
c.容器中气体的平均相对分子质量不随时间而变化
d.容器内的气体密度保持不变
②2Al(s)+3/2O2(g)==Al2O3(s) △H2=-1675.7 kJ/mol
A1和FeO发生铝热反应的热化学方程式是
(2)如图所示的装置中发生反应2A2(g)+B2(g)
 2C(g) △H=-akJ·mol-1(a>0),已知P是可自由滑动的活塞。在相同温度时关闭K,向A、B容器中分别充入2molA2和1molB2两容器分别在500℃时达平衡,A中C的浓度为w1mol·L-1,放出热量 bkJ,B中C的浓度为w2mol·L-1,放出热量 ckJ。请回答下列问题:
2C(g) △H=-akJ·mol-1(a>0),已知P是可自由滑动的活塞。在相同温度时关闭K,向A、B容器中分别充入2molA2和1molB2两容器分别在500℃时达平衡,A中C的浓度为w1mol·L-1,放出热量 bkJ,B中C的浓度为w2mol·L-1,放出热量 ckJ。请回答下列问题:
①此反应的平衡常数表达式为
②比较大小:w1
③若打开K,一段时间后重新达平衡,容器B的体积将
④若让A,B体积相等且固定P,在B中改充入4mol A2和2mol B2,在500℃时达平衡后C 的浓度为w3mol·L-1,则 w1,w3的关系
⑤能说明A中已达到平衡状态的是
A.υ(C)=2υ(B2)
b.容器内气体压强保持不变
c.容器中气体的平均相对分子质量不随时间而变化
d.容器内的气体密度保持不变
18-19高二下·山西大同·期中
类题推荐
回答下列问题:
(1)在80℃时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 2NO2 ΔH>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 ΔH>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
①计算20~40s内用N2O4表示的平均反应速率为___________ mol·L-1·s-1。
②反应进行至100s后将反应混合物的温度降低,混合气体的颜色___________ (填“变浅”“变深”或“不变”)。
③要增大该反应的K值,可采取的措施有___________ (填序号)。
A.增大N2O4起始浓度 B.向混合气体中通入NO2
C.使用高效催化剂 D.升高温度
(2)已知2A2(g)+B2(g) 2C(g) ΔH=-akJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2molA2和1molB2,在500℃时充分反应达到平衡后C的浓度为wmol·L-1,放出热量bkJ。
2C(g) ΔH=-akJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2molA2和1molB2,在500℃时充分反应达到平衡后C的浓度为wmol·L-1,放出热量bkJ。
①a___________ (填“>”“=”或“<”)b。
②若将反应温度升高到700℃,该反应的平衡常数将___________ (填“增大”“减小”或“不变”)。
③能说明该反应已经达到平衡状态的是___________ 。
A.v(C)=2v(B2) B.容器内压强保持不变
C.v逆(A2)=2v正(B2) D.容器内气体的密度保持不变
④使该反应的反应速率增大,且平衡向正反应方向移动的操作是___________ 。
A.及时分离出C气体 B.适当升高温度
C.增大B2的浓度 D.选择高效的催化剂
(1)在80℃时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4
时间/s 物质n/mol | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
②反应进行至100s后将反应混合物的温度降低,混合气体的颜色
③要增大该反应的K值,可采取的措施有
A.增大N2O4起始浓度 B.向混合气体中通入NO2
C.使用高效催化剂 D.升高温度
(2)已知2A2(g)+B2(g)
①a
②若将反应温度升高到700℃,该反应的平衡常数将
③能说明该反应已经达到平衡状态的是
A.v(C)=2v(B2) B.容器内压强保持不变
C.v逆(A2)=2v正(B2) D.容器内气体的密度保持不变
④使该反应的反应速率增大,且平衡向正反应方向移动的操作是
A.及时分离出C气体 B.适当升高温度
C.增大B2的浓度 D.选择高效的催化剂
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 2C(g)
2C(g)