计算题 适中0.65 引用2 组卷281
键能的大小可用于计算化学反应的反应热(△H)。
(1)利用上表中的数据判断发生反应H2(g) + Cl2(g) = 2HCl(g)过程中,当生成1molHCl气体时需要___ (填“吸收”或“放出” )____ kJ能量。
(2)已知N2 (g)+3H2(g) = 2NH3(g) ΔH=-92 kJ/mol,则N—H键的键能是___ kJ·mol-1。
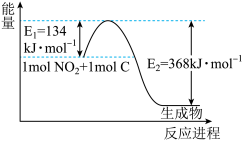
(3)1molNO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化如下图,请写出NO2和CO反应的热化学方程式:____ 。
(4)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1
②2CO(g)+O2(g)=2CO2(g) ΔH2
③H2O(g)=H2O(l) ΔH3
则CH3OH(l)+O2(g)= CO(g) + 2H2O(l) ΔH=_______ (用含ΔH1、ΔH2、ΔH3的式子表示)。
| 化学键 | Cl-Cl | H—H | H—Cl | N≡N |
| 键能/kJ·mol-1 | 243 | 436 | 431 | 946 |
(1)利用上表中的数据判断发生反应H2(g) + Cl2(g) = 2HCl(g)过程中,当生成1molHCl气体时需要
(2)已知N2 (g)+3H2(g) = 2NH3(g) ΔH=-92 kJ/mol,则N—H键的键能是
(3)1molNO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化如下图,请写出NO2和CO反应的热化学方程式:

(4)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1
②2CO(g)+O2(g)=2CO2(g) ΔH2
③H2O(g)=H2O(l) ΔH3
则CH3OH(l)+O2(g)= CO(g) + 2H2O(l) ΔH=
18-19高一下·内蒙古鄂尔多斯·期中
知识点:盖斯定律与热化学方程式根据△H=反应物的键能之和-生成物的键能之和进行计算根据△H=生成物的总能量之和-反应物的总能量之和进行计算 答案解析 【答案】很抱歉,登录后才可免费查看答案和解析! 立即登录
类题推荐
通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。键能的大小可用于估算化学反应的反应热(△H)。
(1)按要求完成填空
a.2HCl(g) = H2(g)+Cl2(g);△H=______________________
b.N2 (g)+3H2(g)= 2NH3(g) ΔH=-92kJ/mol,则N—H键的键能是__________ kJ·mol
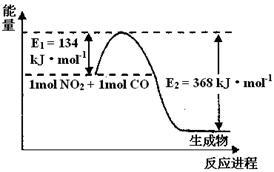
(2)1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式__________________________________
(3) 已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2
③ H2O(g) = H2O(l) ΔH3
则CH3OH(l)+O2(g)=CO(g)+ 2H2O(l)ΔH =__________ (用含ΔH1、ΔH2、ΔH3的式子表示)
(4)已知:2Al (s)+ 3/2O2(g)==Al2O3(s) △H=-1644.3 kJ• mol-1
2Fe (s) +3/2O2(g)==Fe2O3(s) △H=-815.88kJ• mol-1
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式_______________________ 。
| 化学键 | Cl-Cl | H—H | H—Cl | N≡N |
| 键能/kJ·mol | 243 | 436 | 431 | 946 |
(1)按要求完成填空
a.2HCl(g) = H2(g)+Cl2(g);△H=
b.N2 (g)+3H2(g)= 2NH3(g) ΔH=-92kJ/mol,则N—H键的键能是
(2)1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式

(3) 已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2
③ H2O(g) = H2O(l) ΔH3
则CH3OH(l)+O2(g)=CO(g)+ 2H2O(l)ΔH =
(4)已知:2Al (s)+ 3/2O2(g)==Al2O3(s) △H=-1644.3 kJ• mol-1
2Fe (s) +3/2O2(g)==Fe2O3(s) △H=-815.88kJ• mol-1
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式
(1)S8分子可形成单斜硫和斜方硫,转化过程如下:S(s,单斜) S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是
S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是______ (填“S(单斜)”或“S(斜方)”)。
(2)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1)
热化学方程式:H2(g) + Cl2(g) = 2HCl(g) ΔH=-183 kJ·mol-1,则Cl2的键能为____ kJ·mol-1。
(3)标准状况下,6.72LC2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7kJ热量,请写出表示C2H2燃烧热的热化学方程式:____________________________ 。
(4)已知:C(石墨,s)+ O2(g) = CO2(g) ΔH1=-a kJ·mol-1
H2(g) + 1/2O2(g) = H2O(l) ΔH2=-b kJ·mol-1
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) ΔH3=-c kJ·mol-1
计算C(石墨,s)与H2(g)反应生成1 mol CH4(g)的ΔH为____ kJ·mol-1 (用含a,b,c的式子表示)。
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成2 mol N2理论上放出的热量为__________ 。

 S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是
S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是(2)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1)
| 化学键 | H—H | H—Cl |
| 键能 | 436 | 431 |
热化学方程式:H2(g) + Cl2(g) = 2HCl(g) ΔH=-183 kJ·mol-1,则Cl2的键能为
(3)标准状况下,6.72LC2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7kJ热量,请写出表示C2H2燃烧热的热化学方程式:
(4)已知:C(石墨,s)+ O2(g) = CO2(g) ΔH1=-a kJ·mol-1
H2(g) + 1/2O2(g) = H2O(l) ΔH2=-b kJ·mol-1
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) ΔH3=-c kJ·mol-1
计算C(石墨,s)与H2(g)反应生成1 mol CH4(g)的ΔH为
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成2 mol N2理论上放出的热量为

依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___ 。
(2)25℃、101kPa若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量___ 。
(3)25℃、101kPa已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___ 。
(4)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
由此计算△H1=___ kJ·mol-1,已知△H2=-58kJ·mol-1,则△H3=___ kJ·mol-1。
(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
(2)25℃、101kPa若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量
(3)25℃、101kPa已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(4)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2③CO2(g)+H2(g)
 CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3回答下列问题:
已知反应①中相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C O O | H—O | C—H |
| E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算△H1=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


