填空题 0.85 引用1 组卷186
(1)过渡态理论认为:化学反应并不是通过简单的碰撞就能完成的,而是从反应物到生成物的过程中经过一个高能量的过渡态。如图是1molNO2与1mol CO恰好反应生成CO2和NO过程中的能量变化示意图。

试写出NO2和CO反应的热化学方程式:____ ,该反应的活化能是____ kJ•mol﹣1。
如图是某学生模仿如图画出的NO(g)+CO2(g)═NO2(g)+CO(g)的能量变化示意图。则图中E3=__ kJ•mol﹣1,E4=__ kJ•mol﹣1。
(2)在密闭容器中充入1mol H2和1mol I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g) 2HI(g) ΔH<0。保持容器内气体压强不变,向其中加入1molN2,反应速率
2HI(g) ΔH<0。保持容器内气体压强不变,向其中加入1molN2,反应速率____ (填“变大”、“变小”或“不变”),平衡____ 移动(填“向正反应方向”、“向逆反应方向”或“不”)。
(3)T℃,向1 L密闭容器中加入1 mol HI(g),发生反应2HI H2+I2,H2物质的量随时间的变化如图所示。
H2+I2,H2物质的量随时间的变化如图所示。
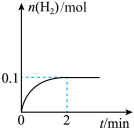
①该温度下,2HI(g) H2(g)+I2(g)的平衡常数K=
H2(g)+I2(g)的平衡常数K=____ 。
②相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则____ 是原来的2倍。
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时H2的体积分数

试写出NO2和CO反应的热化学方程式:
如图是某学生模仿如图画出的NO(g)+CO2(g)═NO2(g)+CO(g)的能量变化示意图。则图中E3=
(2)在密闭容器中充入1mol H2和1mol I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g)
(3)T℃,向1 L密闭容器中加入1 mol HI(g),发生反应2HI

①该温度下,2HI(g)
②相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时H2的体积分数
18-19高二下·江苏苏州·期中


