填空题 较难0.4 引用1 组卷157
铅的冶炼有很多种方法。
(1)瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:
① 2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) ΔH1 = a kJ·mol-1
② PbS(s)+2PbO(s)=3Pb(s)+SO2(g) ΔH2 = b kJ·mol-1
③ PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g) ΔH3 = c kJ·mol-1
反应 PbS(s)+2O2(g)=PbSO4(s) ΔH=_____ kJ·mol-1(用含 a、b、c 的代数式表示)。
(2)还原法炼铅,包含反应 PbO(s)+CO(g) Pb(s)+CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表:
Pb(s)+CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表:
①该反应的ΔH_____ 0(选填“>”、“<”或“=”)。
②当 lgK=1,在恒容密闭容器中放入 PbO 并通入 CO,达平衡时,混合气体中 CO 的体积分数为_____ (保留两位有效数字);
(3)若 T、V 不变条件下向容器中充入一定量的 N2 ,平衡_____ ;若向容器中充入一定量的 CO 气体,平衡向_____ (填“正向”、“逆向”或“不”)移动,再次达到平衡时,CO 的转化率_____ (填“增大”、“减小”或“不变”)。
(1)瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:
① 2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) ΔH1 = a kJ·mol-1
② PbS(s)+2PbO(s)=3Pb(s)+SO2(g) ΔH2 = b kJ·mol-1
③ PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g) ΔH3 = c kJ·mol-1
反应 PbS(s)+2O2(g)=PbSO4(s) ΔH=
(2)还原法炼铅,包含反应 PbO(s)+CO(g)
 Pb(s)+CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表:
Pb(s)+CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表:温度/℃ | 300 | 727 | 1227 |
lgK | 6.17 | 2.87 | 1.24 |
②当 lgK=1,在恒容密闭容器中放入 PbO 并通入 CO,达平衡时,混合气体中 CO 的体积分数为
(3)若 T、V 不变条件下向容器中充入一定量的 N2 ,平衡
18-19高二上·河南·期中
类题推荐
Ⅰ.铅的冶炼有很多种方法。
(1)瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:
①2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) △H1= a kJ•mol-1
②PbS(s)+2PbO(s)=3Pb(s)+SO2(g) △H2= b kJ•mol-1
③PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g) △H3=c kJ•mol-1
反应 3PbS(s)+6O2(g)=3PbSO4(s) △H=___________ kJ•mol-1 (用含 a、b、c 的代数式表示)。
(2)还原法炼铅,包含反应PbO(s)+CO(g) Pb(s)+CO2(g) △H,该反应的平衡常数的对数值与温度的关系如下表
Pb(s)+CO2(g) △H,该反应的平衡常数的对数值与温度的关系如下表
①该反应的△H__________ 0(选填“ >”、“< ”或“=”)。
②当1gK=1,在恒容密闭容器中放入足量的PbO并通入CO,达平衡时,混合气体中CO的体积分数为_______________ (保留两位有效数字);若平衡后再向容器中充入一定量的CO气体,平衡向_______________ (填“正向”、“逆向”或“不”)移动,再次达到平衡时,CO的转化率_______________ (填“增大”、“减小”或“不变”)。
Ⅱ.PbI2可用于人工降雨,可用滴定方法测出PbI2的Ksp。
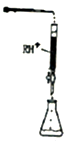
(3)取一定量的PbI2固体,用蒸馏水配制成饱和溶液,准确移取25.00mL PbI2饱和溶液分次加入阳离子交换树脂RH+(发生:2RH++PbI2=R2Pb2++2H++2I-),用锥形瓶接收流出液,最后用蒸馏水淋洗树脂至流出液呈中性,将洗涤液一并转入锥形瓶中(如图)。加入酚酞指示剂,用0.0025mol·L-1NaOH溶液滴定,当达到滴定终点时,用去氢氧化钠溶液20.00mL。确定到滴定终点时锥形瓶中现象为___________________ ,计算PbI2的Ksp为_______________ 。
(1)瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:
①2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) △H1= a kJ•mol-1
②PbS(s)+2PbO(s)=3Pb(s)+SO2(g) △H2= b kJ•mol-1
③PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g) △H3=c kJ•mol-1
反应 3PbS(s)+6O2(g)=3PbSO4(s) △H=
(2)还原法炼铅,包含反应PbO(s)+CO(g)
 Pb(s)+CO2(g) △H,该反应的平衡常数的对数值与温度的关系如下表
Pb(s)+CO2(g) △H,该反应的平衡常数的对数值与温度的关系如下表| 温度/℃ | 300 | 727 | 1227 |
| 1gK | 6.17 | 2.87 | 1.24 |
①该反应的△H
②当1gK=1,在恒容密闭容器中放入足量的PbO并通入CO,达平衡时,混合气体中CO的体积分数为
Ⅱ.PbI2可用于人工降雨,可用滴定方法测出PbI2的Ksp。
(3)取一定量的PbI2固体,用蒸馏水配制成饱和溶液,准确移取25.00mL PbI2饱和溶液分次加入阳离子交换树脂RH+(发生:2RH++PbI2=R2Pb2++2H++2I-),用锥形瓶接收流出液,最后用蒸馏水淋洗树脂至流出液呈中性,将洗涤液一并转入锥形瓶中(如图)。加入酚酞指示剂,用0.0025mol·L-1NaOH溶液滴定,当达到滴定终点时,用去氢氧化钠溶液20.00mL。确定到滴定终点时锥形瓶中现象为

CO用途广泛,工业应用时离不开平衡思想的指导:
Ⅰ.在某一容积为5 L的体积不变的密闭容器内,加入0.3 mol 的CO和0.3 mol的H2O,在有催化剂存在和800 ℃的条件下加热,发生如下反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如图:
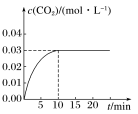
(1)若保持温度和容器的体积不变,向上述平衡体系中,再充入0.3 mol的水蒸气,重新达到平衡后,H2O的转化率___________ (填“升高”“降低”或“不变”)。
(2)在催化剂存在和800 ℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09 mol·L-1;c(CO2)=c(H2)=0.13 mol·L-1,则此时正、逆反应速率的大小: 正
正 ___________  逆(填“>”“<”或“=”)。
逆(填“>”“<”或“=”)。
Ⅱ.还原法炼铅,包含反应PbO (s)+CO(g)=Pb(s)+CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表:
(3)该反应的ΔH___________ 0(填“>”“<”或“=”)。
(4)当lg K=1,在恒容密闭容器中加入PbO并通入CO,达平衡时,混合气体中CO的体积分数为___________ (保留两位有效数字);若向容器中充入一定量的CO气体后,平衡发生移动,再次达到平衡时,CO的百分含量___________ (填“增大”“减小”或“不变”)。
Ⅰ.在某一容积为5 L的体积不变的密闭容器内,加入0.3 mol 的CO和0.3 mol的H2O,在有催化剂存在和800 ℃的条件下加热,发生如下反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如图:

(1)若保持温度和容器的体积不变,向上述平衡体系中,再充入0.3 mol的水蒸气,重新达到平衡后,H2O的转化率
(2)在催化剂存在和800 ℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09 mol·L-1;c(CO2)=c(H2)=0.13 mol·L-1,则此时正、逆反应速率的大小:
Ⅱ.还原法炼铅,包含反应PbO (s)+CO(g)=Pb(s)+CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表:
| 温度/℃ | 300 | 727 | 1 227 |
| lg K | 6.17 | 2.87 | 1.24 |
(4)当lg K=1,在恒容密闭容器中加入PbO并通入CO,达平衡时,混合气体中CO的体积分数为
CO用途广泛,工业应用时离不开平衡思想的指导:
Ⅰ.在一容积为5 L的体积不变的密闭容器内,加入0.3 mol 的CO和0.3 mol的H 2O,在催化剂存在和800 ℃的条件下加热,发生如下反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0,体系中CO2的浓度随时间变化情况如图:
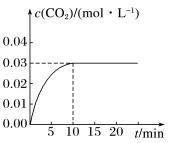
(1)该反应在800℃时的平衡常数K=_______ 。
(2)欲使平衡常数K增大,可采取的措施有_______ 。
(3)若保持温度和容器的体积不变,在上述平衡体系中,再充入0.3 mol的水蒸气,重新达到平衡后,H2O的转化率_______ (填“升高”“降低”或“不变”)。
(4)在催化剂存在和800 ℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09 mol·L-1;c(CO2)=c(H2)=0.13mol·L-1,则此时正、逆反应速率的大小:v正_______ v逆(填“>”“<”或“=”)。
Ⅱ.还原法炼铅,包含反应PbO(s)+CO(g)=Pb(s)+CO2(g) ΔH ,该反应的平衡常数的对数值与温度的关系如表:
(5)该反应的ΔH_______ 0(填“>”“<”或“=”)。
(6)当lgK=1时,在恒容密闭容器中放入PbO并通入CO,达平衡时,混合气体中CO的体积分数为_______ (保留两位有效数字);若再向容器中充入一定量的CO气体后,平衡发生移动,达到新平衡时,CO的百分含量_______ (填“增大”“减小”或“不变”)。
Ⅰ.在一容积为5 L的体积不变的密闭容器内,加入0.3 mol 的CO和0.3 mol的H 2O,在催化剂存在和800 ℃的条件下加热,发生如下反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0,体系中CO2的浓度随时间变化情况如图:

(1)该反应在800℃时的平衡常数K=
(2)欲使平衡常数K增大,可采取的措施有
(3)若保持温度和容器的体积不变,在上述平衡体系中,再充入0.3 mol的水蒸气,重新达到平衡后,H2O的转化率
(4)在催化剂存在和800 ℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09 mol·L-1;c(CO2)=c(H2)=0.13mol·L-1,则此时正、逆反应速率的大小:v正
Ⅱ.还原法炼铅,包含反应PbO(s)+CO(g)=Pb(s)+CO2(g) ΔH ,该反应的平衡常数的对数值与温度的关系如表:
| 温度/℃ | 300 | 727 | 1227 |
| lgK | 6.17 | 2.87 | 1.24 |
(5)该反应的ΔH
(6)当lgK=1时,在恒容密闭容器中放入PbO并通入CO,达平衡时,混合气体中CO的体积分数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


