解答题-结构与性质 适中0.65 引用1 组卷112
氮(N)、磷(P)、砷(As)等ⅤA元素化合物在研究和生产中有重要用途。如我国科研人员研究发现As2O3或写成As4O6,俗称砒霜)对白血病有明显的治疗作用。回答下列问题:
(1)As原子的简化的核外电子排布式为_____ ;P的第一电离能比S大的原因为________ 。
(2)写出一种与CN-互为等电子体的分子___ (用化学式表示);(SCN)2分子中σ键和π键个数比为__ 。
(3)砒霜剧毒,可用石灰消毒生成AsO33-少量AsO43-,其中AsO33-中As的杂化方式为___ ,AsO43-的空间构型为___ 。
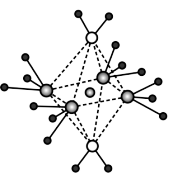
(4)NH4+中H-N-H键角比NH3中H-N-H的键角大的原因是____ ;NH3和水分子与铜离子形成的化合物中阳离子呈轴向狭长的八面体结构(如图Ⅰ),该化合物加热时首先失去水,请从原子结构角度加以分析:____ 。
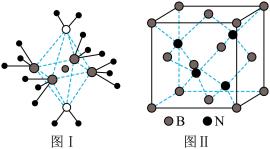
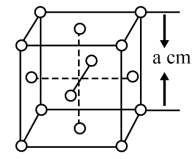
(5)BN的熔点为3000℃,密度为2.25g/cm3,其晶胞结构如上图Ⅱ所示,晶体中一个B原子周围距离最近的N原子有____ 个;若原子半径分别为rN和rB,阿伏伽德罗常数值为NA,则BN晶胞中原子的体积占晶胞体积的百分率为_____ 。
(1)As原子的简化的核外电子排布式为
(2)写出一种与CN-互为等电子体的分子
(3)砒霜剧毒,可用石灰消毒生成AsO33-少量AsO43-,其中AsO33-中As的杂化方式为
(4)NH4+中H-N-H键角比NH3中H-N-H的键角大的原因是

(5)BN的熔点为3000℃,密度为2.25g/cm3,其晶胞结构如上图Ⅱ所示,晶体中一个B原子周围距离最近的N原子有
18-19高二下·吉林松原·阶段练习
类题推荐
氮(N)、磷(P)、砷(As)等VA族元素化合物在研究和生产中有重要用途。如我国科研人员研究发现 As2O3(或写成As4O6,俗称砒霜)对白血病有明显的治疗作用回答下列问题:
(1)As原子的核外电子排布式为____ ;P的第一电离能比S大的原因为____
(2)写出一种与 互为等电子体的粒子
互为等电子体的粒子_ (用化学式表示);(SCN)2分子中 键和
键和 键个数比为
键个数比为___
(3)砒霜剧毒,可用石灰消毒生成 和少量
和少量 ,其中
,其中 中As的杂化方式为
中As的杂化方式为__ , 的空间构型为
的空间构型为___
(4)工业制备铁氧体可使用沉淀法,制备时常加入氨(NH3)、联氨(N2H4)等弱碱。
比较上表中氨(NH3)、联氨(N2H4)的熔沸点,解释其高低的主要原因____ 。苯胺分子可看做氨分子中一个氢原子被苯基取代,苯胺分子中的离域 键表示为
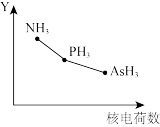
键表示为____ 。PH3是一种无色剧毒、有类似大蒜臭味的气体,它与NH3互为等电子体,二者分子中的键角关系为
_____  (填“>”或“<”)。
(填“>”或“<”)。
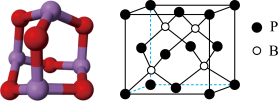
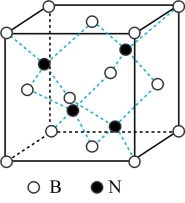
(5)BN的熔点为 ,密度为
,密度为 ,其晶胞结构如图所示,晶体中一个B原子周围距离最近的N原子有
,其晶胞结构如图所示,晶体中一个B原子周围距离最近的N原子有_______ 个;若原子半径分别为 和
和 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则BN晶胞中原子的体积占晶胞体积的百分率为
,则BN晶胞中原子的体积占晶胞体积的百分率为_______ 。
(1)As原子的核外电子排布式为
(2)写出一种与
(3)砒霜剧毒,可用石灰消毒生成
(4)工业制备铁氧体可使用沉淀法,制备时常加入氨(NH3)、联氨(N2H4)等弱碱。
| N2H4 | NH3 | |
| 熔点/℃ | 2 | -77.8 |
| 沸点/℃ | 113.5 | -33.5 |
比较上表中氨(NH3)、联氨(N2H4)的熔沸点,解释其高低的主要原因
(5)BN的熔点为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网