解答题-原理综合题 适中0.65 引用1 组卷220
亚磷酸(H3PO3)是重要的化工原料,可作尼龙增白剂、农药中间体等。
(1)亚磷酸溶液与硝酸银溶液混合生成黑色的银和一氧化氮气体,反应的化学方程式为________ 。
(2)亚磷酸为二元弱酸。
已知:
① H3PO3(aq)+NaOH(aq) NaH2PO3(aq)+H2O(l)△H=-akJ/mol
NaH2PO3(aq)+H2O(l)△H=-akJ/mol
②HCl(aq)+NaOH(aq) NaCl(aq)H2O(l)△H=-bkJ/mol
NaCl(aq)H2O(l)△H=-bkJ/mol
求H3PO3(aq) H+(aq)+H2PO3-(aq) △H=
H+(aq)+H2PO3-(aq) △H= ______
(3)25℃时,H3PO3电离常数Ka1=8.4×10-3,则NaH2PO3水解常数Kh=_____ (结果保留两位有效数字);Na2HPO3为________ (填“正盐”或“酸式盐”),其溶液显_____ (填“酸性”、“中性”、“碱性”或“无法判断”);浓度均为0.1mol/L的Na2HPO3和NaOH的混合液,加水稀释10倍后的溶液中 将
将_______ (填“增大”、“不变”或“减小”)。
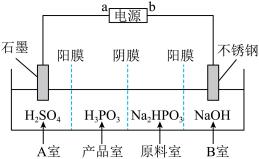
(4)亚磷酸可用电解Na2HPO3溶液来制得,装置如图所示:
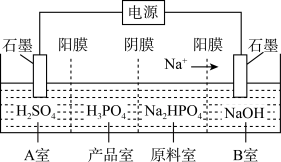
①A室的电极反应式为_________________ ;
②产品室中反应的离子方程式为____________ 。
(1)亚磷酸溶液与硝酸银溶液混合生成黑色的银和一氧化氮气体,反应的化学方程式为
(2)亚磷酸为二元弱酸。
已知:
① H3PO3(aq)+NaOH(aq)
 NaH2PO3(aq)+H2O(l)△H=-akJ/mol
NaH2PO3(aq)+H2O(l)△H=-akJ/mol②HCl(aq)+NaOH(aq)
 NaCl(aq)H2O(l)△H=-bkJ/mol
NaCl(aq)H2O(l)△H=-bkJ/mol求H3PO3(aq)
 H+(aq)+H2PO3-(aq) △H=
H+(aq)+H2PO3-(aq) △H= (3)25℃时,H3PO3电离常数Ka1=8.4×10-3,则NaH2PO3水解常数Kh=
(4)亚磷酸可用电解Na2HPO3溶液来制得,装置如图所示:

①A室的电极反应式为
②产品室中反应的离子方程式为
2019·山东聊城·一模
类题推荐
硫及其化合物在生产、生活中具有广泛的应用,根据所学知识,回答下列问题:
(1)室温下,在某NaHSO3、Na2SO3混合溶液中, 、
、 物质的量分数随pH的变化曲线如图所示,根据图示,
物质的量分数随pH的变化曲线如图所示,根据图示, 的水解平衡常数Kh=
的水解平衡常数Kh=_______

(2)室温下,某浓度的(NH4)2SO3溶液中:
①往(NH4)2SO3溶液中滴加少量的HClO溶液,发生反应的离子方程式为_______ 。
②此时所得溶液的pH_______ (“变大”、“变小”或“不变”)。
(3)亚磷酸(H3PO3)为二元弱酸,是重要的化工原料,可作尼龙增白剂、农药中间体等。25℃时,向一定体积的亚磷酸溶液中滴加等物质的量浓度的NaOH溶液,混合液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。
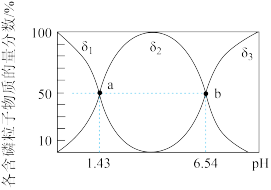
①NaH2PO3为_______ (填“正盐”或“酸式盐”),其溶液显_______ (填“酸性”、“中性”、“碱性”或“无法判断”)。
②写出NaH2PO3水解的离子方程式_______ ;
(4)现有浓度为0.02 mol/L的HCN与0.01 mol/LNaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是_______(填字母编号)。
(1)室温下,在某NaHSO3、Na2SO3混合溶液中,

(2)室温下,某浓度的(NH4)2SO3溶液中:
①往(NH4)2SO3溶液中滴加少量的HClO溶液,发生反应的离子方程式为
②此时所得溶液的pH
(3)亚磷酸(H3PO3)为二元弱酸,是重要的化工原料,可作尼龙增白剂、农药中间体等。25℃时,向一定体积的亚磷酸溶液中滴加等物质的量浓度的NaOH溶液,混合液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。

①NaH2PO3为
②写出NaH2PO3水解的离子方程式
(4)现有浓度为0.02 mol/L的HCN与0.01 mol/LNaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是_______(填字母编号)。
| A.c(H+)>c(OH-) | B.c(H+)<c(OH-) |
| C.c(H+)+c(HCN)=c(OH-) | D.c(HCN)+c(CN-)=0.01 mol/L |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 H2PO3-(aq)+H+(aq) △H=akJ/mol
H2PO3-(aq)+H+(aq) △H=akJ/mol