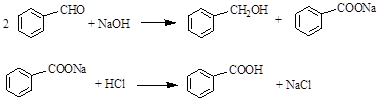解答题-实验探究题 适中0.65 引用1 组卷538
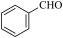
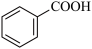
苯甲醛在浓氢氧化钾溶液中发生Cannizzaro反应,反应方程式如下,可用于制备苯甲酸和苯甲醇。
2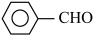 +KOH
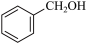
+KOH
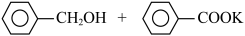 \
\
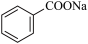
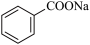
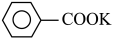 +HCl
+HCl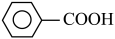
已知:
①乙醚微溶于水,是有机物良好的溶剂,沸点34.6℃,极易挥发,在空气中的沸点160℃。
②苯甲酸在水中的溶解度0.17g(25℃),0.95g(50℃),6.8g(95℃)
实验步骤:
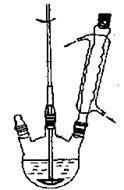
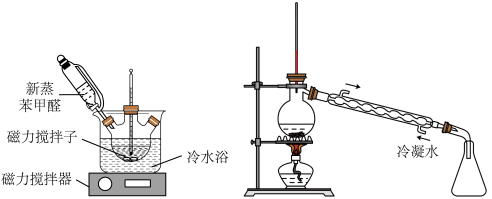
①在50mL三口瓶中加入4.5g KOH和4.5mL水,将装置置于冷水浴中,打开磁力搅拌器,分批加入5mL 新蒸苯甲醛(密度1.04g/mL),使反应物充分混合(如上左图),最后成为白色糊状物,放置24h以上。
②向反应混合物中逐渐加入足量水并振荡,使其完全溶解后倒入_____ (填装置名称)中,用10mL 乙醚萃取3次,合并乙醚萃取液,并依次用3mL饱和亚硫酸氢钠、5mL 10% Na2CO3溶液及5mL水洗涤,分出的乙醚层用无水Na2CO3干燥。
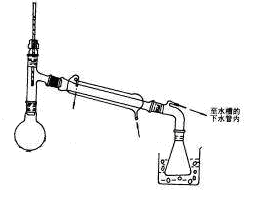
③干燥后的乙醚溶液在水浴中蒸去乙醚,然后适当调整和改造装置(如上右图),继续加热蒸馏,收集198℃~204℃的苯甲醇馏分,产量为2.16g。
④乙醚萃取后的水溶液(水层),用浓盐酸酸化并充分冷却,使苯甲酸完全析出,过滤,粗产品用水重结晶得到苯甲酸,产量是2g。
(1)不断搅拌然后放置24h的目的是____________________________________
(2)步骤②横线处装置名称是___________________________
(3)萃取液共洗涤了3次,其中10% 碳酸钠溶液欲除去的杂质是_______ (填化学式)

(4)使用水浴蒸去乙醚的优点是_____________
(5)蒸去乙醚后适当的调整和改造装置,应将上右图虚线框中的装置换为________ 。
(6)苯甲酸重结晶时,常用冷水洗涤固体,其目的是______ ;苯甲酸重结晶时所需的玻璃仪器有__________________
①烧杯 ②试管 ③锥形瓶 ④酒精灯 ⑤量筒 ⑥短颈玻璃漏斗 ⑦玻璃棒
(7)该实验中Cannizzaro反应的转化率是_____ %(保留1位小数)。通常,该实验中苯甲酸的产率会比苯甲醇更低,但若是某次实验中并未塞紧瓶塞,导致苯甲酸的产率明显偏高,分析可能的原因是__________ 。
2
 +KOH
+KOH
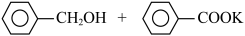 \
\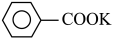 +HCl
+HCl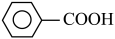

已知:
①乙醚微溶于水,是有机物良好的溶剂,沸点34.6℃,极易挥发,在空气中的沸点160℃。
②苯甲酸在水中的溶解度0.17g(25℃),0.95g(50℃),6.8g(95℃)
实验步骤:
①在50mL三口瓶中加入4.5g KOH和4.5mL水,将装置置于冷水浴中,打开磁力搅拌器,分批加入5mL 新蒸苯甲醛(密度1.04g/mL),使反应物充分混合(如上左图),最后成为白色糊状物,放置24h以上。
②向反应混合物中逐渐加入足量水并振荡,使其完全溶解后倒入
③干燥后的乙醚溶液在水浴中蒸去乙醚,然后适当调整和改造装置(如上右图),继续加热蒸馏,收集198℃~204℃的苯甲醇馏分,产量为2.16g。
④乙醚萃取后的水溶液(水层),用浓盐酸酸化并充分冷却,使苯甲酸完全析出,过滤,粗产品用水重结晶得到苯甲酸,产量是2g。
(1)不断搅拌然后放置24h的目的是
(2)步骤②横线处装置名称是
(3)萃取液共洗涤了3次,其中10% 碳酸钠溶液欲除去的杂质是

(4)使用水浴蒸去乙醚的优点是
(5)蒸去乙醚后适当的调整和改造装置,应将上右图虚线框中的装置换为
(6)苯甲酸重结晶时,常用冷水洗涤固体,其目的是
①烧杯 ②试管 ③锥形瓶 ④酒精灯 ⑤量筒 ⑥短颈玻璃漏斗 ⑦玻璃棒
(7)该实验中Cannizzaro反应的转化率是
2019·天津河东·一模
类题推荐
某化学兴趣小组在实验室中用苯甲醛制备苯甲醇和苯甲酸。有关物质的性质如表所示:
已知:2HCHO+KOH CH3OH+HCOOK
CH3OH+HCOOK
回答下列问题:
(1)向图1所示装置(夹持及加热装置已略去)中加入少量NaOH和水,搅拌溶解,稍冷,加入新蒸过的苯甲醛5.10mL,开启搅拌器,加热回流。
①长久放置的苯甲醛中易含有___ (写结构简式)杂质。
②写出三颈烧瓶内发生反应的化学方程式___ 。
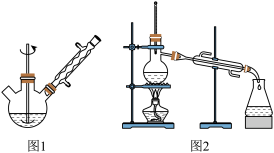
(2)停止加热,从球形冷凝管上口缓缓加入冷水,摇动,冷却后将液体倒入分液漏斗,用乙醚萃取三次,水层保留待用。合并三次萃取液,依次用饱和NaHSO3溶液、Na2CO3溶液、水洗涤。用饱和亚硫酸氢钠溶液洗涤的目的是___ ,而用碳酸钠溶液洗涤可除去醚层中极少量的苯甲酸。
(3)将洗涤后的醚层倒入干燥的锥形瓶内,加入无水MgSO4后再加上瓶塞,静置一段时间后,将锥形瓶中溶液转入图2所示蒸馏装置中,缓缓加热,蒸馏除去乙醚。当温度升到140℃时改用空气冷凝管,收集198℃~206℃的馏分。
①锥形瓶上加塞子的目的是___ ;无水硫酸镁的作用是___ 。
②蒸馏除去乙醚的过程中宜采用的加热方式为___ ;收集的198℃~206℃的馏分为___ (写名称)。
(4)将萃取后的水层慢慢地加入到盛有盐酸的烧杯中,同时用玻璃棒搅拌,析出白色固体。冷却、过滤,得到粗苯甲酸产品,然后提纯得到较纯净的产品。将苯甲酸粗产品提纯所用的实验方法为___ ,最终得到2.1g苯甲酸,其产率为__ %(保留三位有效数字)。
(5)图1和图2装置中都用了冷凝管,下列说法正确的是___ (填选项序号)。
a.两种冷凝管冷凝效果相同,本实验中可以互换使用
b.直形冷凝管一般在用蒸馏法分离物质时使用
c.两种冷凝管的冷凝水进出方向都为“高(处)进低(处)出”
d.球形冷凝管能冷凝回流反应物而减少其蒸发流失,使反应更彻底
| 苯甲醛 | 密度为1.04g/ml;微溶于水,易溶于有机溶剂;易被空气氧化;与饱和NaHSO3溶液反应产生沉淀 |
| 苯甲醇 | 沸点为205.3℃;微溶于水,易溶于醇、醚等 |
| 苯甲酸 | 熔点为121.7℃,沸点为249℃;微溶于水 |
| 乙醚 | 沸点为34.8℃;难溶于水,易燃烧,当空气中含量为1.83%~48.0%时易发生爆炸 |
回答下列问题:
(1)向图1所示装置(夹持及加热装置已略去)中加入少量NaOH和水,搅拌溶解,稍冷,加入新蒸过的苯甲醛5.10mL,开启搅拌器,加热回流。
①长久放置的苯甲醛中易含有
②写出三颈烧瓶内发生反应的化学方程式

(2)停止加热,从球形冷凝管上口缓缓加入冷水,摇动,冷却后将液体倒入分液漏斗,用乙醚萃取三次,水层保留待用。合并三次萃取液,依次用饱和NaHSO3溶液、Na2CO3溶液、水洗涤。用饱和亚硫酸氢钠溶液洗涤的目的是
(3)将洗涤后的醚层倒入干燥的锥形瓶内,加入无水MgSO4后再加上瓶塞,静置一段时间后,将锥形瓶中溶液转入图2所示蒸馏装置中,缓缓加热,蒸馏除去乙醚。当温度升到140℃时改用空气冷凝管,收集198℃~206℃的馏分。
①锥形瓶上加塞子的目的是
②蒸馏除去乙醚的过程中宜采用的加热方式为
(4)将萃取后的水层慢慢地加入到盛有盐酸的烧杯中,同时用玻璃棒搅拌,析出白色固体。冷却、过滤,得到粗苯甲酸产品,然后提纯得到较纯净的产品。将苯甲酸粗产品提纯所用的实验方法为
(5)图1和图2装置中都用了冷凝管,下列说法正确的是
a.两种冷凝管冷凝效果相同,本实验中可以互换使用
b.直形冷凝管一般在用蒸馏法分离物质时使用
c.两种冷凝管的冷凝水进出方向都为“高(处)进低(处)出”
d.球形冷凝管能冷凝回流反应物而减少其蒸发流失,使反应更彻底
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网