解答题-原理综合题 较难0.4 引用1 组卷215
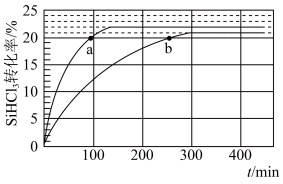
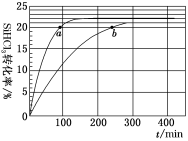
(1)对于反应2SiHCl3(g)===SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
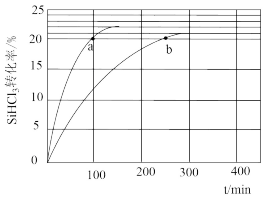
①343 K时反应的平衡转化率α=________ %。平衡常数K343 K=________ (保留2位小数)。
②在343 K下:要提高SiHCl3转化率,可采取的措施是________ ;要缩短反应达到平衡的时间,可采取的措施有________ 、________ 。
③比较a、b处反应速率大小:va________ vb(填“大于”“小于”或“等于”)。反应速率v=v正-v逆=k正x2SiHCl3-k逆xSiH2Cl2xSiCl4,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处的v正/v逆=________ (保留1位小数)。
(2)不同温度下水的离子积常数如表所示:
①请用文字解释随温度升高水的离子积增大的原因 _______________ ;
②10℃时纯水的电离平衡常数为_________ ;计算100℃时纯水中电离产生的氢离子浓度为__________________ 。

①343 K时反应的平衡转化率α=
②在343 K下:要提高SiHCl3转化率,可采取的措施是
③比较a、b处反应速率大小:va
(2)不同温度下水的离子积常数如表所示:
| t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 100 |
| Kw/10-14 | 0.114 | 0.292 | 0.681 | 1.01 | 2.92 | 5.47 | 55.0 |
②10℃时纯水的电离平衡常数为
18-19高二下·黑龙江鹤岗·开学考试
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 SiH2Cl2(g)+ SiCl4(g)
SiH2Cl2(g)+ SiCl4(g)