解答题-实验探究题 较难0.4 引用1 组卷545
某兴趣小组欲探究SO2与Cu(OH)2的反应。
(1)现象I中产生蓝色沉淀的离子方程式是___________ 。
(2)甲为了确认现象II中白色沉淀的成分,进行如下探究。查阅资料:
并进行如下实验:
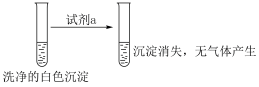
①试剂a是___________ 。
②现象II中生成白色沉淀的离子方程式是___________ 。
(3)甲认为Cu(OH)2沉淀全部转化为CuCl,乙依据实验现象对甲的观点进行反驳,依据的实验现象是_________ 。
(4)丙认为实验存在干扰,欲探究纯净的Cu(OH)2 悬浊液与SO2的反应。
①丙过滤I中的蓝色沉淀,洗涤,取最后一次洗涤液于试管中,_________ (填操作和现象),证明已洗涤干净。再进行如下实验:
②丙预测产物是Cu2O,取砖红色沉淀,洗涤后,_________ (填操作和现象),证明产物是Cu2O。
(5)纯净的Cu(OH)2 悬浊液与SO2发生反应的化学方程式是_________ 。
| 实验 | 实验步骤 | 现象 |
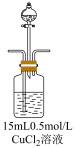 | 步骤1:打开分液漏斗,向烧瓶中加入30mL 0.5 mol/LNaOH溶液 | I. 有蓝色絮状沉淀,静置后分层。 |
| 步骤2:从左侧导管通入SO2气体 | II. 静置后分层,上层溶液为淡绿色,底部有白色沉淀 |
(2)甲为了确认现象II中白色沉淀的成分,进行如下探究。查阅资料:
| CuSO3 | CuCl | Cu2O | |
| 溶解性 | 不溶于水,浅黄色沉淀 | 不溶于水,白色沉淀 | 不溶于水,砖红色沉淀 |
| 性质 | 与酸反应 | 能溶于较浓的HCl溶液 | 酸性体系中不稳定,进一步反应生成Cu和Cu2+ |

①试剂a是
②现象II中生成白色沉淀的离子方程式是
(3)甲认为Cu(OH)2沉淀全部转化为CuCl,乙依据实验现象对甲的观点进行反驳,依据的实验现象是
(4)丙认为实验存在干扰,欲探究纯净的Cu(OH)2 悬浊液与SO2的反应。
①丙过滤I中的蓝色沉淀,洗涤,取最后一次洗涤液于试管中,
| 实验 | 实验步骤 | 现象 |
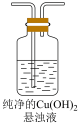 | 从左侧导管通入SO2气体 | III. 静置后分层,上层溶液为淡绿色,底部有砖红色沉淀。 |
(5)纯净的Cu(OH)2 悬浊液与SO2发生反应的化学方程式是
19-20高三上·北京昌平·期末
类题推荐
某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
(1)制取新制Cu(OH)2悬浊液的离子方程式为__________________________________ 。
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明:__________________ ,检验Cu(OH)2洗涤干净的方法是____________________________________________ 。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl+2NH3·H2O
=Cu(NH3)2++Cl-+2H2O、____________________________ 。
②乙同学用另一种方法证明了该白色沉淀为CuCl,参考如下实验方案填写表格:
填写下表空格:
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式:_________________ 。
(4)丙同学通过实验证明:实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中,_________________________________ ,则说明砖红色沉淀是Cu2O。
| 装置 | 序号 | 试管中的药品 | 现象 |
持续通入 | 实验Ⅰ | 1.5 mL1 mol/L CuSO4溶液和3.5 mL 1mol/L NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
实验Ⅱ | 1.5 mL1 mol/L CuCl2溶液和3.5 mL 1 mol/L NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(1)制取新制Cu(OH)2悬浊液的离子方程式为
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明:
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl+2NH3·H2O
=Cu(NH3)2++Cl-+2H2O、
②乙同学用另一种方法证明了该白色沉淀为CuCl,参考如下实验方案填写表格:
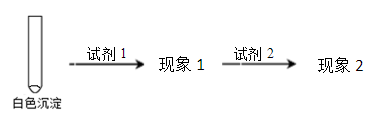
填写下表空格:
| 试剂1 | 试剂2 | 蒸馏水 | |
| 现象1 | 现象2 |
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式:
(4)丙同学通过实验证明:实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中,
高中化学学科核心素养要求进行科学探究。现对二氧化硫的性质进行深入探究。
I.实验、类比、推理是化学学习的重要方法。某课外活动小组根据 与
与 的反应,用如图所示装置探究
的反应,用如图所示装置探究 与
与 的反应,并探究其产物成分。(已知:
的反应,并探究其产物成分。(已知: 与水蒸气在加热时会发生反应)
与水蒸气在加热时会发生反应)
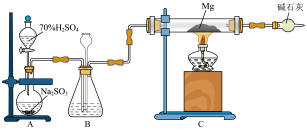
(1)装置B的作用之一是观察 的生成速率,为保证实验的严谨性其中的液体最好选择
的生成速率,为保证实验的严谨性其中的液体最好选择___________ (填序号)
a.饱和 溶液 b.饱和
溶液 b.饱和 溶液
溶液
c.饱和 溶液 d.浓硫酸
溶液 d.浓硫酸
(2)依据 与
与 的反应,三位同学对
的反应,三位同学对 与
与 反应的产物提出不同假设,并将装置
反应的产物提出不同假设,并将装置 中玻璃管内固体产物加入如下图所示的装置
中玻璃管内固体产物加入如下图所示的装置 中大试管,进一步设计实验探究
中大试管,进一步设计实验探究 与
与 反应的产物,若固体产物只有两种,依据充分反应后的现象,完成下列表格:
反应的产物,若固体产物只有两种,依据充分反应后的现象,完成下列表格:

为进一步验证假设③中 的存在,可将
的存在,可将 中试剂换成
中试剂换成___________ 。(填试剂的化学式)
II.某兴趣小组欲探究 与
与 的反应。
的反应。
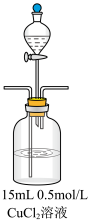
(3)甲为了确认现象II中白色沉淀的成分,进行如下探究。查阅资料:
并进行如下实验:
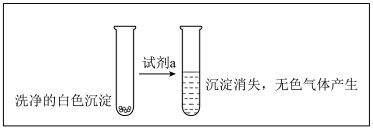
①试剂 是
是___________ 。
②现象II中生成白色沉淀的离子方程式是___________ 。
(4)乙认为实验存在干扰,欲探究纯净的 悬浊液与
悬浊液与 的反应。
的反应。
①乙过滤I中的蓝色沉淀,洗涤,取最后一次洗涤液于试管中,___________ (填操作和现象),证明已洗涤干净。再进行如下实验:
②乙预测产物是 ,取砖红色沉淀,洗涤后,
,取砖红色沉淀,洗涤后,___________ (填操作和现象),证明产物是 。
。
(5)纯净的 悬浊液与
悬浊液与 发生反应的化学方程式是
发生反应的化学方程式是___________ 。
I.实验、类比、推理是化学学习的重要方法。某课外活动小组根据

(1)装置B的作用之一是观察
a.饱和
c.饱和
(2)依据

| 假设 | ||
| ① | 固体不完全溶解,无气泡产生 | 溶液不褪色 |
| ② | 固体不完全溶解,且有气泡产生 | 溶液褪色 |
| ③ | 固体完全溶解,且有气泡产生 |
II.某兴趣小组欲探究

| 实验步骤 | 现象 |
| 步骤1:打开分液漏斗,向烧瓶中加入 | I.有蓝色絮状沉淀,静置后分层。 |
| 步骤2:从左侧导管通入 | II.静置后分层,底部有白色沉淀 |
| 物质 | |||
| 溶解性 | 不溶于水,浅黄色沉淀 | 不溶于水,白色沉淀 | 不溶于水,砖红色沉淀 |
| 性质 | 与酸反应 | 能溶于浓盐酸 | 酸性体系中不稳定,进一步反应生成Cu和 |

①试剂
②现象II中生成白色沉淀的离子方程式是
(4)乙认为实验存在干扰,欲探究纯净的
①乙过滤I中的蓝色沉淀,洗涤,取最后一次洗涤液于试管中,
| 实验 | 实验步骤 | 现象 |
 纯净的 | 从左侧导管通入 | III.静置后分层,上层溶液为蓝色,底部有砖红色沉淀 |
(5)纯净的
某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
(1)制取新制Cu(OH)2悬浊液的离子方程式为 。
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明: 。检验Cu(OH)2洗涤干净的方法是 。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl + 2NH3·H2O = Cu(NH3)2+ +Cl- + 2H2O 、 ____________ 。
②乙同学用另一种方法证明了该白色沉淀为CuCl,实验方案如下:
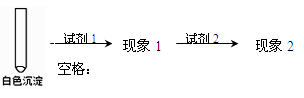
填写下表空格:
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式: 。
(4)丙同学通过实验证明实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中, _______________ ,则说明砖红色沉淀是Cu2O。
| 装置 | 序号 | 试管中的药品 | 现象 |
持续通入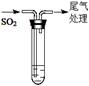 | 实验Ⅰ | 1.5 mL 1 mol·L-1 CuSO4溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
实验Ⅱ | 1.5 mL 1 mol·L-1 CuCl2溶液和3.5 mL 1 mol·L-1 NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净。向洗净后的Cu(OH)2中加入5 mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明: 。检验Cu(OH)2洗涤干净的方法是 。
(3)同学们对白色沉淀的成分继续进行探究。查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸。它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液。
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl + 2NH3·H2O = Cu(NH3)2+ +Cl- + 2H2O 、 ____________ 。
②乙同学用另一种方法证明了该白色沉淀为CuCl,实验方案如下:

填写下表空格:
| 试剂1 | 试剂2 | 蒸馏水 | |
| 现象1 | 现象2 |
(4)丙同学通过实验证明实验Ⅰ中观察到的砖红色沉淀是Cu2O。完成合理的实验方案:取少量Cu2O固体于试管中, _______________ ,则说明砖红色沉淀是Cu2O。
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


