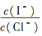解答题-工业流程题 较难0.4 引用1 组卷245
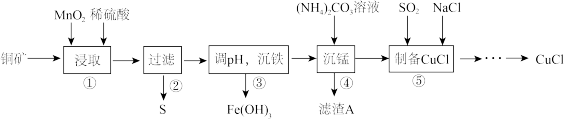
用某铜矿(含CuS以及少量FeO和Fe2O3)制备CuCl的主要流程如下:
已知Fe3+、Mn2+、Cu2+生成氢氧化物沉淀时的pH如下表所示:
(1)浸取时,CuS被浸取的离子方程式为CuS+MnO2+4H+=Cu2++Mn2++S↓+2H2O,该反应的氧化剂是________ (填化学式),Fe2O3被浸取的离子方程式为________________ 。
(2)步骤③调整pH的范围为______ ,滤渣A的成分为________ (填化学式)。
(3)“沉铁”时,需要检验Fe3+是否沉淀完全,所用的试剂为________ (填化学式)。
(4)准确称取所制备的氯化亚铜样品1.600 g,将其置于足量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用0.100 0 mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液25.00 mL,反应中Cr2O72-被还原为Cr3+,计算样品中CuCl的质量分数(写出计算过程)______ 。
已知Fe3+、Mn2+、Cu2+生成氢氧化物沉淀时的pH如下表所示:
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Mn(OH)2 | 7.1 | 10.1 |
| Cu(OH)2 | 4.7 | 6.7 |
(2)步骤③调整pH的范围为
(3)“沉铁”时,需要检验Fe3+是否沉淀完全,所用的试剂为
(4)准确称取所制备的氯化亚铜样品1.600 g,将其置于足量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用0.100 0 mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液25.00 mL,反应中Cr2O72-被还原为Cr3+,计算样品中CuCl的质量分数(写出计算过程)
18-19高二下·江苏·开学考试
类题推荐
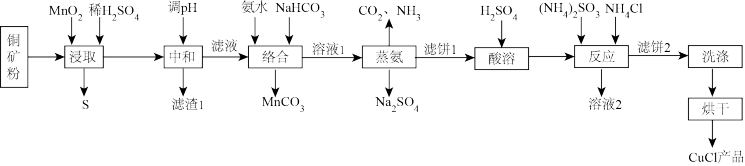
氯化亚铜是一种重要的化工原料,广泛应用于有机合成、石油、油脂、染料等工业。一种利用低品位铜矿(Cu2S、CuS及FeO和Fe2O3等)为原料制取CuCl的工艺流程如下:
已知:①CuCl难溶于醇和水,可溶于氯离子浓度较大的体系;
②CuCl在潮湿空气中易水解氧化;
③已知Cu2+、Mn2+、Fe2+、Fe3+开始生成沉淀和沉淀完全的pH如下表:
回答下列问题:
(1)“浸取”时加入MnO2的作用是_______
(2)滤渣1为_______ ,“中和”时调节pH的范围是_______
(3)“络合”时发生反应生成了配合物Cu(NH3)4CO3,该反应的化学方程式_______
(4)“反应”时的离子方程式_______ ,溶液2中存在的溶质主要有_______ 。
(5)“洗涤”时包括用pH=2的硫酸洗、水洗和乙醇洗,不能省略乙醇洗的理由是_______ 。
(6)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用amol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O 被还原为Cr3+,样品中CuCl的质量分数为
被还原为Cr3+,样品中CuCl的质量分数为_______ [杂质不参与反应;Mr(CuCl)=99.5,列出计算式即可]

已知:①CuCl难溶于醇和水,可溶于氯离子浓度较大的体系;
②CuCl在潮湿空气中易水解氧化;
③已知Cu2+、Mn2+、Fe2+、Fe3+开始生成沉淀和沉淀完全的pH如下表:
| Cu(OH)2 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀pH | 4.7 | 8.3 | 8.1 | 1.2 |
| 完全沉淀pH | 6.7 | 9.8 | 9.6 | 3.2 |
(1)“浸取”时加入MnO2的作用是
(2)滤渣1为
(3)“络合”时发生反应生成了配合物Cu(NH3)4CO3,该反应的化学方程式
(4)“反应”时的离子方程式
(5)“洗涤”时包括用pH=2的硫酸洗、水洗和乙醇洗,不能省略乙醇洗的理由是
(6)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用amol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O
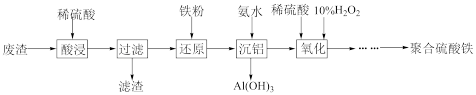
聚合硫酸铁[[Fex(OH)y(SO4)z],Fe为+3价]是高效水处理剂。实验室用某冶金厂的废渣(主要成分为Fe2O3、Al2O3和少量SiO2)制备聚合硫酸铁的流程如下:
回答下列问题:
(1)“酸浸”时,Fe2O3与稀硫酸反应的化学方程式为___________ 。
(2)滤渣的主要成分是___________ (填化学式),“还原”后,检验溶液中是否还存在Fe3+的试剂是___________ 。
(3)常温下,不同金属离子生成氢氧化物开始沉淀和完全沉淀时的pH如下表所示:
①“沉铝”时应控制溶液pH的范围是___________ 。
②写出“沉铝”时反应的离子方程式:___________ 。
(4)聚合硫酸铁[Fex(OH)y(SO4)z]的组成可通过下列实验测定:
Ⅰ.称取m g聚合硫酸铁溶于稀盐酸中,向所得溶液中滴加BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体23.30 g;
Ⅱ.另称取m g聚合硫酸铁溶于稀硫酸中,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并后用0.500 mol/L的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液32.00 mL。
①实验Ⅱ中,酸性KMnO4溶液与Fe2+反应生成Mn2+等物质的离子方程式为___________ 。
②通过计算确定该聚合硫酸铁的化学式为___________ 。

回答下列问题:
(1)“酸浸”时,Fe2O3与稀硫酸反应的化学方程式为
(2)滤渣的主要成分是
(3)常温下,不同金属离子生成氢氧化物开始沉淀和完全沉淀时的pH如下表所示:
| 金属阳离子 | Fe2+ | Fe3+ | Al3+ |
| 开始沉淀时的pH | 6.5 | 1.5 | 3.3 |
| 完全沉淀时的pH | 9.7 | 3.2 | 5.2 |
①“沉铝”时应控制溶液pH的范围是
②写出“沉铝”时反应的离子方程式:
(4)聚合硫酸铁[Fex(OH)y(SO4)z]的组成可通过下列实验测定:
Ⅰ.称取m g聚合硫酸铁溶于稀盐酸中,向所得溶液中滴加BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体23.30 g;
Ⅱ.另称取m g聚合硫酸铁溶于稀硫酸中,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并后用0.500 mol/L的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液32.00 mL。
①实验Ⅱ中,酸性KMnO4溶液与Fe2+反应生成Mn2+等物质的离子方程式为
②通过计算确定该聚合硫酸铁的化学式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网