解答题-工业流程题 适中0.65 引用1 组卷341
氯化亚铜(CuCl)常用作有机合成工业中的催化剂,在空气中迅速被氧化成绿色;见光则分解,变成褐色。如图是工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:
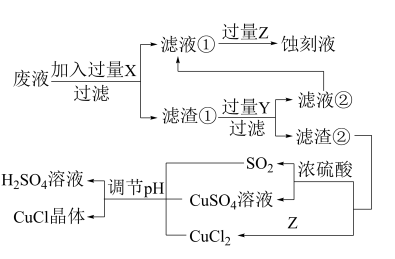
根据以上信息回答下列问题:
(1)生产过程中X的化学式为________ 。
(2)写出产生CuCl的化学方程式:_______________________________ 。
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由_____________________________________________________ ;
实际生产中SO2要适当过量,原因可能是_______________________________ (答一点即可)。
(4)实验探究pH对CuCl产率的影响如下表所示:
析出CuCl晶体最佳pH为________ ,当pH较大时CuCl产率变低,原因是______________________ 。调节pH时,________ (填“能”或“不能”)用相同pH的硝酸代替硫酸,理由__________________ 。
(5)氯化亚铜的定量分析:
①称取样品0.25 g和过量的FeCl3溶液于锥形瓶中,充分溶解。
②用0.10 mol·L-1硫酸铈标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+。三次平行实验结果如下(平行实验结果相差不能超过1%):
则样品中CuCl的纯度为________ (结果保留三位有效数字)。

根据以上信息回答下列问题:
(1)生产过程中X的化学式为
(2)写出产生CuCl的化学方程式:
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由
实际生产中SO2要适当过量,原因可能是
(4)实验探究pH对CuCl产率的影响如下表所示:
| pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| CuCl产率/% | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
析出CuCl晶体最佳pH为
(5)氯化亚铜的定量分析:
①称取样品0.25 g和过量的FeCl3溶液于锥形瓶中,充分溶解。
②用0.10 mol·L-1硫酸铈标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+。三次平行实验结果如下(平行实验结果相差不能超过1%):
| 平行实验次数 | 1 | 2 | 3 |
| 0.25 g样品消耗硫酸铈 标准溶液的体积/mL | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为
19-20高三上·辽宁·期末
类题推荐
氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸。工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程如图所示:
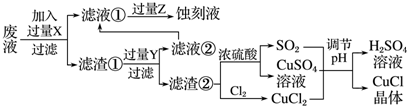
根据以上信息回答下列问题:
(1)写出生产过程中X________ ;Y________ (填化学式)。
(2)析出的CuCl晶体不用水而用无水乙醇洗涤的目的是________________________ ;生产过程中调节溶液的pH不能过大的原因是________________________ 。
(3)写出生成CuCl的化学方程式:__________________________________ 。
(4)在CuCl的生成过程中理论上不需要补充SO2气体,其理由是_________________ 。
(5)已知:常温下Ksp(CuCl)=1.6×10-7,Ksp(CuI)=1.2×10-12,现向CuCl饱和溶液中加入NaI固体至c(I-)=0.1mol/L,此时溶液中c(Cu+)/c(Cl-)=________ 。
(6)氯化亚铜的定量分析
①称取样品0.25 g置于已放入10 mL过量的FeCl3溶液的锥形瓶中,不断摇动。
②待样品溶解后,加水50 mL,邻菲罗啉指示剂2滴。
③立即用0.10 mol·L-1硫酸铈标准溶液滴定至终点,同时做空白实验一次。
已知:
CuCl+FeCl3===CuCl2+FeCl2;Fe2++Ce4+===Fe3++Ce3+。
如此再重复2次测得:
④数据处理:计算得CuCl的纯度为_________ (平行实验结果相差不能超过0.3%)。

根据以上信息回答下列问题:
(1)写出生产过程中X
(2)析出的CuCl晶体不用水而用无水乙醇洗涤的目的是
(3)写出生成CuCl的化学方程式:
(4)在CuCl的生成过程中理论上不需要补充SO2气体,其理由是
(5)已知:常温下Ksp(CuCl)=1.6×10-7,Ksp(CuI)=1.2×10-12,现向CuCl饱和溶液中加入NaI固体至c(I-)=0.1mol/L,此时溶液中c(Cu+)/c(Cl-)=
(6)氯化亚铜的定量分析
①称取样品0.25 g置于已放入10 mL过量的FeCl3溶液的锥形瓶中,不断摇动。
②待样品溶解后,加水50 mL,邻菲罗啉指示剂2滴。
③立即用0.10 mol·L-1硫酸铈标准溶液滴定至终点,同时做空白实验一次。
已知:
CuCl+FeCl3===CuCl2+FeCl2;Fe2++Ce4+===Fe3++Ce3+。
如此再重复2次测得:
| 1 | 2 | 3 | |
| 空白实验消耗硫酸铈 标准溶液的体积/mL | 0.75 | 0.50 | 0.80 |
| 0.25 g样品消耗硫酸铈 标准溶液的体积/mL | 24.65 | 25.75 | 24.90 |
④数据处理:计算得CuCl的纯度为
氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸;在空气中迅速被氧化成绿色;见光则分解,变成褐色;下图是工业上以制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程如下:
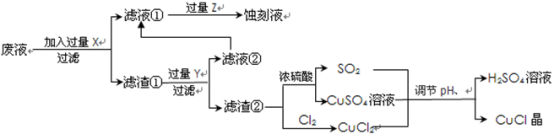 根据以上信息回答下列问题:
根据以上信息回答下列问题:
(1)该生产过程还可以与氯碱工业、硫酸工业生产相结合,工业生产硫酸的方法是______________ 、氯碱工业的装置是_____________________ 。
(2)写出生产过程中X__________ Y___________ (填化学式)
(3)写出产生CuCl的化学方程式________________________________________________________ 。
(4)生产中为了提高CuCl产品的质量,采用______________ 法快速过滤,析出的CuCl晶体不用水而用无水乙醇洗涤的目的是______________________________ ;生产过程中调节溶液的pH不能过大的原因是______________________________ 。
(5)在CuCl的生成过程中理论上不需要补充SO2气体,其理由是__________________________ 。
(6)在CuCl的生成过程中除环境问题、安全问题外,你认为还应该注意的关键问题是:
_____________________________________ 。
(7)氯化亚铜的定量分析:
①称取样品0.25g(称准至0.0002g)置于预先放入玻璃珠50粒和10ml过量的FeCl3溶液250ml锥形瓶中,不断摇动;玻璃珠的作用是____________________________ 。
②待样品溶解后,加水50ml,邻菲罗啉指示剂2滴;
③立即用0.10 mol·L-1硫酸铈标准溶液滴至绿色出现为终点;同时做空白试验一次。已知:CuCl + FeCl3 =CuCl2 + FeCl2 Fe2+ + Ce4+= Fe3+ + Ce3+
如此再重复二次测得:
④数据处理:计算得CuCl的纯度为____________ 。(平行实验结果相差不能超过0.3%)
|
 根据以上信息回答下列问题:
根据以上信息回答下列问题:(1)该生产过程还可以与氯碱工业、硫酸工业生产相结合,工业生产硫酸的方法是
(2)写出生产过程中X
(3)写出产生CuCl的化学方程式
(4)生产中为了提高CuCl产品的质量,采用
(5)在CuCl的生成过程中理论上不需要补充SO2气体,其理由是
(6)在CuCl的生成过程中除环境问题、安全问题外,你认为还应该注意的关键问题是:
(7)氯化亚铜的定量分析:
①称取样品0.25g(称准至0.0002g)置于预先放入玻璃珠50粒和10ml过量的FeCl3溶液250ml锥形瓶中,不断摇动;玻璃珠的作用是
②待样品溶解后,加水50ml,邻菲罗啉指示剂2滴;
③立即用0.10 mol·L-1硫酸铈标准溶液滴至绿色出现为终点;同时做空白试验一次。已知:CuCl + FeCl3 =CuCl2 + FeCl2 Fe2+ + Ce4+= Fe3+ + Ce3+
如此再重复二次测得:
| 1 | 2 | 3 | |
| 空白实验消耗硫酸铈标准溶液的体积(ml) | 0.75 | 0.50 | 0.80 |
| 0.25克样品消耗硫酸铈标准溶液的体积(ml) | 24.65 | 24.75 | 24.70 |
④数据处理:计算得CuCl的纯度为
氯化亚铜(CuCl)可用作有机合成的催化剂,CuCl微溶于水,不溶于醇和稀酸,可溶于Cl-浓度较大的溶液(CuCl+Cl- CuCl
CuCl ),在潮湿空气中易水解、易氧化。工业上用黄铜矿(主要成分是CuFeS2,还含有少量的SiO2)制备CuCl的工艺流程如图:
),在潮湿空气中易水解、易氧化。工业上用黄铜矿(主要成分是CuFeS2,还含有少量的SiO2)制备CuCl的工艺流程如图:
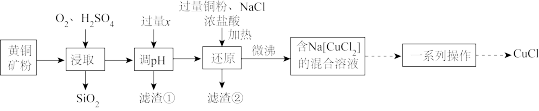
25℃时,相关物质的Ksp见表。
回答下列问题:
(1)黄铜矿预先粉碎的目的是_______ 。
(2)调pH加入的过量x为_______ (填化学式),滤渣①的成分_______ (填化学式)。
(3)“还原”时,铜粉转化为Na[CuCl2]的离子反应方程式为_______ 。
(4)已知:温度、pH对CuCl产率的影响如图1、图2所示。则析出CuCl晶体的最佳条件为_______ 。
A.温度在60℃左右pH为2.0~2.5 B.温度在90℃左右pH为2.0~2.5
C.温度在60℃左右pH为5.0~6.0 D.温度在90℃左右pH为5.0~6.0
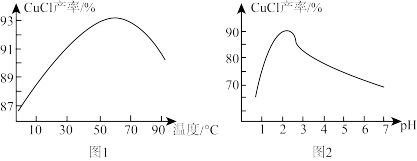
(5)析出的氯化亚铜晶体要立即用无水乙醇洗涤,“醇洗”可快速除去滤渣表面的水,防止滤渣被空气氧化为碱式氯化铜[Cu2(OH)3Cl]。写出氯化亚铜被氧化为碱式氯化铜的化学反应方程式_______ 。
(6)粗产品中氯化亚铜含量的测定:
①称取样品3.0 g于锥形瓶中,再加入过量的FeCl3溶液充分溶解,配制250 mL溶液。②从中取出25.00mL溶液,用0.1000 mol·L-1硫酸铈[Ce(SO4)2]标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2 Fe2++Ce4+=Fe3++Ce3+。
三次平行实验,到达滴定终点时,消耗硫酸铈标准溶液的体积分别为26.05 mL、24.05 mL、23.95 mL。则样品中CuCl的纯度为_______ (结果保留三位有效数字)。

25℃时,相关物质的Ksp见表。
| 物质 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | CuCl |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-19.7 | 1×10-5.9 |
(1)黄铜矿预先粉碎的目的是
(2)调pH加入的过量x为
(3)“还原”时,铜粉转化为Na[CuCl2]的离子反应方程式为
(4)已知:温度、pH对CuCl产率的影响如图1、图2所示。则析出CuCl晶体的最佳条件为
A.温度在60℃左右pH为2.0~2.5 B.温度在90℃左右pH为2.0~2.5
C.温度在60℃左右pH为5.0~6.0 D.温度在90℃左右pH为5.0~6.0
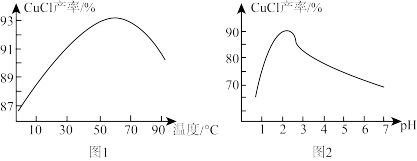
(5)析出的氯化亚铜晶体要立即用无水乙醇洗涤,“醇洗”可快速除去滤渣表面的水,防止滤渣被空气氧化为碱式氯化铜[Cu2(OH)3Cl]。写出氯化亚铜被氧化为碱式氯化铜的化学反应方程式
(6)粗产品中氯化亚铜含量的测定:
①称取样品3.0 g于锥形瓶中,再加入过量的FeCl3溶液充分溶解,配制250 mL溶液。②从中取出25.00mL溶液,用0.1000 mol·L-1硫酸铈[Ce(SO4)2]标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2 Fe2++Ce4+=Fe3++Ce3+。
三次平行实验,到达滴定终点时,消耗硫酸铈标准溶液的体积分别为26.05 mL、24.05 mL、23.95 mL。则样品中CuCl的纯度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


