填空题 适中0.65 引用1 组卷502
反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
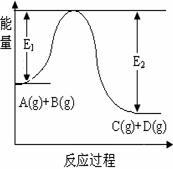
(1)该反应是__________ 反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率________ (填“增大”“减小”“不变”)。
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_______ ,E2_______ (填“增大”“减小”“不变”)。
(4)已知下列热化学方程式:
①H2(g)+1/2O2(g)=H2O(l);ΔH=-285 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g);ΔH=-241.8 kJ·mol-1
③C(s)+1/2O2(g)=CO(g);ΔH=-110.5 kJ·mol-1
④ C(s)+O2(g)=CO2(g);ΔH=-393.5 kJ·mol-1
回答下列问题:
① 燃烧1gH2生成液态水,放出的热量为__________________ 。
②写出CO燃烧热的热化学方程式___________________________________________ 。
 C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是
(2)当反应达到平衡时,升高温度,A的转化率
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
(4)已知下列热化学方程式:
①H2(g)+1/2O2(g)=H2O(l);ΔH=-285 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g);ΔH=-241.8 kJ·mol-1
③C(s)+1/2O2(g)=CO(g);ΔH=-110.5 kJ·mol-1
④ C(s)+O2(g)=CO2(g);ΔH=-393.5 kJ·mol-1
回答下列问题:
① 燃烧1gH2生成液态水,放出的热量为
②写出CO燃烧热的热化学方程式
11-12高二上·江西赣州·阶段练习
类题推荐
(1)已知CH3OH(l)的燃烧热△H=-238.6 kJ/mol,CH3OH(l)+ O2(g)=CO2(g)+2H2O(g) △H=-a kJ/mol,则a
O2(g)=CO2(g)+2H2O(g) △H=-a kJ/mol,则a__ 238.6(填“>”“<”或“=”)。
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:__ 。
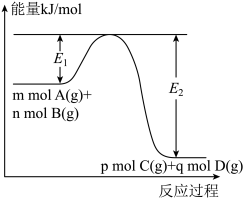
(3)mA(g)+nB(g) pC(g)+qD(g)在反应过程中的能量变化如图所示,回答下列问题。
pC(g)+qD(g)在反应过程中的能量变化如图所示,回答下列问题。

该反应△H=_____ (用E1、E2表示)kJ•mol-1;在反应体系中加入催化剂,E1将____ (填“增大”“减小”或“不变”,下同),△H将______ 。
(4)已知CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数K随温度的变化如表:
H2(g)+CO2(g)的平衡常数K随温度的变化如表:
回答下列问题:
①该反应的△H_____ 0(填“>”“<”或“=”)。
②已知在一定温度下,C(s)+CO2(g) 2CO(g)的平衡常数为K1,C(s)+H2O(g)
2CO(g)的平衡常数为K1,C(s)+H2O(g) CO(g)+H2(g)的平衡常数为K2,则K、K1、K2之间的关系是
CO(g)+H2(g)的平衡常数为K2,则K、K1、K2之间的关系是___ 。
③500℃时,若起始时c(CO)=2 mol•L-1,c(H2O)=2 mol•L-1,则平衡时CO的转化率为____ 。
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
(3)mA(g)+nB(g)
 pC(g)+qD(g)在反应过程中的能量变化如图所示,回答下列问题。
pC(g)+qD(g)在反应过程中的能量变化如图所示,回答下列问题。
该反应△H=
(4)已知CO(g)+H2O(g)
 H2(g)+CO2(g)的平衡常数K随温度的变化如表:
H2(g)+CO2(g)的平衡常数K随温度的变化如表:| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
①该反应的△H
②已知在一定温度下,C(s)+CO2(g)
 2CO(g)的平衡常数为K1,C(s)+H2O(g)
2CO(g)的平衡常数为K1,C(s)+H2O(g) CO(g)+H2(g)的平衡常数为K2,则K、K1、K2之间的关系是
CO(g)+H2(g)的平衡常数为K2,则K、K1、K2之间的关系是③500℃时,若起始时c(CO)=2 mol•L-1,c(H2O)=2 mol•L-1,则平衡时CO的转化率为
(1)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,CH3OH(l)+3/2O2(g)===CO2(g)+2H2O(g)ΔH=-a kJ/mol,则 a___ 238.6(填“>”、“<”或“=”)。
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:_________________________________ 。
(3)反应mA(g)+nB(g) pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。
pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。

该反应△H =____ (用含E1、E2式子表示);在反应体系中加入催化剂,E1___ ,E2___ ,(填增大、减小、不变)。
(4)已知:CO (g) +H2O (g) H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
回答下列问题:
①该反应的ΔH=__________ 填“>”、“=”或“<”)。
②已知在一定温度下,C(s) +CO2 (g) 2CO(g)平衡常数K1;C (s) +H2O (g)
2CO(g)平衡常数K1;C (s) +H2O (g) CO(g) +H2 (g)平衡常数K2。则K、K1 、K2之间的关系是
CO(g) +H2 (g)平衡常数K2。则K、K1 、K2之间的关系是__________________________ 。
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
(3)反应mA(g)+nB(g)
 pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。
pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。 
该反应△H =
(4)已知:CO (g) +H2O (g)
 H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
①该反应的ΔH=
②已知在一定温度下,C(s) +CO2 (g)
 2CO(g)平衡常数K1;C (s) +H2O (g)
2CO(g)平衡常数K1;C (s) +H2O (g) CO(g) +H2 (g)平衡常数K2。则K、K1 、K2之间的关系是
CO(g) +H2 (g)平衡常数K2。则K、K1 、K2之间的关系是组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网