单选题 较难0.4 引用10 组卷911
宝鸡被誉为“青铜器之乡”,出土了大盂鼎、毛公鼎、散氏盘等五万余件青铜器。研究青铜器(含Cu、Sn等)在潮湿环境中发生的腐蚀对于文物保护和修复有重要意义。下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图,下列说法不正确的是
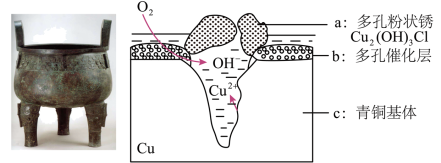

| A.青铜器发生电化学腐蚀,图中c作负极 |
| B.潮湿环境中Cl-浓度大有利于多孔粉状锈的生成 |
| C.若生成0.2 mol Cu2(OH)3Cl,则消耗的O2体积为4.48L |
| D.环境中的Cl−与正、负两极反应的产物作用生成a的离子方程式为2Cu2++3OH−+Cl−===Cu2 (OH)3Cl↓ |
18-19高二上·福建·期末
类题推荐
我国历史悠久,有灿烂的青铜文明,出土大量的青铜器。研究青铜器中(含Cu、Sn等)在潮湿环境中发生的腐蚀对于文物保护和修复有重要意义。下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。下列说法不正确的是


| A.青铜器发生电化学腐蚀,图中c作负极,被氧化 |
| B.正极发生的电极反应为O2+4e-+2H2O=4OH- |
| C.环境中的C1-与正、负两极反应的产物作用生成a的离子方程式为2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓ |
| D.若生成2 mol Cu2(OH)3Cl, 则理论上消耗标准状况下O2的体积为22.4 L |
研究青铜器在潮湿环境中发生的腐蚀对于文物保护和修复有重要意义。如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图,下列说法不正确的是
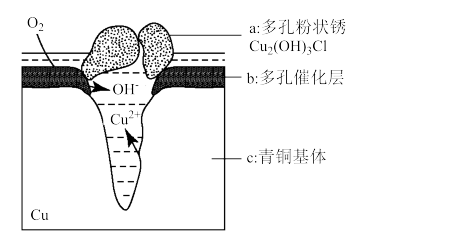

| A.青铜器发生电化学腐蚀,图中c被氧化 |
| B.正极反应式为 |
| C.环境中的Cl-与正、负极反应的产物作用生成Cu2(OH)3Cl的离子方程式为 |
| D.若生成0.2 mol Cu2(OH)3Cl,则理论上消耗O2的质量为3.2 g |
如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。下列说法不正确的是( )
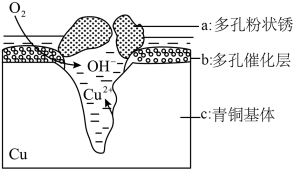

| A.腐蚀过程中,负极是c |
| B.正极反应是O2 + 4e-+2H2O=4OH- |
| C.若生成4.29gCu2(OH)3Cl,则理论上耗氧体积为0.224L (相对原子质量Cu 64,Cl35.5) |
| D.环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓ |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


