解答题-实验探究题 适中0.65 引用1 组卷96
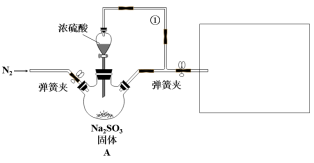
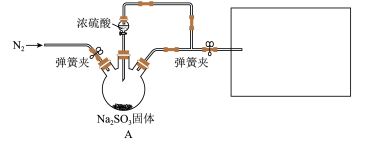
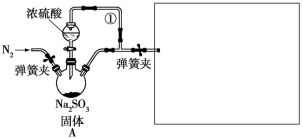
某同学设计了如图装置用于制取SO2和验证SO2的漂白性、水溶液的酸性、还原性。
试回答下列问题:
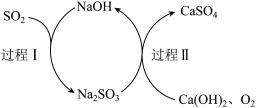
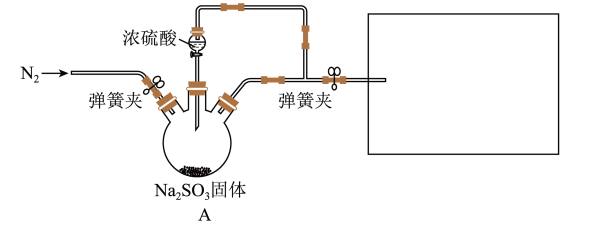
(1)装置A中发生反应的化学方程式为______________ 。
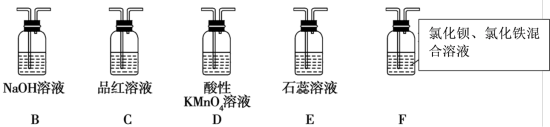
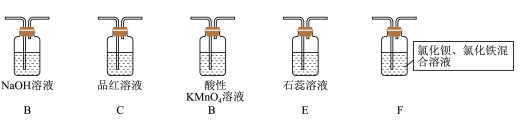
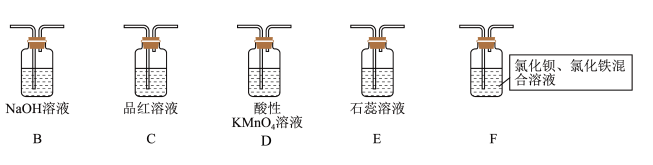
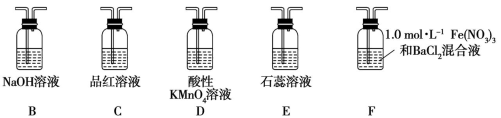
(2)在框图内选择合适装置(从B~E中选择)依次验证SO2的漂白性、水溶液的酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→_______ (填装置的字母编号)。
(3)装置D中发生反应的离子方程式是______________ 。
(4)实验前须鼓入N2,目的是____________ ,简述此操作的必要性:____ 。
(5)已知:1.0 mol·L-1的Fe(NO3)3溶液的pH=1,若将SO2气体通入装置F,装置F中产生了白色沉淀,其成分是______________ (填化学式),分析F中产生白色沉淀的可能原因及观察到的其他现象:______ 。
(6)实验中发现Na2SO3可能部分被氧化,现需测定Na2SO3的纯度:称取10.00 g产品,配成100 mL溶液,移取25.00 mL溶液,用0.200 0 mol·L-1酸性KMnO4溶液进行滴定,消耗KMnO4溶液20.00 mL,其中KMnO4→Mn2+。产品中Na2SO3的质量分数为_______ 。
试回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)在框图内选择合适装置(从B~E中选择)依次验证SO2的漂白性、水溶液的酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→
(3)装置D中发生反应的离子方程式是
(4)实验前须鼓入N2,目的是
(5)已知:1.0 mol·L-1的Fe(NO3)3溶液的pH=1,若将SO2气体通入装置F,装置F中产生了白色沉淀,其成分是
(6)实验中发现Na2SO3可能部分被氧化,现需测定Na2SO3的纯度:称取10.00 g产品,配成100 mL溶液,移取25.00 mL溶液,用0.200 0 mol·L-1酸性KMnO4溶液进行滴定,消耗KMnO4溶液20.00 mL,其中KMnO4→Mn2+。产品中Na2SO3的质量分数为
2019高三上·全国·专题练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网