解答题-原理综合题 适中0.65 引用1 组卷38
目前,人们对环境保护、新能源的开发很重视。
Ⅰ.(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体:
4CO(g)+2NO2(g) 4CO2(g)+N2(g)。恒温恒容条件下,能够说明该反应已达到平衡状态的是
4CO2(g)+N2(g)。恒温恒容条件下,能够说明该反应已达到平衡状态的是____ (填序号);
A.容器内混合气体颜色不再变化 B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2) D.容器内混合气体平均密度保持不变
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s)ΔH=-l59.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5 kJ·mol-1
③H2O(l)=H2O(g)ΔH=+44.0 kJ· mol-1,
写出CO2与NH3合成尿素和液态水的热化学反应方程式_____________________ 。
(3)在饱和的KHCO3电解液中,电解活化CO2制备乙醇的原理如图所示。
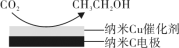
①阴极的电极反应式是___________________________ 。
②从电解后溶液中分离出乙醇的操作方法是____________ (选填字母)。
a.分液 b.过滤 c.蒸馏 d.升华
Ⅱ.工业上利用吸热反应C(s)+2H2O(g) CO2(g)+2H2(g),可制备氢气,氢能源是一种安全高效的新能源。一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器发生反应,其相关数据如表所示:
CO2(g)+2H2(g),可制备氢气,氢能源是一种安全高效的新能源。一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器发生反应,其相关数据如表所示:
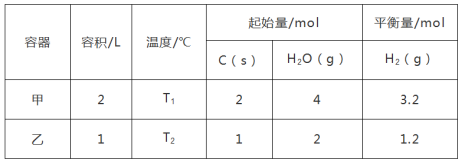
T1℃时,该反应的平衡常数K=_______ ;T1_______ T2(填“>”、“=”或“<”)。
Ⅲ.利用H2和CO2在一定条件下可以合成乙烯:6H2(g)+2CO2(g)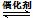 CH2=CH2(g)+4H2O(g),已知不同温度对CO2的平衡转化率及催化剂的催化效率影响如图所示,
CH2=CH2(g)+4H2O(g),已知不同温度对CO2的平衡转化率及催化剂的催化效率影响如图所示,
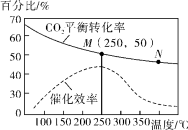
下列有关说法不正确的是________ (填序号)。
①不同条件下反应,N点的速率最大
②M点时平衡常数比N点时平衡常数大
③实际反应应尽可能在较低的温度下进行,以提高CO2的平衡转化率
④温度低于250℃时,随温度升高乙烯的产率减小
Ⅰ.(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体:
4CO(g)+2NO2(g)
 4CO2(g)+N2(g)。恒温恒容条件下,能够说明该反应已达到平衡状态的是
4CO2(g)+N2(g)。恒温恒容条件下,能够说明该反应已达到平衡状态的是A.容器内混合气体颜色不再变化 B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2) D.容器内混合气体平均密度保持不变
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s)ΔH=-l59.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5 kJ·mol-1
③H2O(l)=H2O(g)ΔH=+44.0 kJ· mol-1,
写出CO2与NH3合成尿素和液态水的热化学反应方程式
(3)在饱和的KHCO3电解液中,电解活化CO2制备乙醇的原理如图所示。

①阴极的电极反应式是
②从电解后溶液中分离出乙醇的操作方法是
a.分液 b.过滤 c.蒸馏 d.升华
Ⅱ.工业上利用吸热反应C(s)+2H2O(g)
 CO2(g)+2H2(g),可制备氢气,氢能源是一种安全高效的新能源。一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器发生反应,其相关数据如表所示:
CO2(g)+2H2(g),可制备氢气,氢能源是一种安全高效的新能源。一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器发生反应,其相关数据如表所示:
T1℃时,该反应的平衡常数K=
Ⅲ.利用H2和CO2在一定条件下可以合成乙烯:6H2(g)+2CO2(g)
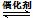 CH2=CH2(g)+4H2O(g),已知不同温度对CO2的平衡转化率及催化剂的催化效率影响如图所示,
CH2=CH2(g)+4H2O(g),已知不同温度对CO2的平衡转化率及催化剂的催化效率影响如图所示,
下列有关说法不正确的是
①不同条件下反应,N点的速率最大
②M点时平衡常数比N点时平衡常数大
③实际反应应尽可能在较低的温度下进行,以提高CO2的平衡转化率
④温度低于250℃时,随温度升高乙烯的产率减小
18-19高三上·湖北荆门·阶段练习
类题推荐
目前,人们对环境保护、新能源开发很重视。
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体:4CO(g)+2NO2(g)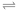 4CO2(g)+N2(g),恒温恒容条件下,能够说明该反应已达到平衡状态的是
4CO2(g)+N2(g),恒温恒容条件下,能够说明该反应已达到平衡状态的是________ (填序号);
A.容器内混合气体颜色不再变化 B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2) D.容器内混合气体密度保持不变
(2)用活性炭还原法也可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)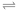 N2(g)+CO2(g) ΔH。在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g) ΔH。在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
①根据图表数据分析T1℃时,该反应在0~20 min的平均反应速率v(CO2)=________ ;计算该反应的平衡常数K=______ 。
②根据上表数据判断,由30 min到40 min时改变的条件可能是(任写一种)__________________ 。
③30 min后升高温度至T2℃,达到新平衡时,容器中NO、N2、CO2的浓度之比为5∶3∶3,此时NO的转化率_______ (填“升高”或“降低”),ΔH_____ 0(填“>”或“<”)。
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-l59.5 kJ· mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5 kJ· mol-1
③H2O(l)=H2O(g) ΔH=+44.0 kJ· mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式_____________________ 。
(4)科学家利用原电池原理,在酸性介质中将NO2转化为HNO3,则该转化的负极反应式为:_________________________________ 。
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体:4CO(g)+2NO2(g)
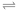 4CO2(g)+N2(g),恒温恒容条件下,能够说明该反应已达到平衡状态的是
4CO2(g)+N2(g),恒温恒容条件下,能够说明该反应已达到平衡状态的是A.容器内混合气体颜色不再变化 B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2) D.容器内混合气体密度保持不变
(2)用活性炭还原法也可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)
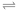 N2(g)+CO2(g) ΔH。在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g) ΔH。在T1℃时,反应进行到不同时间测得各物质的量浓度如下:| 时间/min 浓度/( mol·L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
②根据上表数据判断,由30 min到40 min时改变的条件可能是(任写一种)
③30 min后升高温度至T2℃,达到新平衡时,容器中NO、N2、CO2的浓度之比为5∶3∶3,此时NO的转化率
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-l59.5 kJ· mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5 kJ· mol-1
③H2O(l)=H2O(g) ΔH=+44.0 kJ· mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式
(4)科学家利用原电池原理,在酸性介质中将NO2转化为HNO3,则该转化的负极反应式为:
目前,人们对环境保护、新能源开发很重视。
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,能使有毒气体转化为无毒气体:4CO(g)+2N02(g) C02(g)+N2(g),恒温恒容条件下,能够说明该反应已达到平衡状态的是
C02(g)+N2(g),恒温恒容条件下,能够说明该反应已达到平衡状态的是_____ 填字母);
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C. 2v逆(NO2)=v正(N2)
D.容器内混合气体密度保持不变
(2)用活性炭还原法也可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g) N2(g)+CO2(g)△H。在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g)△H。在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
①根据图表数据分析Tl℃时,该反应在0~20 min的平均反应速率v(C02)=___ ;计算该反应的平衡常数K=____ 。(保留两位有效数字)
②根据上表数据判断,由30 min到40 min时改变的条件可能是(任写一种)_____ 。
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=-l59.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H=+116.5kJ/mol
③H2O(l)=H2O(g)△H=+44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式____ 。
(4)科学家利用原电池原理,在酸性溶液中将N02转化为HN03,则该转化的负极电极方程式为____ 。
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,能使有毒气体转化为无毒气体:4CO(g)+2N02(g)
 C02(g)+N2(g),恒温恒容条件下,能够说明该反应已达到平衡状态的是
C02(g)+N2(g),恒温恒容条件下,能够说明该反应已达到平衡状态的是A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C. 2v逆(NO2)=v正(N2)
D.容器内混合气体密度保持不变
(2)用活性炭还原法也可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)
 N2(g)+CO2(g)△H。在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g)△H。在T1℃时,反应进行到不同时间测得各物质的量浓度如下:| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
| 浓度/mol·L-1 | ||||||
| NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①根据图表数据分析Tl℃时,该反应在0~20 min的平均反应速率v(C02)=
②根据上表数据判断,由30 min到40 min时改变的条件可能是(任写一种)
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=-l59.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H=+116.5kJ/mol
③H2O(l)=H2O(g)△H=+44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式
(4)科学家利用原电池原理,在酸性溶液中将N02转化为HN03,则该转化的负极电极方程式为
目前,人们对环境保护、新能源开发很重视。
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体:4CO(g)+2NO2(g) 4CO2(g)+N2(g)。恒温恒容条件下,能够说明该反应已达到平衡状态的是
4CO2(g)+N2(g)。恒温恒容条件下,能够说明该反应已达到平衡状态的是________  填字母代号
填字母代号 。
。
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.2V逆(NO2)=V正(N2)
D.容器内混合气体密度保持不变
(2)用活性炭还原法也可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g) N2(g)+CO2(g)△H时,反应进行到不同时间测得各物质的量浓度如下表所示:
N2(g)+CO2(g)△H时,反应进行到不同时间测得各物质的量浓度如下表所示:
①根据表中数据分析T1℃时,该反应在0~20min的平均反应速率v(CO2)________ ;计算该反应的平衡常数
________ 。
②根据上表数据判断,由30min到40min时改变的条件可能是________  任写一种
任写一种 。
。
③若30min后升高温度至T2℃,达到新平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,此时NO的转化率________  填“升高”或“降低”
填“升高”或“降低” ,△H
,△H________  填“
填“ ”或“
”或“ ”
” 。(3)以
。(3)以 与
与 为原料可合成化肥尿素化学式为
为原料可合成化肥尿素化学式为 。已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=-159.5kJ/mol②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H=+116.5kJ/mol,③H2O(l)=H2O(g)△H=+44.0kJ/mol,写出CO2与NH3合成尿素和液态水的热化学方程式
。已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=-159.5kJ/mol②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H=+116.5kJ/mol,③H2O(l)=H2O(g)△H=+44.0kJ/mol,写出CO2与NH3合成尿素和液态水的热化学方程式_____
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体:4CO(g)+2NO2(g)
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.2V逆(NO2)=V正(N2)
D.容器内混合气体密度保持不变
(2)用活性炭还原法也可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)
| 浓度/(mol 时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
②根据上表数据判断,由30min到40min时改变的条件可能是
③若30min后升高温度至T2℃,达到新平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,此时NO的转化率
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


