解答题-结构与性质 适中0.65 引用4 组卷496
N、Cu及其相关化合物用途非常广泛。回答下列问题:
(1)基态铜原子的价电子排布式为__________________ 。
(2)铜与钾处于同周期且最外层电子数相同,铜的熔沸点及硬度均比钾大,其原因是___________________________ 。
(3)NH3分子的立体构型为_________ ,中心原子的杂化类型是_________ 。
(4)N、S、P是组成蛋白质的常见元素。三种元素中第一电离能最大的是_________ ,电负性最小的是_________ 。(填元素符号)
(5)已知:Cu2O熔点为1235℃,CuCl熔点为426℃,则可判定Cu2O为_________ (填“离子晶体”或“分子晶体”,下同),CuCl为_________ 。
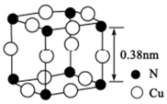
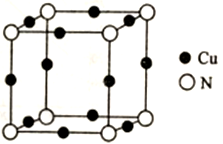
(6)氮与铜形成的一种化合物的晶胞结构如图所示。
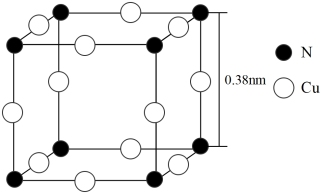
与每个Cu原子紧邻的Cu原子有_________ 个,阿伏伽德罗常数的数值为NA,该晶体的密度为_________ (列出计算式)g·cm-3。
(1)基态铜原子的价电子排布式为
(2)铜与钾处于同周期且最外层电子数相同,铜的熔沸点及硬度均比钾大,其原因是
(3)NH3分子的立体构型为
(4)N、S、P是组成蛋白质的常见元素。三种元素中第一电离能最大的是
(5)已知:Cu2O熔点为1235℃,CuCl熔点为426℃,则可判定Cu2O为
(6)氮与铜形成的一种化合物的晶胞结构如图所示。

与每个Cu原子紧邻的Cu原子有
19-20高三上·重庆·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网