填空题 适中0.65 引用1 组卷165
医学上常用酸性高锰酸钾溶液和草酸溶液的反应用于测定血钙的含量回答下列问题:
(1)配平以下离子方程式,并用单线桥表示电子转移的方向和数目:
______ +_____MnO4-+_____H2C2O4=_____CO2↑+_____Mn2++____。
(2)该反应中的还原剂是______ 。
(3)反应转移了0.4mol电子,则消耗KMnO4的物质的量为______ mol。
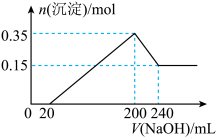
(4)将一定质量的镁、铝合金投入100 mL一定物质的量浓度的HCl中,合金全部溶解,向所得溶液中滴加5 mol·L-1NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液体积关系如下图。
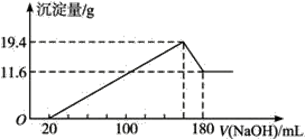
①原合金中铝的质量分数是___________ 。
②盐酸的物质的量浓度是_____________ 。
(1)配平以下离子方程式,并用单线桥表示电子转移的方向和数目:
(2)该反应中的还原剂是
(3)反应转移了0.4mol电子,则消耗KMnO4的物质的量为
(4)将一定质量的镁、铝合金投入100 mL一定物质的量浓度的HCl中,合金全部溶解,向所得溶液中滴加5 mol·L-1NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液体积关系如下图。

①原合金中铝的质量分数是
②盐酸的物质的量浓度是
18-19高一上·内蒙古乌兰察布·阶段练习
类题推荐
电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表
①室温下,一定浓度的HCOONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是_______ 。
②0.1mol·L-1NaCN溶液和0.1mol·L-1NaHCO3溶液中,c(CN-)_______ c(HCO )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。
③常温下,pH相同的三种溶液a、HCOONab、NaCNc、Na2CO3,其物质的量浓度由大到小的顺序是_______ (填编号)。
④将少量CO2通入NaCN溶液,反应的离子方程式是_______ 。
(2)室温下,用0.100mol·L-1盐酸溶液滴定20.00mL0.100mol·L-1的某氨水溶液,滴定曲线如图所示:
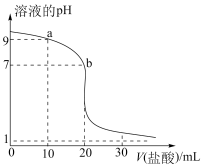
①b点液中离子浓度大小的关系式为_______ 。
②a点所示的溶液中电荷守恒式为_______ 。
(3)已知Ksp(BaCO3)=2.6×10-9,Ksp(BaSO4)=1.1×10-10
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为_______ mol·L-1
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中
_______ (保留三位有效数字)。
(1)已知部分弱酸的电离常数如下表
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离常数(25℃) | Ka=1.77×10-4 | Ka=4.3×10-10 | Ka1=5.0×10-7 Ka2=5.6×10-11 |
①室温下,一定浓度的HCOONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是
②0.1mol·L-1NaCN溶液和0.1mol·L-1NaHCO3溶液中,c(CN-)
③常温下,pH相同的三种溶液a、HCOONab、NaCNc、Na2CO3,其物质的量浓度由大到小的顺序是
④将少量CO2通入NaCN溶液,反应的离子方程式是
(2)室温下,用0.100mol·L-1盐酸溶液滴定20.00mL0.100mol·L-1的某氨水溶液,滴定曲线如图所示:

①b点液中离子浓度大小的关系式为
②a点所示的溶液中电荷守恒式为
(3)已知Ksp(BaCO3)=2.6×10-9,Ksp(BaSO4)=1.1×10-10
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网