单选题 适中0.65 引用1 组卷88
如图装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中正确的是:
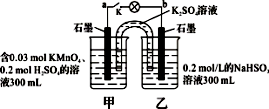

| A.当电路中有0.06 mol电子转移时,乙烧杯中溶液c(H+) 约为0.1 mol · L-1 |
| B.乙池中的还原产物为SO42- |
| C.电池工作时,甲烧杯中溶液的pH逐渐增大 |
| D.电池工作时,盐桥中的K+移向乙烧杯,外电路的电流方向是从b到a |
18-19高二上·浙江台州·阶段练习
类题推荐
根据反应KMnO4+FeSO4+H2SO4-MnSO4+Fe2(SO4)3+K2SO4+H2O(未配平)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。下列说法不正确的是


| A.石墨b是原电池的负极,乙中发生氧化反应 |
| B.电池工作时,盐桥中的K+向甲烧杯中移动 |
| C.甲烧杯中的电极反应式: |
| D.忽略溶液体积变化,Fe2(SO4)3浓度变为1.5 mol/L,则反应中转移的电子为0.1 mol |
根据反应KMnO4+FeSO4+H2SO4→MnSO4+Fe2(SO4)3+K2SO4+H2O(未配平)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
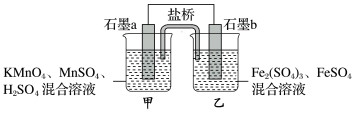

| A.石墨b是原电池的负极,发生氧化反应 |
| B.忽略溶液体积变化,Fe2(SO4)3浓度变为1.5 mol/L,则反应中转移的电子为0.1 mol |
| C.甲烧杯中的电极反应式:MnO4-+5e-+8H+=Mn2++4H2O |
| D.电池工作时,盐桥中的K+向甲烧杯中移动 |
根据反应KMnO4+FeSO4+H2SO4→MnSO4+Fe2(SO4)3+K2SO4+H2O(未配平)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
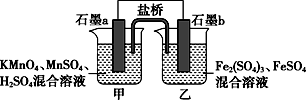

| A.石墨b是原电池的负极,发生氧化反应 |
| B.甲烧杯中的电极反应式:MnO4-+5e-+8H+===Mn2++4H2O |
| C.电池工作时,盐桥中的阴阳离子分别向乙甲烧杯中移动,保持溶液中的电荷平衡 |
| D.忽略溶液体积变化,Fe2(SO4)3浓度变为1.5 mol/L,则反应中转移的电子为0.1 mol |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


