解答题-原理综合题 较难0.4 引用1 组卷83
煤是一种重要的化工原料,人们将利用煤制取的水煤气、焦炭、甲醚等广泛用于工农业生产中。
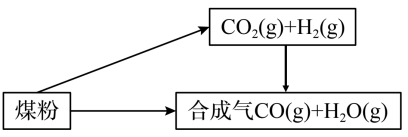
(1)已知: ①


 +131.3kJ·mol-1
+131.3kJ·mol-1
②


 +41.3kJ·mol-1
+41.3kJ·mol-1
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为______ ,该反应在________ (填“高温”、“低温”或“任何温度”)下有利于正向自发进行。
(2)有人利用炭还原法处理氮氧化物,发生反应
 N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和
N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和 ,在
,在 ℃时,不同时间测得各物质的浓度如下表所示:
℃时,不同时间测得各物质的浓度如下表所示:
①10~20 内,N2的平均反应速率
内,N2的平均反应速率
________________ ;
②30 后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是
后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是_________ (填字母序号)。
A.通入一定量的 B.加入一定量的活性炭
B.加入一定量的活性炭
C.加入合适的催化剂 D.适当缩小容器的体积
(3)研究表明:反应

 平衡常数随温度的变化如下表所示:
平衡常数随温度的变化如下表所示:
若反应在500℃时进行,设起始时 和
和 的浓度均为0.020
的浓度均为0.020 ,在该条件下达到平衡时,
,在该条件下达到平衡时,  的转化率为
的转化率为__________ 。
(4)用 做燃料电池电解
做燃料电池电解 溶液、
溶液、 和
和 混合液的示意图如图1所示,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时
混合液的示意图如图1所示,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时 、
、 两极上产生的气体体积相同。
两极上产生的气体体积相同。

a.图1中A极产生的气体在标准状况下的体积为__________ ;
b.电极为 、
、 的装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2所示,则图中③线表示的是
的装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2所示,则图中③线表示的是__________ (填离子符号)的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要__________  5.0
5.0
 溶液。
溶液。
c.乙炔(CH≡CH)是重要的化工原料,广泛应用于焊割、燃料电池及有机合成等。乙炔-空气燃料电池是一种碱性(20%-30%的KOH溶液)燃料电池。电池放电时,负极的电极反应式为__________ 。

(1)已知: ①

②

则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为
(2)有人利用炭还原法处理氮氧化物,发生反应
 N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和
N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和
①10~20
②30
A.通入一定量的
C.加入合适的催化剂 D.适当缩小容器的体积
(3)研究表明:反应
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(4)用

a.图1中A极产生的气体在标准状况下的体积为
b.电极为
c.乙炔(CH≡CH)是重要的化工原料,广泛应用于焊割、燃料电池及有机合成等。乙炔-空气燃料电池是一种碱性(20%-30%的KOH溶液)燃料电池。电池放电时,负极的电极反应式为
2018·安徽阜阳·三模
类题推荐
(1)煤是一种重要的化工原料,人们将利用煤制取的水煤气、焦炭、甲醚等广泛用于工农业生产中。(1)已知:①C(s)+H2O(g)═CO(g)+H2(g) △H=+131.3kJ·mol-1
②CO2(g)+H2(g)═CO(g)+H2O(g) △H=+41.3kJ·mol-1
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为____________ 。该反应在____________ (填“高温”、“低温”或“任何温度”)下有利于正向自发进行。
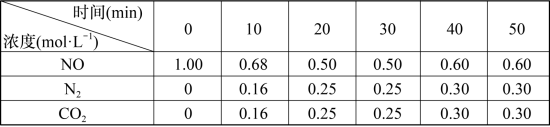
(2)有人利用炭还原法处理氮氧化物,发生反应C(s)+2NO(g) N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:
N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:
①10~20min内,N2的平均反应速率v(N2)=____________ 。
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是_________ 填字母序号)。
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.适当缩小容器的体积
(3)研究表明:反应CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
若反应在500℃时进行,设起始时CO和H2O的浓度均为0.020mol·L-1,在该条件下达到平衡时,CO的转化率为____________ 。
②CO2(g)+H2(g)═CO(g)+H2O(g) △H=+41.3kJ·mol-1
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为
(2)有人利用炭还原法处理氮氧化物,发生反应C(s)+2NO(g)
 N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:
N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:| 时间(min) 浓度(mol·L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①10~20min内,N2的平均反应速率v(N2)=
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.适当缩小容器的体积
(3)研究表明:反应CO(g)+H2O(g)
 H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
H2(g)+CO2(g)平衡常数随温度的变化如下表所示:| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
若反应在500℃时进行,设起始时CO和H2O的浓度均为0.020mol·L-1,在该条件下达到平衡时,CO的转化率为
煤和煤制品(如水煤气、焦炭、甲醚等)已广泛应用于工农业生产中。
(1)已知:C(s)+H2O(g)=CO(g)+H2(g) △H=+131.3 kJ·mol-l
CO2(g)+H2(g)=CO(g)+H2O(g) △H=+41.3kJ·mol-l
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为_______ ,该反应在_______ (填“高温”、“低温”或“任何温度”)下有利于正向自发进行。
(2)利用炭还原法可处理氮氧化物(如NO等),发生的反应为C(s)+2NO(g)⇌N2 (g)+ CO2 (g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得的各气体的浓度如下表所示:
①10~20 min内,N2的平均反应速率可v(N2)=_______ 。
②30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是____ (填字母)。
A.通入一定量的NO B.加入一定量的活性炭 C.加入合适的催化剂 D.适当缩小容器的体积
(3)研究表明,反应CO(g)+H2O(g)⇌H2(g)+CO2(g)的平衡常数随温度的变化如下表所示:
若反应在500℃时进行,设起始时CO和H2O的浓度均为0.020 mol·L-l,在该条件下达到平衡时,CO的转化率为_______ 。
(1)已知:C(s)+H2O(g)=CO(g)+H2(g) △H=+131.3 kJ·mol-l
CO2(g)+H2(g)=CO(g)+H2O(g) △H=+41.3kJ·mol-l
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为
(2)利用炭还原法可处理氮氧化物(如NO等),发生的反应为C(s)+2NO(g)⇌N2 (g)+ CO2 (g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得的各气体的浓度如下表所示:
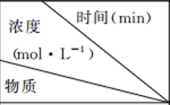 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
②30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是
A.通入一定量的NO B.加入一定量的活性炭 C.加入合适的催化剂 D.适当缩小容器的体积
(3)研究表明,反应CO(g)+H2O(g)⇌H2(g)+CO2(g)的平衡常数随温度的变化如下表所示:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
目前,人们对环境保护、新能源开发非常重视。
(1)已知:①CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g) ΔH1=860.0kJ•mol-1
②2NO2(g)⇌N2O4(g) ΔH2=66.9kJ•mol-1
写出 CH4催化还原 N2O4(g)生成 N2、H2O(g)和 CO2的热化学方程式_______
(2)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应:C(s)+2NO(g)⇌N2(g)+CO2(g) ΔH,在t1℃时,反应进行到不同时间测得各物质的物质的量浓度如表:
① 据表中数据分析,t1℃时,该反应在0~20min 的平均反应速率 v(NO)=_______ ,该反应的平衡常数K=_______ 。(常数结果保留 2位小数)
②30min时,只改变某一条件,根据上表中的数据判断改变的条件可能是_______ (填字母代号)。
A.适当缩小容器的体积 B.加入合适的催化剂 C.加入一定量的活性炭 D.通入一定量的NO
③若30min后升高温度至t2℃,达到平衡时,容器中NO、N2、CO 的浓度之比为5∶3∶3,则达到新平衡时NO 的转化率_______ (填“升高”或“降低”);ΔH_______ 0(填“>”或“<”)。
(3)以甲烷为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
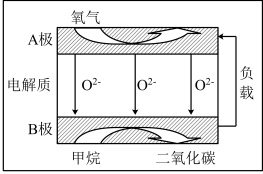
B极上的电极反应式为_______ ;若用该燃料电池做电源,用石墨做电极电解100mL1mol/L的硫酸铜溶液,当两极收集到的气体体积相等时,理论上消耗的甲烷的体积为_______ (标况下)。
(1)已知:①CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g) ΔH1=860.0kJ•mol-1
②2NO2(g)⇌N2O4(g) ΔH2=66.9kJ•mol-1
写出 CH4催化还原 N2O4(g)生成 N2、H2O(g)和 CO2的热化学方程式
(2)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应:C(s)+2NO(g)⇌N2(g)+CO2(g) ΔH,在t1℃时,反应进行到不同时间测得各物质的物质的量浓度如表:
① 据表中数据分析,t1℃时,该反应在0~20min 的平均反应速率 v(NO)=
 | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.3 | 0.3 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.3 | 0.3 | 0.36 | 0.36 |
②30min时,只改变某一条件,根据上表中的数据判断改变的条件可能是
A.适当缩小容器的体积 B.加入合适的催化剂 C.加入一定量的活性炭 D.通入一定量的NO
③若30min后升高温度至t2℃,达到平衡时,容器中NO、N2、CO 的浓度之比为5∶3∶3,则达到新平衡时NO 的转化率
(3)以甲烷为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:

B极上的电极反应式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


