解答题-实验探究题 困难0.15 引用1 组卷730
从宏观现象探究微观本质是重要的化学学科素养。
I. 以亚硫酸钠(Na2SO3)为实验对象,探究其性质。实验如下:
【资料1】亚硫酸(H2SO3)易分解生成SO2和H2O。
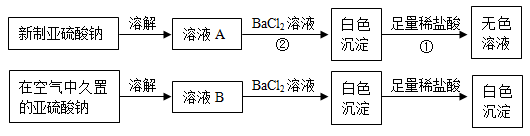
(1)写出上述实验中①、②的离子方程式_________________ ,_________________ 。
(2)通过上述实验可知,在空气中久置的亚硫酸钠固体中会混有_____________ (填化学式),亚硫酸钠在空气中变质体现了亚硫酸钠的_________________ 性。
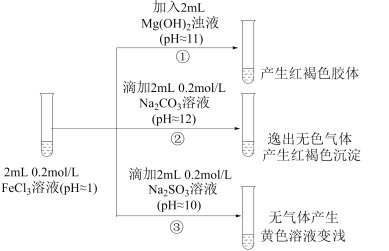
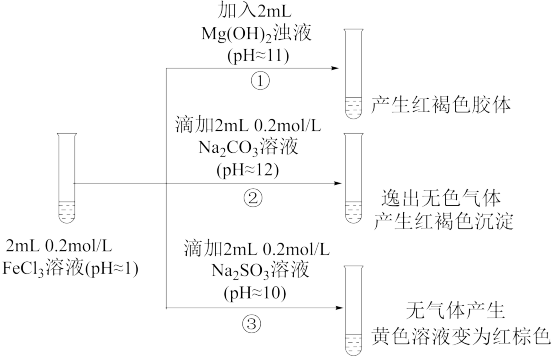
II. 以FeCl3溶液为实验对象,探究其与碱性物质之间反应的复杂多样性。实验如下:
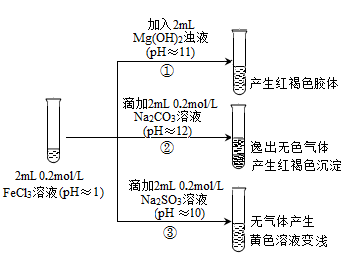
【资料2】含Fe3+的溶液中加入KSCN溶液,溶液由黄色变为红色;
含Fe2+的溶液中加入K3Fe(CN)6溶液,生成蓝色沉淀。
(1)①中反应的离子方程式是_____________________________ 。
(2)②中逸出的无色气体是_______________________________ 。
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加BaCl2溶液,产生白色沉淀。得出结论:FeCl3与Na2SO3发生了氧化还原反应,离子方程式是_______________ 。
乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是_________ 。
(4)由上述实验可知,下列说法正确的是________ (填字母)。
a. 盐与碱反应时,盐和碱都必须可溶于水
b. 盐溶液可能呈中性、碱性、酸性
c. 盐与盐反应时,不一定生成两种新盐
d. 盐与盐反应时,发生的不一定是复分解反应
I. 以亚硫酸钠(Na2SO3)为实验对象,探究其性质。实验如下:
【资料1】亚硫酸(H2SO3)易分解生成SO2和H2O。

(1)写出上述实验中①、②的离子方程式
(2)通过上述实验可知,在空气中久置的亚硫酸钠固体中会混有
II. 以FeCl3溶液为实验对象,探究其与碱性物质之间反应的复杂多样性。实验如下:

【资料2】含Fe3+的溶液中加入KSCN溶液,溶液由黄色变为红色;
含Fe2+的溶液中加入K3Fe(CN)6溶液,生成蓝色沉淀。
(1)①中反应的离子方程式是
(2)②中逸出的无色气体是
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加BaCl2溶液,产生白色沉淀。得出结论:FeCl3与Na2SO3发生了氧化还原反应,离子方程式是
乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是
(4)由上述实验可知,下列说法正确的是
a. 盐与碱反应时,盐和碱都必须可溶于水
b. 盐溶液可能呈中性、碱性、酸性
c. 盐与盐反应时,不一定生成两种新盐
d. 盐与盐反应时,发生的不一定是复分解反应
18-19高一上·北京·期中
类题推荐
从宏观现象探究微观本质是重要的化学学科素养。以FeCl3溶液为实验对象,探究其与碱性物质之间反应的复杂多样性,实验如下:
(1)①中反应的离子方程式是___________ 。
(2)②中逸出的无色气体是___________ ;从物质类别角度分析,Na2CO3与Na2SO3在化学方面的共性是__________ (写一条);从化合价角度分析,Na2CO3与Na2SO3在化学方面的差异是__________ (写一条)。
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
I.甲取③中红棕色溶液少许,滴入盐酸酸化的BaCl2溶液,产生白色沉淀。甲得出结论:FeCl3与Na2SO3发生氧化还原反应,离子方程式是___________ 。
II.乙认为甲的实验不严谨,重新设计并进行实验,证实了甲的结论是正确的。其实验方案是____________ 。
(4)根据实验,FeCl3溶液与碱性物质之间的反应多样性与__________ 有关。
| 2mL0.2mol/LFeCl3溶液(pH=1) | 加入试剂 | 现象 |
| ①2mLMg(OH)2浊液(pH=11) | 产生红褐色胶体 | |
| ②滴加2mL0.2mol/LNa2CO3溶液(pH=12) | 逸出无色气体,产生红褐色沉淀 | |
| ③滴加2mL0.2mol/LNa2SO3溶液(pH=10) | 无色气体产生,黄色溶液变为红棕色 |
(1)①中反应的离子方程式是
(2)②中逸出的无色气体是
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
I.甲取③中红棕色溶液少许,滴入盐酸酸化的BaCl2溶液,产生白色沉淀。甲得出结论:FeCl3与Na2SO3发生氧化还原反应,离子方程式是
II.乙认为甲的实验不严谨,重新设计并进行实验,证实了甲的结论是正确的。其实验方案是
(4)根据实验,FeCl3溶液与碱性物质之间的反应多样性与
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网