填空题 适中0.65 引用2 组卷74
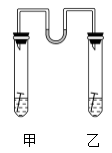
如图所示,甲、乙两试管中各放一枚铁钉,甲试管为NaCl溶液,乙试管为NH4Cl溶液,数天后观察到的现象是______________________________ ,甲中正极反应式为___________________________ ,乙中正极反应式为___________________________ ,试管中残留气体的平均相对分子质量的变化为:甲________ ,乙________ 。

2018高二上·全国·专题练习
类题推荐
化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)理论上讲,任何自发的氧化还原反应都可以设计成原电池。利用反应“ ”设计成一个化学电池,该电池的负极发生
”设计成一个化学电池,该电池的负极发生____ (填“氧化”或“还原”)反应,电解质溶液是_____ 溶液。
(2)为了探究化学反应中的能量变化,某同学设计了相同条件下如图一、图二(铜、锌之间导线连接)的两个实验,有关实验的下列说法正确的是______(填字母)。
(3)某同学利用原电池反应检测金属的活动性顺序,设计了相同条件下如图三( 的
的 溶液)、图四(
溶液)、图四( 的
的 溶液)的两个实验。
溶液)的两个实验。 向
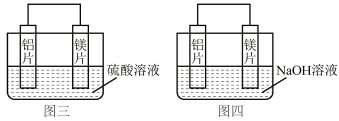
向_____ (填“镁片”或“铝片”)移动;
②图四中铝片为_____ 极,其电极反应式为:_____ 。
③依据该实验得出的下列结论中,正确的有_____ (填字母)。
A.利用原电池反应判断金属活动性强弱不一定准确
B.镁的金属性不一定比铝的金属性强
C.初中所学的金属活动性顺序已过时,没有实用价值
D.电极不变,电解质溶液不同,电极反应也可能不同
(4)一定量的Zn与足量的稀硫酸反应制氢气,反应过程中生成气体的体积随时间的变化如图五中的曲线①。某同学欲通过改变某一条件将其曲线①变成曲线②。下列措施能实现其目的的是_____(填字母)。
(5)为减少汽车尾气的污染,逐步向着新能源汽车发展。肼—空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,工作原理如图六所示。回答下列问题:_____ 。
②电池工作时, 移向
移向______ 电极(填“左侧”或“右侧”);电池工作一段时间后,电解质溶液的pH将____ (填“增大”、“减小”或“不变”)。
(6)白磷在氧气中燃烧的化学方程式可用结构式表示如图七:
根据表中数据计算: (白磷)在氧气中充分反应
(白磷)在氧气中充分反应______ (填“吸收”或“放出”)______  能量。
能量。
(1)理论上讲,任何自发的氧化还原反应都可以设计成原电池。利用反应“
(2)为了探究化学反应中的能量变化,某同学设计了相同条件下如图一、图二(铜、锌之间导线连接)的两个实验,有关实验的下列说法正确的是______(填字母)。
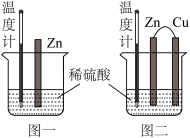
| A.图一和图二中温度计读数均高于室温 | B.温度计读数图一高于图二 |
| C.图一和图二只在锌棒表面产生气泡 | D.产生气体的速率图二快于图一 |
(3)某同学利用原电池反应检测金属的活动性顺序,设计了相同条件下如图三(
②图四中铝片为
③依据该实验得出的下列结论中,正确的有
A.利用原电池反应判断金属活动性强弱不一定准确
B.镁的金属性不一定比铝的金属性强
C.初中所学的金属活动性顺序已过时,没有实用价值
D.电极不变,电解质溶液不同,电极反应也可能不同
(4)一定量的Zn与足量的稀硫酸反应制氢气,反应过程中生成气体的体积随时间的变化如图五中的曲线①。某同学欲通过改变某一条件将其曲线①变成曲线②。下列措施能实现其目的的是_____(填字母)。
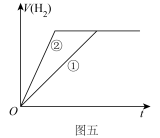
| A.滴加少量的 | B.滴加少量的浓硫酸 |
| C.加入少量的 | D.加入少量的 |
(5)为减少汽车尾气的污染,逐步向着新能源汽车发展。肼—空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,工作原理如图六所示。回答下列问题:

②电池工作时,
(6)白磷在氧气中燃烧的化学方程式可用结构式表示如图七:
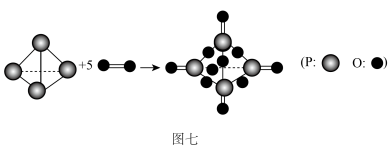
| 化学键 | ||||
| 键能( | 200 | 360 | 500 | 585 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


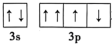 不能表示基态硫原子的价电子轨道表示式,因为违背了
不能表示基态硫原子的价电子轨道表示式,因为违背了

