解答题-原理综合题 适中0.65 引用2 组卷157
甲醇是一种优质燃料,在工业上常用CO和H2合成甲醇,反应方程式为CO(g)+2H2(g)  CH3OH(g)。
CH3OH(g)。
已知:
①CO(g)+1/2O2(g)=CO2(g) △H1=-283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) △H2=-241.8kJ/mol
③CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H3=-192.2kJ/mol
回答下列问题:
(1)计算CO(g)+2H2(g) CH3OH(g)的反应热△H4=
CH3OH(g)的反应热△H4=________________ 。
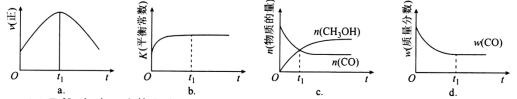
(2)若在绝热、恒容的密闭容器中充入1 mol CO、2 mol H2,发生CO(g)+2H2(g) CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是
CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是________ (填选项字母)。
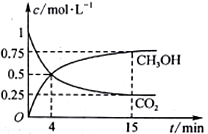
(3)T1℃时,在一个体积为5 L的恒容容器中充入1 mol CO、2 mol H2,经过5 min达到平衡,CO的转化率为0.8,则5 min内用H2表示的反应速率为v(H2)=_______________________ 。T1℃时,在另一体积不变的密闭容器中也充入1 mol CO、2 mol H2,达到平衡时CO的转化率为0.7,则该容器的体积______ 5 L(填“>”“<”或“=”);T1℃时,CO(g)+2H2(g)  CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=____________________________ 。
(4)为了提高燃料的利用率可以将甲醇设计为燃料电池,写出KOH作电解质溶液时,甲醇燃料电池的负极反应式:_________________________ 。该电池负极与水库的铁闸相连时,可以保护铁闸不被腐蚀,这种电化学保护方法叫做___________ 。
(5)含有甲醇的废水随意排放会造成水污染,可用ClO2将其氧化为CO2,然后再加碱中和即可。写出处理甲醇酸性废水过程中,ClO2与甲醇反应的离子方程式:_________ 。
 CH3OH(g)。
CH3OH(g)。已知:
①CO(g)+1/2O2(g)=CO2(g) △H1=-283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) △H2=-241.8kJ/mol
③CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H3=-192.2kJ/mol
回答下列问题:
(1)计算CO(g)+2H2(g)
 CH3OH(g)的反应热△H4=
CH3OH(g)的反应热△H4=(2)若在绝热、恒容的密闭容器中充入1 mol CO、2 mol H2,发生CO(g)+2H2(g)
 CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是
CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是
(3)T1℃时,在一个体积为5 L的恒容容器中充入1 mol CO、2 mol H2,经过5 min达到平衡,CO的转化率为0.8,则5 min内用H2表示的反应速率为v(H2)=
 CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=(4)为了提高燃料的利用率可以将甲醇设计为燃料电池,写出KOH作电解质溶液时,甲醇燃料电池的负极反应式:
(5)含有甲醇的废水随意排放会造成水污染,可用ClO2将其氧化为CO2,然后再加碱中和即可。写出处理甲醇酸性废水过程中,ClO2与甲醇反应的离子方程式:
18-19高三上·福建泉州·期中
类题推荐
运用化学反应原理知识研究如何利用CO、SO2等污染有非常重要的意义。
(1)用CO可以合成甲醇。
已知:CH3OH(g)+ O2(g)=CO2(g)+2H2O(1) ΔH1
O2(g)=CO2(g)+2H2O(1) ΔH1
CO(g)+ O2(g)=CO2(g) ΔH2
O2(g)=CO2(g) ΔH2
H2(g)+ (g)=.H2O(1) ΔH3
(g)=.H2O(1) ΔH3
请写出由CO和H2形成CH3OH的热化学方程式__________ 。
(2)下表所列数据是CO和H2形成CH3OH的反应在不同温度下的化学平衡常数(K),由表中数据判断该反应的ΔH__________ 0(填“>”、“=”或“<”)
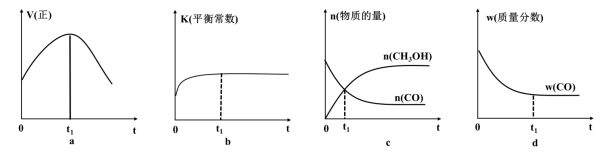
(3)若在绝热、恒容的密闭容器中充入1molCO、2molH2,发生CO(g)+2H2(g) CH3OH(g)反应,下列示意图能说明该反应在进行到t1时刻为平衡状态的是
CH3OH(g)反应,下列示意图能说明该反应在进行到t1时刻为平衡状态的是__________ (填选项字母)。
(4)T1℃时,在一个体积为1L的恒容容器中充入1molCO、3molH2,经过5min达到平衡,CO的转化率为0.8,则5min内用H2表示的反应速率为v(H2)__________ 。此时,这个反应的平衡常数是__________ ,反应温度为__________ ℃。
(5)为了提高燃料的利用率可以将甲醇设计为燃料电池,写出KOH作电解质溶液时,甲醇燃料电池的负极反应式__________ 。
(1)用CO可以合成甲醇。
已知:CH3OH(g)+
CO(g)+
H2(g)+
请写出由CO和H2形成CH3OH的热化学方程式
(2)下表所列数据是CO和H2形成CH3OH的反应在不同温度下的化学平衡常数(K),由表中数据判断该反应的ΔH
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
 CH3OH(g)反应,下列示意图能说明该反应在进行到t1时刻为平衡状态的是
CH3OH(g)反应,下列示意图能说明该反应在进行到t1时刻为平衡状态的是
(4)T1℃时,在一个体积为1L的恒容容器中充入1molCO、3molH2,经过5min达到平衡,CO的转化率为0.8,则5min内用H2表示的反应速率为v(H2)
(5)为了提高燃料的利用率可以将甲醇设计为燃料电池,写出KOH作电解质溶液时,甲醇燃料电池的负极反应式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是______(填选项字母)。
CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是______(填选项字母)。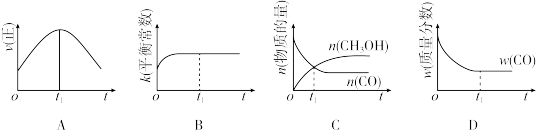
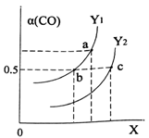
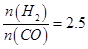 时,达到平衡状态,CH3OH的体积分数可能是图象中的______点。
时,达到平衡状态,CH3OH的体积分数可能是图象中的______点。
 CH3OH(g) ΔH=-116kJ/mol
CH3OH(g) ΔH=-116kJ/mol