填空题 较难0.4 引用1 组卷422
已知:
又已知不同温度下, 、
、 的值如下:
的值如下:
(1)若 时进行反应①,
时进行反应①, 的起始浓度为
的起始浓度为 ,
, 后建立平衡,则
后建立平衡,则 的转化率为
的转化率为__________ ,用 表示的反应速率为
表示的反应速率为__________ 。
(2) 进行反应③,其平衡常数为
进行反应③,其平衡常数为 为
为__________ (求具体数值),焓变
__________ (填“>”“=”或“<”)0,若已知该反应仅在高温时正反应自发,则
__________ (填“>”“=”或“<”)0。
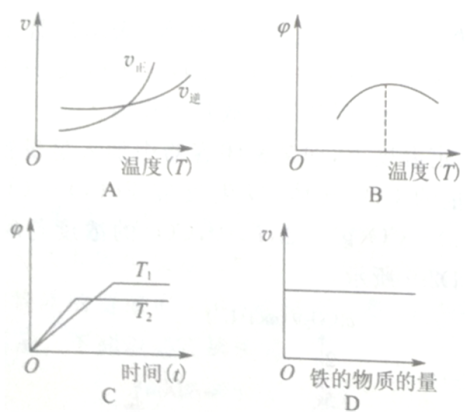
(3)下列图象符合反应②的是__________ (填序号)。(图中v是速率, 为混合物中
为混合物中 的体积分数)
的体积分数)
| ① | ||
| ② | ||
| ③ |
| 温度/℃ | ||
| 500 | ||
| 700 | ||
| 900 |
(2)
(3)下列图象符合反应②的是

17-18高二·全国·单元测试
类题推荐
已知:
Fe(s)+CO2(g) FeO(s)+CO(g) K1 ①
FeO(s)+CO(g) K1 ①
Fe(s)+H2O(g) FeO(s)+H2(g) K2 ②
FeO(s)+H2(g) K2 ②
H2(g)+CO2(g) H2O(g)+CO(g) K3 ③
H2O(g)+CO(g) K3 ③
又已知不同温度下,K1、K2值如下表:
(1)若500 ℃时进行反应①,CO2起始浓度为2 mol•L-1,2分钟后建立平衡,则CO2转化率为________ ,用CO表示的速率为________________ 。
(2)900 ℃进行反应③,其平衡常数K3为____________ (求具体数值),焓变 ΔH_______ 0(填“>”“=”或“<”)。
(3)下列图像符合反应②的是___________ (填序号)(图中v是速率,φ为混合物中H2的体积百分含量)。
A.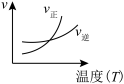 B.
B.  C.
C.  D.
D. 
Fe(s)+CO2(g)
Fe(s)+H2O(g)
H2(g)+CO2(g)
又已知不同温度下,K1、K2值如下表:
温度/℃ | K1 | K2 |
500 | 1.00 | 3.15 |
700 | 1.47 | 2.26 |
900 | 2.40 | 1.60 |
(1)若500 ℃时进行反应①,CO2起始浓度为2 mol•L-1,2分钟后建立平衡,则CO2转化率为
(2)900 ℃进行反应③,其平衡常数K3为
(3)下列图像符合反应②的是
A.
 B.
B.  C.
C.  D.
D. 
在密闭容器中发生:2NO(g)+2CO(g) 2CO2+N2(g)△H=-QkJ/mol,已知:c(CO2)随温度(T)、时间(t)的变化曲线如右图所示,则:
2CO2+N2(g)△H=-QkJ/mol,已知:c(CO2)随温度(T)、时间(t)的变化曲线如右图所示,则:
(1)T1___ T2 ,其理由是_________________
(2)在T2温度下,0~2s内的平均反应速率v(N2)=___
(3)在温度T3下,在两个体积均为1.0L的恒容密闭容器中发生该反应.
①T3时该反应的平衡常数K=___ ,若起始时向容器Ⅰ中充入1.0mol NO,1.5mol CO和2.0molCO2,0.5molN2,则反应向___ (填“正”或“逆”)反应方向进行。
②平衡时两容器中CO的转化率:Ⅰ___ Ⅱ,容器Ⅰ中反应达平衡后,若要进一步提高CO的转化率,可采取的措施为___ (答一条即可)。
 2CO2+N2(g)△H=-QkJ/mol,已知:c(CO2)随温度(T)、时间(t)的变化曲线如右图所示,则:
2CO2+N2(g)△H=-QkJ/mol,已知:c(CO2)随温度(T)、时间(t)的变化曲线如右图所示,则: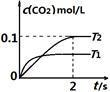
(1)T1
(2)在T2温度下,0~2s内的平均反应速率v(N2)=
(3)在温度T3下,在两个体积均为1.0L的恒容密闭容器中发生该反应.
| 容器编号 | 起始物质的量 | 平衡时物质的量 |
| Ⅰ | 2.0molNO,2.0molCO | 1.0molCO2 |
| Ⅱ | 4.0molNO,4.0molCO |
①T3时该反应的平衡常数K=
②平衡时两容器中CO的转化率:Ⅰ
Ⅰ.晶体硅在氧气中燃烧的热化学方程式为
 ,有关键能数据如下表:
,有关键能数据如下表:
(1)已知1mol Si中含2mol Si-Si键,1mol 中含4mol Si-O键,则x的值为
中含4mol Si-O键,则x的值为___________ 。
Ⅱ.对于反应 ,在其他条件不变时,改变其中一个条件则生成Z的速率怎样变化(填“增大”“减小”或“不变”):
,在其他条件不变时,改变其中一个条件则生成Z的速率怎样变化(填“增大”“减小”或“不变”):
(2)①升高温度:___________ ;②增大容器容积:___________ ;③加入X:___________ :
Ⅲ.反应
 ;测得在不同温度下,该反应的平衡常数K值随温度的变化如下:
;测得在不同温度下,该反应的平衡常数K值随温度的变化如下:
(3)若500℃时进行该反应, 起始浓度为2
起始浓度为2  ,CO的平衡浓度为
,CO的平衡浓度为___________ 。
(4)该反应中的a___________ 0(填“大于”“小于”或“等于”)。
(5)700℃反应达到平衡,要使该平衡正向移动,其他条件不变时,可以采取的措施有___________(填序号)。
(6)下列图象符合该反应的是___________ (填字母)(图中v是速率、 为混合物中CO含量,T为温度且
为混合物中CO含量,T为温度且 )
)
A.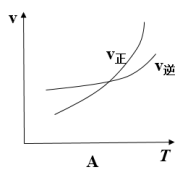 B.
B.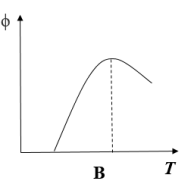 C.
C.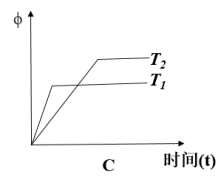
| 化学键 | Si-O | O=O | Si-Si |
| 键能/ | x | 498.8 | 176 |
(1)已知1mol Si中含2mol Si-Si键,1mol
Ⅱ.对于反应
(2)①升高温度:
Ⅲ.反应
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
(4)该反应中的a
(5)700℃反应达到平衡,要使该平衡正向移动,其他条件不变时,可以采取的措施有___________(填序号)。
| A.缩小反应器体积 | B.通入 |
| C.升高温度到900℃ | D.使用合适的催化剂 |
A.
 B.
B. C.
C.
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


